1. 临床资料
患者女,34岁,G1P1,因“剖宫产术后46天,阴道大量流血2天”于2023年10月7日入院。2023年9月22日患者于外院因“孕39周4天、持续性枕横位”阴道试产失败行剖宫产术,产1男婴,手术过程顺利,术后宫缩好,阴道流血少,产后恢复良好。2023年9月21日患者无明显诱因突发阴道大量流血,色鲜红转为暗红,伴血块,约800 ml,伴胸闷、憋气,外院就诊,血常规示血红蛋白75 g/L,予输血浆600 ml、去白红细胞3U、补液等对症支持治疗,予缩宫素促进宫缩、头孢哌酮钠舒巴坦钠抗感染治疗,后复查血常规示血红蛋白86 g/L,好转后出院。2023年10月5日无明显诱因再次出现阴道大量流血,出血量不清,伴头晕、乏力等失血性休克症状,外院就诊血常规示:血红蛋白92 g/L,予去白红细胞2U、血浆400 ml、补液等对症支持治疗,并给予缩宫素促进宫缩、头孢美唑钠预防感染治疗,后复查血常规示:血红蛋白91 g/L,好转后出院。出院后患者仍有阴道少量流血,为求进一步诊治患者于2023年10月7日就诊于我院。妇科检查:外阴发育正常,可见少量暗红色血迹,下腹部可见剖宫产瘢痕,愈合好,宫底腹部未探及,余未见明显异常。入院辅助检查:血红蛋白88 g/L,C-反应蛋白5.09 mg/L,降钙素原0.08 ng/mL,血钾3.2 mmol/L,白蛋白33.7 g/L,余未见明显异常。阴道彩超示:子宫前位,大小约4.72 × 4.02 × 5.56 cm,肌壁回声不均匀,子宫前壁下段回声粗强,左侧壁、右侧壁、前壁见低回声结节,大小分别约1.42 × 1.03 cm、1.48 × 0.88 cm (突向宫腔)、1.51 × 0.87 cm。子宫前壁下段肌层回声不均,右侧壁下段可见一搏动性囊性团块(图1),大小约1.75 × 1.24 cm,突向宫腔下段,壁厚,CDFI:内见红蓝相间血流信号,PW可见双向动脉血流频谱,团块似与右侧宫旁动脉血管相连(图2)。双附件区未见明显异常包块。

Figure 1. Ultrasound shows an anechoic sac in the lower segment of the right uterine wall
图1. 超声示子宫右侧壁下段可见一无回声囊

Figure 2. Color flow and spectral Doppler imaging revealed marked aliasing and bidirectional flow
图2. 彩色血流和频谱多普勒成像显示明显的混叠和双向血流
剖宫产后子宫,右侧壁下段囊性团块,考虑假性动脉瘤可能。2023年10月8日盆腔CTA示子宫右侧高密度影,子宫出血灶可能(图3)。
向患者及家属交代病情及风险,患者及家属表示理解,同意遵介入科会诊介入下盆腔动脉CT血管造影(DSA),如发现出血,要求行子宫动脉栓塞术(UAE)。患者于2023年10月11日局麻下行子宫动脉栓塞术 + 子宫假性动脉瘤栓塞术 + 化学物质栓塞术 + 子宫动脉造影术 + 腹主动脉造影术,术中见右侧子宫动脉可见假性动脉瘤形成(图4)。

Figure 3. Pelvic CTA shows a high-density shadow on the right side of the uterus, and uterine bleeding may occur
图3. 盆腔CTA示子宫右侧高密度影,子宫出血灶可能
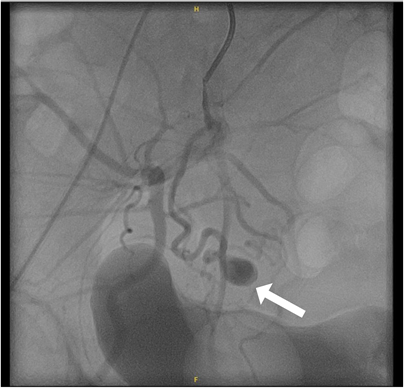
Figure 4. Contrast imaging shows a contrast agent retention mass visible in the pelvic cavity
图4. 造影示盆腔内可见一造影剂滞留团
左侧子宫动脉未见明显出血征象,微导管超选至右侧子宫动脉假性动脉瘤近端,应用约0.6 ml Onyx胶进行栓塞。栓塞后再次造影示假性动脉未见显影,栓塞效果满意(图5)。
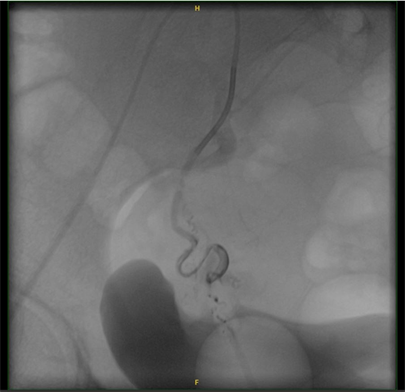
Figure 5. Follow up angiography after right uterine artery embolization shows satisfactory embolization effect
图5. 右侧子宫动脉栓塞后复查造影示栓塞效果满意
手术顺利,术后患者恢复良好。2023年10月12日行下肢血管超声检查示:右侧小腿肌间静脉血栓形成,复查D-二聚体示410 ng/mL,予低分子肝素抗凝治疗,右下肢制动,避免挤捏患肢。术后第2天患者阴道出血停止,术后第30天复查阴道彩超示子宫及双侧附件未见明显异常,嘱出院后继续抗凝治疗1月,出院随访复查下肢血管超声及腹部超声,未见明显异常,目前患者未月经来潮,无特殊不适。
2. 讨论
2.1. 临床特点
产后出血(PPH)指胎儿娩出后24 h内,阴道分娩者出血量 ≥ 500 ml,剖宫产者 ≥ 1000 ml,是分娩严重并发症,我国将产后24 h后至产后6周内发生的生殖道大量出血称为晚期产后出血 [1] 。导致晚期产后出血的原因有很多,如子宫复旧不全、妊娠物质残留、剖宫产切口愈合不良、感染、生殖道血肿等,子宫动脉假性动脉瘤(UAP)是近几年来发生报道率越来越高的导致剖宫产术后晚期产后出血的较为少见的病因 [2] 。子宫动脉假性动脉瘤 [3] 是指由于子宫动脉壁缺陷所导致部分周围血液外渗,受动脉搏动的持续冲击的影响,被周围组织包绕,形成与受损动脉腔相通的血肿样组织或搏动性包块 [2] 。剖宫产术是导致子宫假性动脉瘤最常见妇产科操作 [4] ,其次是经阴分娩及人工流产术。其临床表现缺乏特异性,故极容易被误诊和漏诊,由于UAP仅为一层疏松结缔组织、缺乏正常血管结构,因此发生破裂出血的风险较真性动脉瘤显著增高。若瘤腔与宫腔相通,主要临床症状为阴道大量出血;若瘤腔与腹腔相通,则主要表现为腹腔内出血;若瘤腔因周围组织包绕或血栓形成可致出血停止,瘤腔自行闭合,可无明显不适 [5] 。
2.2. 诊断
对于不明原因的产后出血,应首先排除常见病因,如胎儿附属物残留、感染、子宫复旧不良等,采取常规治疗措施无效则应考虑到子宫假性动脉瘤的可能。结合超声、CT、MRI、数字减影血管造影术(DSA)等检查,可准确诊断本病。经阴道彩色多普勒超声是诊断UAP快速、准确、无创的方法之一。结合现病史及症状,当超声提示子宫内有异常无回声区域时即应考虑到UAP存在的可能。彩色多普勒超声血流显像可观察到红蓝相间的湍流状血流,在子宫动脉动脉裂口即假性动脉瘤的入口颈部可见高速血流频谱,特点为“阴–阳征”:收缩期高速流,舒张期反向中速流的往返血流曲线,这是由于瘤体内和血管内的压力在心动周期的转换造成的压力梯度所致 [6] 。相关文献报道,彩色多普勒超声诊断UAP的灵敏度可达94%,特异度可高达95% [7] 。对于诊断复杂者可加行CT及MRI,增强CT可见明显异常强化UAP瘤体及出血灶,MRI可见T1轻度高信号影,T2不均质低信号,增强扫描强化明显,可显示内部血凝块影 [2] 。血管造影(DSA)是诊断子宫假性动脉瘤的金标准,它不仅用于诊断,也可直接指导子宫假性动脉瘤的栓塞治疗 [8] 。但是如果UAP中有血栓形成,瘤腔被填充,无活动性出血,DSA也可呈现假阴性结果。Yahyayev等 [9] 曾报道1例DSA造影结果呈阴性,后经阴道多普勒彩色超声证实为UAP瘤腔内血栓形成,瘤腔被血栓全部填充,造成假阴性结果。因此,多普勒彩色超声检查结合DSA对于UAP的诊断是必要的。
2.3. 鉴别诊断
UAP需与其他子宫血管异常如子宫动静脉瘘(UAVF)等相鉴别。子宫动静脉瘘(UAVF)是指子宫动脉分支与子宫静脉丛之间形成的异常直接交通的血管病理性病变,属于子宫动静脉畸形 [10] 。UAP和UAVF在超声及MRI等有明显鉴别点。UAP彩色多普勒超声可见“阴–阳征”;而UAVF表现为连续性血流流速曲线改变,可见混乱呈五彩镶嵌状的湍流血流,其内血流呈高速低阻,动脉内为单向或双向血流,静脉血流动脉化 [11] 。对于原因不明的产后出血,应考虑到本病的同时,可借助彩超、CTA等辅助检查,与其他疾病进行鉴别诊断。
2.4. 治疗
治疗UAP的主要方法有期待治疗、选择性子宫动脉栓塞术及开腹手术等,其中选择性动脉栓塞术是该病的一线治疗方法,应结合患者病情、生育情况、意愿、医疗水平及健康情况等多方面因素来综合考虑患者的治疗方案。
2.4.1. 期待治疗
部分无明显临床症状、风险较低的子宫假性动脉瘤患者,可行期待治疗 [3] ,Takahashi等人曾报道了3例自发缓解的病例,并指出症状很少或无症状的小直径UAP病例可在严密观察下行期待治疗 [12] ,但也有研究发现UAP破裂的风险并不一定和其直径大小呈正相关。Wu T等人 [3] 发现,UAP破裂患者的肿块并不大于未破裂患者的肿块。另外,破裂也会导致肿块直径缩小。
2.4.2. 选择性动脉栓塞术
Kulkarni S等人发现,子宫动脉假性动脉瘤栓塞治疗更容易识别出血部位,缩短住院时间,保持生育能力,选择性子宫动脉栓塞术是治疗子宫动脉假性动脉瘤较为安全有效的一线方法 [13] 。主要优点在于侵入性小、可快速控制出血、复发率低、成功率高、安全性高、可保留生育功能,而且即使栓塞术失败,仍可采用动脉结扎及子宫切除术等其他治疗方法 [7] 。栓塞术失败的主要常见原因在于栓塞不彻底,不能将UAP的所有供血动脉全部阻断,遗漏对侧子宫动脉侧支供血或卵巢动脉等其他交通支供血,Cooper等人曾报道1例在单侧子宫动脉栓塞后,由于侧支供血,不得不重复栓塞对侧血管的病例,这提示双侧子宫动脉栓塞可能比单侧栓塞更有效 [14] 。因此目前大多数学者提倡在DSA下对UAP可能存在的双侧供血动脉进行栓塞。患者在栓塞治疗后立即复查彩色多普勒超声,每3月复查1次,连续随访3年。
2.4.3. 手术
UAP的手术方式主要包括子宫动脉结扎及全子宫切除术等。在病情稳定情况下,大多数学者推荐首选选择性子宫动脉栓塞术,在选择性子宫动脉栓塞术失败或者急性大出血病情危急等情况下,则可采用手术治疗 [2] 。据文献报道,动脉结扎在治疗产后出血的有效率在42%~100%不等 [2] ,差异较大,考虑子宫动脉结扎术后再次进行动脉栓塞操作较为困难,实际可操作性差,故应先考虑行选择性动脉栓塞术,如失败则可再考虑行选择性子宫动脉结扎术。Alboni C等 [15] 曾报道1例剖宫产术后因子宫动脉假性动脉瘤致晚期产后出血行选择性动脉栓塞术失败后再次急诊入院行全子宫切除术的病例。
总之,UAP是一种发病率较低的妇产科手术操作并发症。与子宫动脉假性动脉瘤相关的常见妇产科操作有:剖宫产术、剖腹或腹腔镜下子宫肌瘤剔除术、全子宫切除术、宫颈锥切术、人工流产术、诊断性刮宫术等。大多数学者认为与子宫动脉的损伤史有关,但仍有部分患者无明确子宫动脉损伤病史。临床上主要常见症状表现为阴道流血,部分病例无特殊症状。Baba等人 [16] 研究提示UAP的破裂可能与UAP内血流/压力比值以及瘤壁强度之间的平衡有关,并提出“舒张期血流缺失”可作为影响UAP预后的指标之一。血流/压力和UAP瘤壁强度,是否可以作为预测UAP分辨率的候选指标,有待进一步研究,但可提示我们在未来可将UAP内血流/压力和UAP瘤壁强度作为一种常规检查手段来帮助预测UAP破裂风险。彩色多普勒超声、CT等可对该疾病进行诊断,DSA被认为是诊断该疾病的“金标准”,并可为行选择性动脉栓塞术提供依据。
参考文献
NOTES
*通讯作者。