1. 引言
恶性肿瘤,即癌症,仍是全世界的一个主要死因 [1] 。据世界卫生组织报告,每年将近1000万例的死因由癌症所引起。目前临床上广泛采用手术疗法、化学治疗、放射治疗及分子靶向治疗等方法治疗癌症。治疗肿瘤的难点不仅在于肿瘤的强侵袭性、强播散性、易转移性,且还在于化疗药物缺乏选择性并且会导致许多毒副作用 [2] 。光热转换疗法是(Photothermal therapy, PTT)是近年来迅速发展起来的一种肿瘤微创治疗技术,其基本原理是在入射光激发下,靶向肿瘤部位的光吸收剂利用其光热转换效应产生大量热量,可以使肿瘤组织局部升高并达到一定温度(通常温度迅速升高到48℃以上),致使肿瘤细胞的损伤以及热消融,从而达到杀死肿瘤细胞的目的。随着纳米技术的快速发展,纳米药物已为实时监测和治疗癌症细胞创造了平台。研究人员们研发出了各种用于核磁共振、近红外荧光成像、光声成像和其他检测肿瘤的成像技术的纳米技术平台。研究表明,具有良好光热转换特性的材料,即光热转换剂(PTA),可尝试应用于肿瘤的光热治疗中,但需要具有低毒性和良好生物相容性等特点。在近红外光范围具有良好吸收性能的纳米材料已被用于肿瘤光热治疗,并取得了一定的进展,如金纳米材料 [3] [4] [5] 、碳纳米材料 [6] [7] [8] 、近红外辐射吸收的有机小分子 [9] [10] [11] 等。
聚多巴胺(PDA)作为一种常见的纳米材料,具有优良的物理和化学特性,如金属离子螯合、光热转换、高分散性、良好的生物相容性和降解性;同时具有很好的包覆能力,可负载大量药物;表面含有大量的官能团,使其容易吸附于药物或进行功能化修饰以提高靶向肿瘤细胞的能力,还降低了纳米材料的细胞毒性。目前已被广泛用于生物医学领域,如生物传感、药物载体、生物成像、组织工程和抗菌剂等 [12] [13] [14] [15] [16] 。基于此,在本研究中,我们基于盐酸多巴胺在碱性条件下氧化自聚合制备纳米材料的方法制备PDA纳米颗粒,再利用乙二胺诱导降解PDA纳米颗粒,最终得到荧光聚多巴胺纳米粒子(FPNPs)。该纳米粒子具有较高光热转换效率,并对其在肿瘤细胞成像与光热治疗方面的应用进行了较为深入的研究。
2. 实验部分
2.1. 仪器与试剂
扫描电子显微镜(ZEISS Gemini SEM 300);共聚焦超高分辨显微镜(TCS SP8 STED 3X);紫外–可见吸收光谱(UV-Vis);傅立叶转换红外光谱仪(FTIR);酶标仪(Multiskan FC);荧光光谱仪(Cary Eclipse);红外热成像相机(Fotric 220)。
盐酸多巴胺,三羟甲基氨基甲烷(Tris),乙二胺(EDA),青霉素–链霉素溶液(100X),胎牛血清,DMEM高糖,噻唑蓝(MTT),二甲基亚砜(DMSO),磷酸盐缓冲液(PBS 1X),细胞活性与细胞毒性检测试剂盒,无水乙醇等均为分析纯购买自上海阿拉丁试剂有限公司;实验所用均为去离子水。
2.2. FPNPs纳米粒子的合成及光热性质表征
2.2.1. 聚多巴胺(PDA)纳米颗粒的合成
将称量好的40 mg盐酸多巴胺溶于15 mL去离子水中,随后加入20 mL无水乙醇溶液,利用超声波清洗器振荡混匀。将30 mg三羟甲基氨基甲烷(Tris)溶于10 mL去离子水中,振荡混匀。将两种溶液混合在一起,转移到锥形瓶中,并放入磁子,室温下500 rpm磁力搅拌24 h。反应过程中,透明无色溶液逐渐变为黑色。用滴管移取反应液20 mL于半透膜中,去夹子封住半透膜。烧杯中加入适量去离子水,再放入封好的半透膜和磁子,在500 rpm下纯化三天。最后对中间产物的纯化产品进行冻干,得到聚多巴胺纳米粒子。
2.2.2. 荧光聚多巴胺纳米颗粒(FPNPs)的合成
将上述未纯化的含有中间产物的溶液中继续加入2 mL乙二胺(EDA),在室温下500 rpm搅拌24 h,可观察到溶液逐渐由黑色变为棕褐色。用滴管移取反应液20 mL于半透膜中,取夹子封住半透膜。烧杯中加入适量去离子水,再放入封好的半透膜和磁子,在500 rpm下纯化三天。最后对最终产物的纯化产品进行冻干,得到FPNPs。
2.2.3. FPNPs光热转换性能测试
用波长为808 nm的激光(1 W/cm2)照射不同浓度的FPNPs溶液和PDA溶液,以纯水为对照,照射时间为7 min,每隔30 s测试一次溶液的温度,并用红外热成像仪记录下不同时间点纯水、FPNPs溶液和PDA溶液的温度变化情况。同时,为了进一步研究具有近红外吸收的FPNPs光热效应稳定性,用激光照射FPNPs溶液(0.3 mg/mL) 5 min,每隔30 s测试一次溶液温度,待溶液温度冷却至室温,再次打开激光,重复上述步骤,激光开/关四次以测定材料的光热循环稳定性能。
2.2.4. 细胞毒性及活性实验
在96孔板中接种培养的HeLa细胞,每孔加液量100 µL,边缘孔用无菌PBS填充,细胞在37℃,5% CO2培养箱内培养12 h后,完全贴壁,第二天更换新鲜的培养基,每孔加入50 µL的新鲜培养液和50 µL含有浓度为100 µg/mL的FPNPs,另一个培养基中加入50 µL的新鲜培养液和50 µL含有浓度为100 µg/mL的PDA,在培养箱内继续培养12 h。对FPNPs和PDA组给予808 nm (2.0 W/cm2)的激光照射10 min,激光照射结束后,细胞继续培养24 h。配置5 mg/mL的MTT溶液,吸去培养上清液后,每孔中加入90 µL培养基,再加入10 µL MTT溶液,于培养箱内继续培养4 h。终止培养,小心吸去孔内上清液,每孔中加入100 µL的DMSO,慢慢振荡10 min,使其充分溶解。在酶标仪OD 490 nm处测量各孔的吸光值,以它的吸光度记为100%,计算Hela细胞经FPNPs、PDA培养后的细胞存活率。
2.2.5. 细胞死活染色实验
将HeLa细胞接种于6孔板,培养24 h。用含有FPNPs、PDA (分别为100 µg/mL)的新鲜培养基代替旧培养基,共培养4 h。利用PBS小心冲洗细胞,加入新鲜的DMEM培养基,给予细胞激光照射。培养24 h后,用PBS轻轻冲洗细胞,吸去的DMEM,用含培养基的Calcein AM和PI溶液(每孔1 mL)孵育30 min。具体的Calcein AM/PI染色工作液如下:将1 µL的Calcein AM溶液(1000X)和1 µL的PI (1000X) 加入10 mL的Assay Buffer (1X)中(用Calcein AM将活细胞染成绿色,用PI将死亡细胞染成红色)混合均匀。然后,每孔加入1 mL Calcein AM/PI染色工作液,放到培养箱内孵育30 min后,用新鲜PBS洗涤3次,通过荧光显微镜观察成像。
3. 结果与讨论
3.1. PDA和FPNPs纳米颗粒的形貌与组成表征
PDA纳米粒最初是通过前驱体分子多巴胺在Tris缓冲溶液中的自聚合得到的。如图1(a)、图1(b)所示,PDA颗粒的形态主要由尺寸为150 nm~200 nm的球形结构组成。形成FPNPs过程中可以清晰看到得到的纳米颗粒的粒径明显减小,且观察到FPNPs尺寸分布均一(如图1(c)、图1(d)。说明PDA通过加入乙二胺有效分解形成具有良好水溶性的FPNPs,从而使其适合于各种有机、聚合物、无机或生物物种的功能化。

Figure 1. (a), (b) SEM images of PDA nanoparticles; (c), (d) SEM images of FPNPs nanoparticles
图1. (a)、(b) PDA纳米颗粒的扫描电镜照片;(c)、(d) FPNPs纳米颗粒的扫描电镜照片
3.2. PDA和FPNPs纳米颗粒的光学性质表征
我们详细研究了所制备的纳米颗粒的光学性质。将制备的PDA纳米颗粒分散在水溶液中,紫外光下溶液出现蓝色(图2中的插图)。在图2(a)中,紫外–可见–近红外光谱图显示,FPNPs在紫外区域显示明显的光吸收,尾部延伸到可见范围,其肩部在350 nm~400 nm处观察到。在经过表面原位聚合多巴胺壳层过后,纳米颗粒的水分散液的颜色便由原来的蓝色变为了浅绿色。基于FPNPs优异的荧光稳定性和生物相容性,我们对不同浓度的FPNPs溶液通过荧光光谱仪扫描后得到谱图如图2(b)所示,结果显示FPNPs的荧光强度随浓度升高而增强。
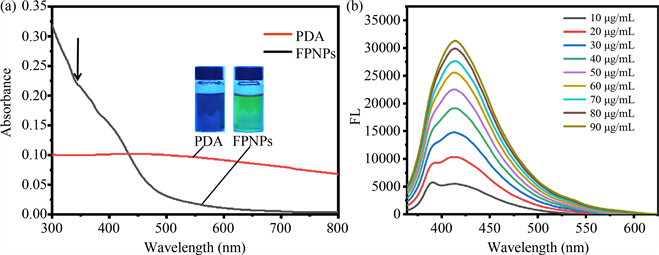
Figure 2. (a) UV-vis-NIR absorbance spectra of PDA and FPNPs aqueous solutions; (b) FL emission spectra of FPNPs with different concentrations: 10, 20, 30, 40, 50, 60, 70, 80, and 90 µg/mL
图2. (a) PDA和FPNPs的水溶液的紫外–可见–近红外光谱;(b) 不同浓度FPNPs溶液的荧光光谱,从下到上FPNPs的浓度为:10、20、30、40、50、60、70、80和90 µg/mL
3.3. FPNPs纳米颗粒的光热性能研究
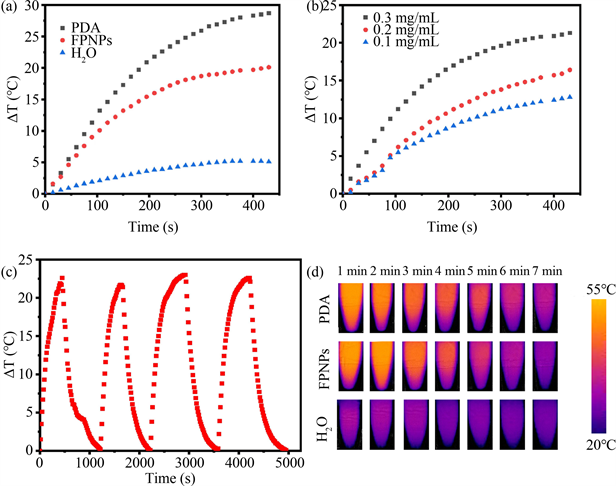
Figure 3. (a) The temperature elevation of 0.3 mg/mL PDA solution, FPNPs solution and deionized water under 808 nm laser irradiation with 1.0 W/cm2; (b) Temperature change curves of FPNPs dispersions with different concentrations under 808 nm laser irradiation at a power density of 1.0 W/cm2; (c) Temperature curves of FPNPs with concentrations of 0.3 mg/mL for four laser on/off cycles; (d) Photothermal images of 0.3 mg/mL of PDA solution, FPNPs solution and pure water exposed to 808 nm laser (1.0 W/cm2) recorded at 7 min
图3. (a) 0.3 mg/mL的PDA溶液和FPNPs溶液以及去离子水在808 nm激光(1.0 W/cm2)照射下的升温曲线;(b) 不同浓度的FPNPs溶液在808nm激光(1.0 W/cm2)照射下的升温变化曲线;(c) 浓度为0.3 mg/mL的FPNPs溶液在激光开/关四次循环照射下的温度变化曲线;(d) 浓度为0.3 mg/mL的PDA溶液、FPNPs溶液和纯水在808 nm激光(1.0 W/cm2)照射7 min内的红外热成像照片
由于FPNPs具有良好的光热转换效率,接下来研究了其光热性能。如图3(d)所示,为了研究FPNPs的光热转换效率,使用了808 nm的近红外激光照射不同浓度的FPNPs溶液,照射时间为7 min,激光密度为1.0 W/cm2,同时用纯水作为对照组。将FPNPs溶液、PDA溶液及去离子水在连续红外激光照射7 min后使用红外热成像相机测试溶液温度变化情况。结果显示在808 nm的近红外光照射下,在FPNPs溶液中,温度从22.0℃上升到43.9℃,而在PDA溶液中,温度从22.0℃上升到55℃,相比之下,纯水温度的变化可以忽略不计,只增加了5.1℃ (图3(a))。在照射时间为7 min的情况下,在同等激光功率照射条件下,FPNPs溶液的温度随着浓度的增加而升高(图3(b))。为了进一步研究具有广泛近红外吸收的FPNPs光热效应稳定性,记录了FPNPs溶液(0.3 mg/mL, 1.0 mL)的加热和冷却曲线(图3(c))。经过四次激光照射升温循环实验后,每次溶液的温度变化基本一致,表明FPNPs具有良好的光热转换稳定性。以上实验结果表明,FPNPs纳米粒子具有良好的光热转换效率,可作为一种潜在的肿瘤近红外光热治疗剂。
3.4. FPNPs纳米颗粒的肿瘤细胞光热治疗研究
MTT检测结果如图4(a)所示,可以观察到在HeLa细胞在FPNPs中孵育24 h后存活率仍保持在95%,而在PDA中孵育24 h后存活90%。经808 nm激光照射后FPNPs组、PDA组的细胞存活率保持在40%以下,表明FPNPs、PDA在经激光照射后对肿瘤细胞具有光热杀灭性能。为了研究FPNPs的荧光成像,将HeLa细胞分别与FPNPs、PDA预孵育4 h,然后进行荧光成像。FPNPs组和PDA组的荧光图像如图4(b)所示,显然,经PDA处理的细胞没有检测到任何荧光,而经FPNPs处理的细胞获得明显的绿色荧光。表明FPNPs纳米颗粒被肿瘤细胞摄取后表现出低细胞毒性,且可用于细胞的荧光成像。
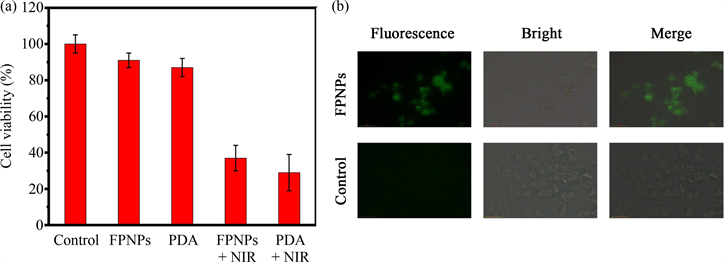
Figure 4. (a) The activity of HeLa cells after different treatments; (b) Fluorescence imaging of HeLa cells treated by FPNPs and PDA
图4. (a) 经不同处理后HeLa细胞的活性;(b) HeLa细胞经FPNPs、PDA处理后的荧光成像
4. 结论
在本文中,通过多巴胺在碱性条件下氧化自聚合生成聚多巴胺,并以乙二胺对聚多巴胺进行诱导降解,制备出了具有荧光特性的FPNPs纳米粒子。以此方法制备的FPNPs纳米粒子结构更稳定,其高水溶性使得在实际生物医学应用具有广阔的应用前景,且FPNPs纳米粒子具有很高的光热转换效率,可用于肿瘤细胞的光热治疗以及实时的荧光监测等。
基金项目
本项目由国家自然科学基金(批准号:22007052),以及国家级大学生创新创业项目(202310304025Z)支持。
NOTES
*通讯作者。