1. 引言
盐酸羟胺是羟胺系列产品中重要的化工原料和有机合成中间体,广泛用于作为还原剂和羰基化合物制备肟 [1] 。尤其在合成尼龙有机化工产品中,盐酸羟胺合成环已酮肟 [2] 再合成环已酰胺单体再合成尼龙产品。化工反应中羟胺进行肟化反应时,过量的羟胺会被一次性加入,这就会导致反应完全后的废水中会残留不同浓度的羟胺废水。羟胺废水中有机物成分多造成水质中COD含量高。同时羟胺中的氨氮在水体中是以游离态的形式存在,高氨氮、高COD成分是引发水质富营养化和造成环境污染的重要原因。针对废水单一高氨氮或者高COD特性,目前研究发现催化湿式氧化法处理效果最好,但是由于反应体系为高温高压,在废水中由于组成成分或有硝酸盐,这就造成极大的安全隐患,安全风险系数太高 [3] 。生物降解法对高氨氮、高COD废水适用性太小,目前处理废水中COD控制2000 mg/L,氨氮控制200 mg/L以下的活性细菌是比较通用的 [4] 。离子交换法、液膜法、电化学法处置高氨氮、高COD废水效果很好,但是处置成本太高,不适合规模化处置。而化学氧化还原法中芬顿试剂处置对高COD废水的降解效果很好,对于氨氮用芬顿试剂处置效果有限不适用。
因此要实现化工合成中羟胺废水的规范处置,关键之一就是实现废水中高氨氮的有效处理。通过研究发现羟胺废水中铵根离子是与羟基结合固定的,而其他废水中铵根离子是游离的,三价铁能有效地与羟胺催化反应去除,而芬顿试剂中能源源不断地产生三价铁。因此采用芬顿氧化技术处理羟胺废水为实际可行的有效方法。本文实验研究了芬顿试剂(硫酸亚铁和双氧水)配比、不同温度、反应时间时长、pH值、加入方式等关键影响因子对于废水处理的影响,找出最佳优化参数,实现酸性高浓度氨氮、COD废水的高效处置。
2. 实验部分
2.1. 实验的材料与装置
实验材料:安徽某尼龙公司产生的酸性高氨氮COD废水。废水的理化性质为COD = 100000~150000 mg/L;TDS = 500~700 mg/L;氨氮 = 1000~2000 mg/L;pH ≤ 1。
实验试剂:40% NaOH溶液(由分析纯氢氧化钠固体和蒸馏水配置)、30%双氧水溶液(分析纯)、硫酸亚铁溶液(由分析纯硫酸亚铁固体和蒸馏水配置)。
实验装置:自动电子搅拌装置、搅拌粒子、3口500 ml玻璃平底烧瓶、有刻度的滴液漏斗、恒温装置。
实验设备:Multiskan SkyHigh全波长酶标仪,厂家赛默飞;多pH计量器,厂家梅特勒托利。
2.2. 实验步骤
取250 ml的酸性高氨氮COD废水(以下简称“废水”),先利用恒温装置控制反应体系温度在恒定温度保持不变,其次加入配好的40%氢氧化钠溶液调节体系pH达到所需要求,再次芬顿试剂(30%双氧水和配比硫酸亚铁溶液)进行氧化还原反应处置,反应时间x h,氧化还原处置后的溶液最后加入40%氢氧化钠溶液调节反应体系pH为7,测试处置废水中氨氮、COD含量。
3. 优化条件参数
3.1. 芬顿试剂(30%双氧水和配比硫酸亚铁溶液)配比——摩尔比对废水中氨氮和COD去除的影响
控制其他反应参数恒定:pH = 3,温度T = 40℃,反应4 h。变动的反应参数:芬顿试剂配比(过氧化氢:铁)分别为1:1,4:1,8:1,12:1,16:1,20:1,测试处置后废水中氨氮、COD含量。

Table 1. Effect of different Fenton reagent ratio (molar ratio) on removal of ammonia nitrogen and COD
表1. 不同芬顿试剂配比(摩尔比)对氨氮、COD去除的影响
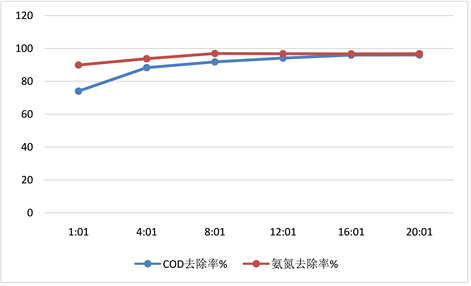
Figure 1. Effect of different Fenton reagent ratio (molar ratio) on removal rate of ammonia nitrogen and COD
图1. 不同芬顿试剂配比(摩尔比)对氨氮、COD去除率的影响
见表1数据分析可知,芬顿试剂配比(过氧化氢:铁)为16:1时,废水检测数据中COD、氨氮去除率达到最高值见图1。FeSO∙7HO的加入量过低或过高,氧化还原处理效果均会有不同程度下降。其原因是Fe2+是催化产生单位量HO产生的羟基自由基增加,而自由基参与了与有机物的反应;当Fe2+的浓度过低时产生的羟基自由基偏低,进而影响氧化还原反应,Fe2+的浓度过高时,会加快H2O2发生无效分解,释放出氧气,也影响氧化还原反应。Fe2+催化氧化羟胺中氨氮的分解,因此随着Fe2+的浓度的增加会加速羟胺中氨氮,进而达到一定值就不再催化氧化。
反应机理 [4] [5] :
3.2. pH值对COD、氨氮去除率的影响
控制其他反应参数恒定:芬顿试剂摩尔配比(过氧化氢:铁)为16:1,温度T = 40℃,反应4 h。变动的反应参数:调节pH至2,3,4,5,6,7,加入,测试处置后废水中氨氮、COD含量。

Table 2. Effect of pH value on removal of ammonia nitrogen and COD
表2. pH值对氨氮、COD去除的影响

Figure 2. Effect of pH value on removal rate of ammonia nitrogen and COD
图2. pH值对氨氮、COD去除率的影响
见表2数据可知,控制反应体系中pH值的升高,COD的去除率会出现先升高后降低的现象。当pH值从1到4时的,COD的去除率急速上升,当pH值为3时去除率达到最大见图2值,COD的降解率为96.03%,当pH值大于4后,COD去除率明显出现缓慢趋势,尤其是在当pH值大于5后,去除率下降趋势特别明显。分析原因反应体系在强酸时,体系中存在大量H+,H+极易与∙OH发生反应,进而造成∙OH无效分解 [5] 。随着pH值的逐渐上升,反应体系中H+适中,从而使得H+的限制慢慢消失,在pH值为3时,COD去除率达到最佳。当pH值在4之后,COD去除率缓慢下降,这是Fe2+催化活力逐渐下降导致,根据Ksp,Fe在pH偏中性将逐渐形成Fe(OH)3沉淀或铁的复杂络合物。
随着pH值的升高,氨氮的去除率逐渐上升。pH在2~4之间时氨氮的去除率较大,当pH值为3时去除率达到最高见图2。而当pH较高高于5后,Fe将形成Fe(OH)3沉淀或铁的复杂络合物,而失去催化能力,但是随着pH升高,废水中氨氮气体溢出增加,尤其pH到7时,氨氮气体溢出最为明显。虽然pH值的升高,氨氮去除率升高见图2,但是有部分氨氮气体溢出,因此不能作为氨氮氧化去除的依据。
3.3. 温度和时间对氨氮COD去除率的影响
控制其他反应参数恒定:加入芬顿试剂摩尔配比(过氧化氢:铁)为16:1,pH = 3,反应4 h。变动的反应参数:控制起始反应温度到10℃,20℃,30℃,40℃,50℃,60℃,反应时间分别为60 min,120 min,180 min,240 min,300 min,360 min,测试处置后废水中氨氮、COD含量。

Table 3. Effect of reaction temperature and reaction time on COD removal
表3. 反应温度和反应时间对COD去除的影响

Figure 3. Effect of reaction temperature and reaction time on COD removal rate
图3. 反应温度和反应时间对COD去除率的影响

Table 4. Effect of reaction temperature and reaction time on removal of ammonia nitrogen
表4. 反应温度和反应时间对氨氮去除的影响
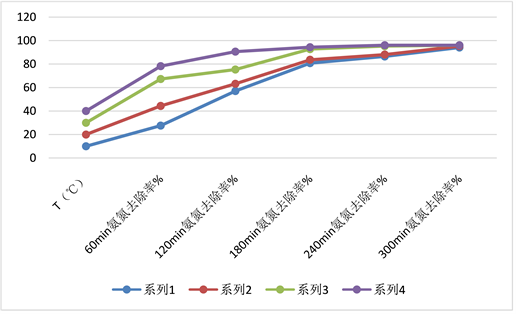
Figure 4. Effect of reaction temperature and reaction time on removal rate of ammonia nitrogen
图4. 反应温度和反应时间对氨氮去除率的影响
见表3和见表4中数据分析,控制反应体系温度在40℃之前,随着的温度的不断提升,废水中氧化还原的反应有明显加强,废水中COD的去除率不断上升见图3。而在温度高于40℃时,促进作用趋缓,不利于有机物的降解。分析原因时,局部升高温度时,温度会催化过氧化氢产生大量羟基自由基,羟基自由基加强了催化氧化反应的进行 [5] [6] ,但是超过40℃,过氧化氢分解反应大于羟基自由基产生反应,不利于催化氧化反应的进行。但温度高于40℃时,羟胺废水易爆沸,有安全风险,也不利于反应的进行。
见表3和见表4中数据分析,反应时间对于反应有着至关重要的作用。表中数据表面在氧化还原的起始阶段的反应速率非常迅速:前120 min内,COD的去除率不断提高见图3,整个反应速率基本稳定,大量的氨氮、有机物被氧化 [6] ,反应体系中氢离子、双氧水和硫酸亚铁的浓度足以维持较快的反应速率。当时间超过120 min后,有机物的去除效果有缓慢趋势,从表中数据分析,废水中氨氮、COD被氧化还原完成了80%见图3和见图4。因此根据以上数据分析结论:此类高氨氮COD废水中氧化还原反应进行的程度,在反应速率一定的情况下,直接受制于反应时间的长短。
3.4. 不同加入方式对氨氮、COD去除率的影响
控制其他反应参数恒定:加入芬顿试剂摩尔配比(过氧化氢:铁)为16:1,pH = 3,温度T = 40℃,反应4 h。变动的反应参数:加入方式,加入方式1:先加入硫酸亚铁,再加入双氧水;加入方式2:先加入双氧水,在加入硫酸亚铁;加入方式3:先加入硫酸亚铁,滴加双氧水;加入方式4:配置硫酸亚铁溶液后,先加入双氧水,再滴加硫酸亚铁溶液;加入方式5:同时滴加硫酸亚铁和双氧水溶液。

Table 5. Effects of different adding methods on removal of ammonia nitrogen and COD
表5. 不同加入方式对氨氮、COD去除的影响
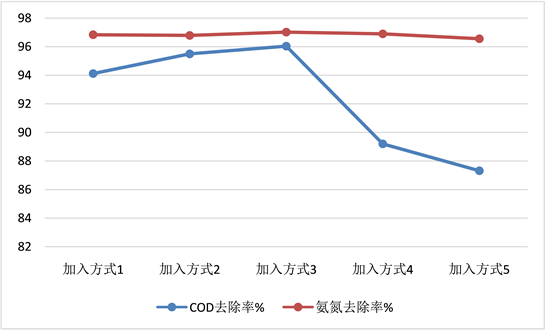
Figure 5. Effects of different addition methods on removal rates of ammonia nitrogen and COD
图5. 不同加入方式对氨氮、COD去除率的影响
见表5数据分析,投加方式3对于COD的去除率效果最好,其原因是先加入硫酸亚铁后再H2O2分批滴加时,[H2O2]/[Fe]相对比例降低 [7] ,即催化剂浓度相对提高,从而催化氧化产生使羟基自由基增加,羟基自由基是氧化能力重要指标,从而了提高H2O2的利用率,最终强化了氧化效果见图5。投加方式对于氨氮的去除无任何影响见图5。
3.5. 优化条件下氨氮、COD的去除率
根据以上反应参数,设定反应体系pH = 3,温度为40℃,芬顿试剂配比(过氧化氢:铁摩尔比)为16:1,加入方式:先加入硫酸亚铁,滴加双氧水,反应时间为240 min,对废水进行氧化还原实验。

Table 6. The removal rates of ammonia nitrogen and COD were optimized
表6. 优化条件下氨氮、COD的去除率
见表6不同实验优化条件下对高浓度氨氮COD废水进行处理后,氨氮、COD被去除96%,经脱盐处理后再进行生化处置后,达标排放,实现了羟胺废水的最终处置。
4. 结论
(1) 酸性高氨氮COD废水氧化还原处置的主要影响因素有芬顿试剂H2O2和Fe2+摩尔比、反应时间和温度、pH值、投加方式等。
(2) 对于氨氮为1745 mg/L,COD为13200 mg/L的酸性高氨氮废水,Fenton试剂法的最佳操作条件为:芬顿试剂配比(过氧化氢:铁)为16:1,芬顿试剂投加方式:先加入硫酸亚铁,滴加双氧水,体系pH值为3,反应时间为240 min,起始温度为40℃。在此条件下清洗溶剂废水最大去除率达到了96%。