1. 引言
肝细胞癌(HCC)是一种恶性程度极高的癌症,几乎占原发性肝癌的95% [1] 。根据最新的全球癌症统计数据显示,全球报告了约84万例肝癌新发病例和78万例死亡病例,分别占所有癌症病例和死亡病例的4.7%和8.2% [2] 。尽管许多患者在早期获得了有效的诊断和治疗,但复发率仍然很高,5年生存率仅为5% [3] 。因此,尽管阐明了HCC的发病机制,但其预后仍然很差 [4] 。因此,迫切需要寻找早期诊断和预后标志物和精准治疗策略,以改善肝癌患者的预后和生活质量。
细胞焦亡是一种新的程序性细胞死亡形式,其特征是细胞肿胀,大气泡从质膜吹出 [5] 。Gasdermin家族蛋白是执行焦亡的关键蛋白,GSDME (DFNA5)是Gasdermin (GSDM)家族成员之一,GSDME (DFNA5)最初称为常染色体显性耳聋5基因,是在染色体7p15.3上发现的一种特殊形式的常染色体显性、进行性、感觉神经性和非综合征性耳聋 [6] 。一方面,GSDME在一部分癌症中低表达,并且GSDME表达水平降低也与生存预后降低相关,表明GSDME可能作为抑制因子起到抑癌作用 [7] 。然而,另一方面,GSDME在部分癌症中表达上调,并且GSDME表达水平升高也与生存预后较差相关 [8] [9] 。随着研究的深入,GSDME在癌症中的作用越来越突出。目前GSDME的结构和功能研究也已在各种癌症中从生理学和病理学方面进行;然而,从目前公开的临床资料来看,GSDME在肝癌中的临床意义尚未完全清楚 [9] [10] 。
我们的研究首次利用TCGA等公共数据库对GSDME进行了多组学系统分析,包括GSDME的表达、临床生存预后、免疫细胞浸润和免疫治疗检查点等一系列相关研究,总体而言,我们的研究揭示了GSDME在肝癌进展的新视角,并为治疗肝癌提供了潜在的靶点分子。
2. 资料与方法
2.1. GSDME基因表达的分析
在这项研究,我们首先运用基于TCGA的TIMER数据库(https://cistrome.shinyapps.io/timer/)分析了32中常见癌症的GSDME基因表达 [11] 。GEPIA (http://gepia.cancer-pku.cn/)是一个交互式在线网络工具,我们用于分析来自TCGA和GTEx项目的肝癌组织样本的GSDME差异表达 [12] 。UALCAN (https://ualcan.path.uab.edu/)是一个基于TCGA的网站,可以用来分析肿瘤和正常组织的相对基因表达,以及基于种族、肿瘤分级和组织分级的相对基因表达和其他临床病理特征 [13] 。在这项研究中,该数据库用于探索GSDME在肝癌中不同肿瘤等级中的mRNA表达和蛋白表达。
2.2. GSDME基因在肝癌中的生存分析
Kaplan-Meier生存数据库(http://kmplot.com/analysis/)提供了10461个样本的数据分析,包括胃癌、乳腺癌和HCC样本等等 [14] 。我们根据不同的临床病理变量,探讨GSDME的表达与LIHC临床预后的关系,并计算出95%可信区间的危险比(HR)和对数等级P值。
2.3. 免疫浸润和相关免疫检查点分析
TIMER2数据库(http://timer.cistrome.org/)分析靶基因表达与免疫细胞临床相关性的关系。在这项研究中,我们研究了GSDME的mRNA表达与肿瘤浸润免疫细胞之间的相关性,包括B细胞、CD4+T细胞、CD8+T细胞、中性粒细胞、巨噬细胞、和自然杀伤细胞(NK)。我们还使用TIMER2探讨了GSDME表达与免疫检查点相关基因表达之间的相关性,主要为程序性细胞死亡蛋白1 (PD-1)-PDCD1、细胞毒性T淋巴细胞相关蛋白4 (CTLA4)和程序性细胞死亡配体1 (PD-L1)-CD274基因。
2.4. GSDME蛋白的免疫组织化学染色结果分析
为了观察GSDME蛋白在LIHC组织中的表达情况,我们利用HPA蛋白图谱 (https://www.proteinatlas.org/),观察GSDME蛋白的病理变化。这是研究蛋白质在人体组织和细胞中定位和表达的宝贵资源 [15] 。在我们的研究中,HPA011326抗体用于染色,免疫组织化学检测的蛋白表达水平分为强、中、弱或阴性。
3. 结果
3.1. GSDME在肝细胞癌中表达上调
根据Timer2.0数据库的分析结果,我们发现GSDME mRNA在多种癌症中都有上调表达,包括胆管癌、头颈鳞状细胞癌、肾癌、肺鳞癌、胰腺癌和肝细胞癌(图1)。为了验证数据库中的结果,我们运用GEPIA和UALCAN进一步研究了GSDME在肝癌中的表达,我们发现GSDME mRNA在癌组织中的表达显著高于癌旁组织(图2(A)和图2(B)),GSDME的蛋白表达在肝癌细胞中的表达高于在正常肝组织中的表达(图2(C))。*P < 0.05,**P < 0.01,***P < 0.001。

Figure 1. The expression map of GSDME gene in pan-cancer
图1. GSDME基因在泛癌中的表达图
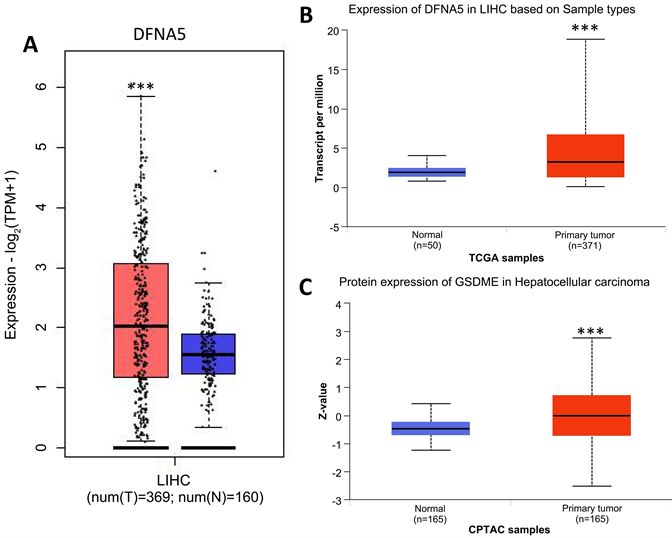
Figure 2. The expression map of GSDME gene in liver cancer
图2. GSDME基因在肝癌中的表达图
3.2. GSDME表达与肝癌进展相关
随后,利用UALCAN数据库分析,发现GSDME的表达与肝癌的分级分期、TP53突变和淋巴结转移状态显著相关(图3)。以上结果均提示GSDME在肝细胞癌中异常表达,可作为肝细胞癌进展的生物标志物。

Figure 3. The expression map of GSDME gene in HCC subgroup stratification
图3. GSDME基因在HCC亚组分层中的表达图
3.3. GSDME表达与肝癌患者预后密切相关
采用Kaplan-Meier生存曲线分析GSDME表达与肝癌患者临床预后的关系。结果表明,GSDME的表达与肝癌的总生存期(OS)和疾病特异性生存期(DSS)显著相关(P < 0.05),然而,它与无进展生存期(PFS)无显著相关(P > 0.05) (图4),结果说明高表达GSDME的肝癌患者有着较短的总生存期(OS)和疾病特异性生存期(DSS)。
3.4. 肝细胞癌中GSDME的表达与免疫细胞浸润的强相关性
使用TIMER2.0,我们发现GSDME的表达与免疫细胞浸润显着相关(图5)。免疫细胞的表达,包括B细胞、自然杀伤(NK)细胞、CD4+T细胞、肿瘤相关巨噬细胞(TAM)和中性粒细胞。然而,GSDME的表达与CD8+T细胞的浸润无明显相关性。综上所述,GSDME可能广泛参与肿瘤免疫细胞浸润,在HCC的发生发展中起着至关重要的作用。
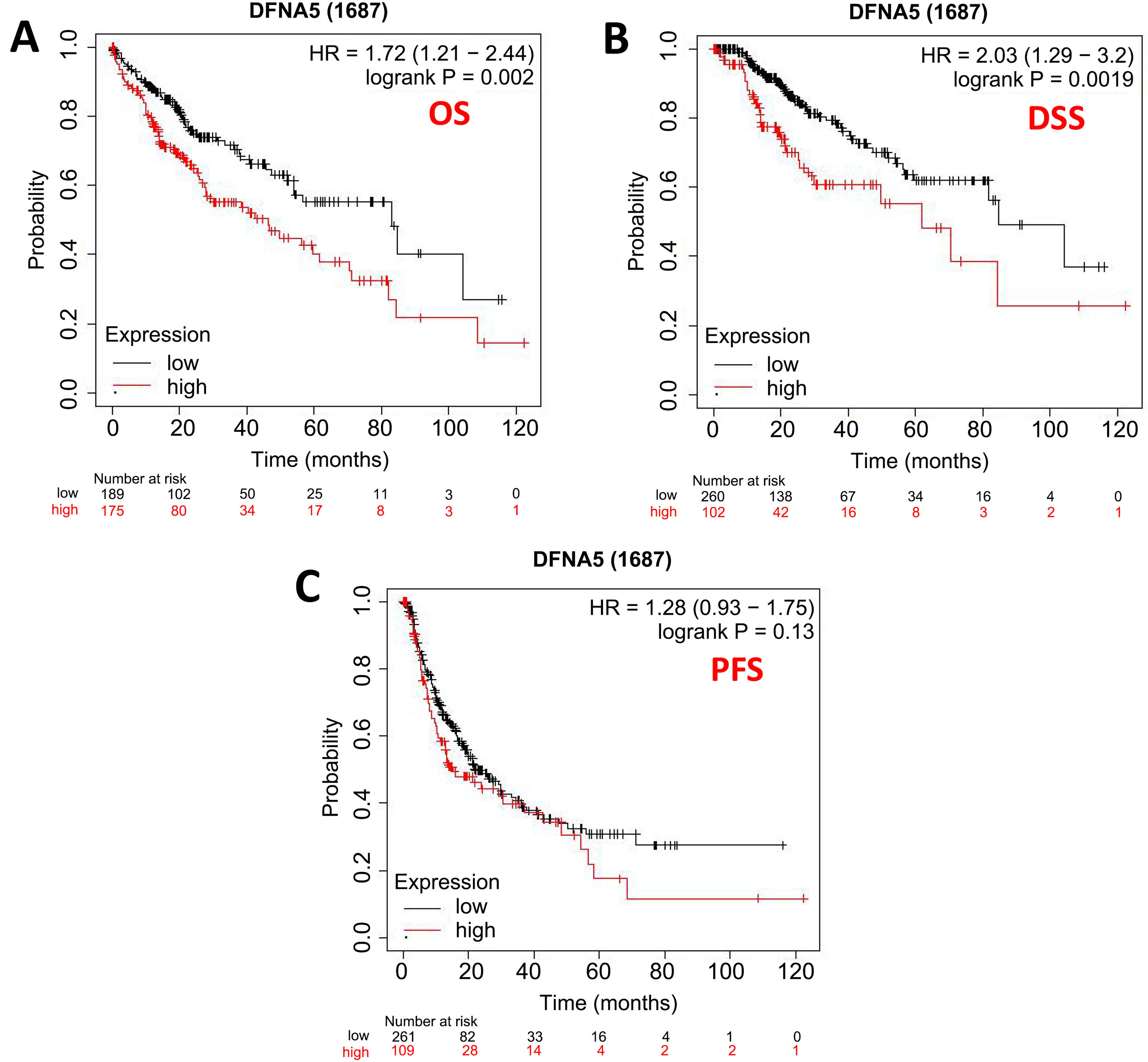
Figure 4. Survival curve analysis of GSDME gene expression and prognosis of liver cancer
图4. GSDME基因表达与肝癌预后意义的生存曲线分析图


Figure 5. Correlation analysis between GSDME gene expression and HCC infiltrating immune cell marker gene expression
图5. GSDME基因表达与HCC浸润性免疫细胞标志基因表达的相关性分析

Figure 6. Correlation analysis between GSDME gene expression and tumor immune checkpoints
图6. GSDME基因表达与肿瘤免疫检查点的相关性分析
3.5. GSDME表达与免疫检查点的相关性分析
为深入了解GSDME表达和免疫治疗相关检查点的相关性,使用TIMER2.0数据库研究发现GSDME的表达与PD-1 (PDCD1) (P < 0.001, r = 0.208)、PD-L1 (CD274) (P < 0.001, r = 0.192)、和CTLA4 (P < 0.001, r = 0.25)的表达是显著正性相关(spearman分析) (图6)。
3.6. 免疫组织化学(IHC)检测GSDME基因在肝癌中的蛋白表达
为进一步实验验证GSDME在肝癌患者组织的真实表达情况,运用HPA数据库,在我们的研究中,HPA011326抗体用于免疫组织化学染色,免疫组织化学检测的GSDME蛋白表达水平分为强、中、弱或阴性。我们发现GSDME在肝癌组织中呈强表达,在正常的肝组织中呈弱表达(图7),这进一步证实GSDME蛋白的表达在肝癌的发展中起到重要的作用。

Figure 7. Protein expression of GSDME in HCC clinical samples
图7. LIHC临床样本中GSDME的蛋白表达
4. 讨论
越来越多的证据表明,焦亡执行蛋白GSDME (DFNA5)参与了各种癌症类型的一系列生物学过程,包括个体发育、体内外环境平衡和病理生理过程 [16] 。根据最新的文献报道,GSDME的表达与人类疾病,特别是与恶性肿瘤有着密切的关系。然而,GSDME基因在肿瘤发病机制中的作用及其潜在的分子机制值得进一步研究,特别是目前关于GSDME在肝癌中的研究甚少 [17] 。因此,我们对GSDME的表达、预后、基因改变、免疫细胞浸润和可能的分子机制进行了全面分析。
先前的研究已经证明了GSDME在多种疾病中的作用,例如多种肿瘤化疗药物被证明是通过caspase3/GSDME信号通路影响肝癌的进展 [18] 。在我们的研究中,根据GEPIA数据库和TCGA数据库,与肝脏正常样本相比,LIHC具有更高水平的GSDME表达。LIHC中上调的GSDME表达与晚期临床病理参数(组织分级、肿瘤分级和淋巴结转移)相关,同时也与不良预后有关(OS),表明GSDME可以作为肝癌预后的生物标志物。
免疫疗法彻底改变了肿瘤治疗的管理,其机理主要是重新启动并维持肿瘤免疫循环以恢复正常的抗肿瘤免疫活性 [19] 。不幸的是,目前,免疫疗法仅使一部分患者受益,其中一个原因是癌细胞可能有效地逃避由固有免疫抑制微环境引起的宿主免疫系统。对于HCC,近年来分子靶向治疗和免疫治疗发挥了一定的治疗作用 [20] 。例如,免疫检查点抑制剂的开发已显示出临床疗效 [21] 。然而,由于其有一定的副作用,大多数HCC患者无法从免疫检查点抑制剂中获益。因此,有必要进一步寻找免疫相关基因,以改善HCC患者的预后。
据报道,肝癌中GSDME水平显着升高,并且与这些患者的不良预后有关,这可能是由于肿瘤微环境中异常的免疫细胞浸润 [22] 。在本研究中,相关性分析揭示了GSDME与PD-L1 (CD274)、CTLA4、PD-1 (PDCD1)和免疫细胞(如巨噬细胞、B细胞、NK细胞、中性粒细胞、CD4+T细胞等)。此外,与GSDME的低表达组相比,免疫细胞(巨噬细胞、B细胞、NK细胞、中性粒细胞、CD4+T细胞)的富集在高表达组中更高。我们的结果表明,在肝癌肿瘤的微环境中,GSDME与免疫浸润和免疫抑制密切相关。综上所述,我们提供了大量证据支持GSDME作为HCC早期预后生物标志物的临床应用。应更深入地研究有关用于LIHC治疗的GSDME相关通路的进一步分析。
然而,尽管在整合现有TCGA数据库的信息方面做出了很多努力,但目前的研究仍然存在一些局限性 [23] 。首先,虽然生物信息学分析为我们提供了GSDME在癌症中的一些重要见解,但有必要进行生物学研究体外或体内实验以检查我们的发现并加速临床应用。进一步的机理探索将有助于阐明GSDME在分子水平上的作用。其次,翻译后修饰在调节细胞内信号转导和调节因子的活性方面具有重要价值,但这些数据库中没有GSDME的翻译后修饰数据。第三,发现GSDME表达与癌症免疫和临床生存预后相关;然而,我们不确定GSDME通过明确的信号通路影响临床生存。
因此,我们才刚刚开始了解GSDME的分子机制及其在肝癌研究中的新兴作用,需要做大量的工作来进一步拓宽GSDME在人类癌症中的应用。
基金项目
广西医科大学青年科学基金项目(GXMUYSF202328);广西壮族自治区卫生健康委员会自筹经费科研课题(Z20210959)。
参考文献
NOTES
*共同第一作者。
#通讯作者。