1. 引言
在给水处理工艺中,常见的消毒剂主要是液氯、氯胺、次氯酸钠和二氧化氯等,次氯酸钠因其安全性高、消毒能力强、持续时间久、投加方式简单等备受各大供水企业的青睐 [1] 。近年来,省内供水企业正在陆续开展次氯酸钠工艺的改造升级。在使用次氯酸钠的过程中,逐步发现了次氯酸钠产品携带的溴酸盐过高会影响整体的供水品质 [2] 。此外,溴酸钾是一种致癌物质,过量食用会损害人的中枢神经、血液及肾脏。国际癌症研究机构已将该化合物列为2B级潜在致癌物 [3] 。因此,为了确保出水水质安全,方便快捷的溴酸盐含量的检测迫在眉睫。
为此,各地的政府推出了不少监管标准,例如DB32/T 3701-2019《江苏省城市自来水厂关键水质指标控制标准》 [4] 、DB4403/T 60-2020《深圳市饮用水水质标准》 [5] 、《苏州市自来水厂出厂水水质指标限值》 [6] 等。但是,以上指标的检测方法只适用于生活饮用水中溴酸盐的检测,并未直接对次氯酸盐中的溴酸盐进行检测。为了弥补这一空缺,抓好次氯酸钠产品质量的源头控制,提高检测和监管效率,本实验参照GB/T 5750.10-2006溴酸盐离子色谱法检测饮用水中溴酸盐的方法 [7] [8] ,摸索出了适用于次氯酸钠中溴酸盐离子色谱法的直接检测方法,并已成功运用到次氯酸钠日常质量管理中,可以更加有效地直接对次氯酸钠进行管控,减少净水产品所带来的危害,有助于进一步优化制水工艺。
2. 实验
2.1. 实验原理
溶液中的溴酸盐随氢氧根系统淋洗液进入阴离子交换分析系统(由保护柱和分析柱组成),根据分析柱对各物质的亲和力不同进行分离,已分离的物质流经阴离子抑制系统转化成具有高电导率的强酸,而淋洗液则转化成低电导率的弱酸或水,由电导检测器测量各种物质组分的电导率,以保留时间定性,峰面积或峰高定量 [9] 。
2.2. 实验仪器与试剂
2.2.1. 仪器
1) 实验仪器设备:Thermo Fisher Integrion高压离子色谱仪和Chromeleon色谱工作站。
2) ADRS-600 (4 mm)阴离子电解再生抑制器,AS-DV自动进样器。
3) 色谱分析柱:AS-19-4 μm耐高压阴离子分析柱。
4) 色谱保护柱:AG-19-4 μm耐高压阴离子保护柱。
5) 前处理柱:Ag柱、H柱。
6) Milli-Q超纯水系统。
7) 滤器及滤膜:0.22 μm滤膜。
2.2.2. 实验试剂
1) 纯水(去离子超纯水):含各种待测阴离子应低于仪器的最低检测限,实验用水为二次去离子水(电阻率18.5 MΩ·cm)。
2) 色谱标准物:溴酸盐标准溶液(ρ = 100 μg/mL),直接购买市售有证标准溶液,按标准溶液证书要求保存,使用时应恢复至室温,并摇匀。
2.3. 实验方法及色谱条件
AS-19-4 μm耐高压阴离子色谱分析柱,AG-19-4 μm耐高压阴离子色谱保护柱,ADRS-600 (4 mm)阴离子电解再生抑制器,淋洗液:淋洗液发生器产生的高纯KOH溶液,淋洗过程为等度淋洗,淋洗液浓度为8 mmol/L;流速设置为1.0 mL/min;进样量以500 μL定量环;柱温设置为30℃,电导池温度35℃,定量方式以峰面积定量。
2.4. 标准溶液的配制
溴酸盐标准使用溶液[ρ(BrO3−) = 1.0 mg/L],取1.0 mL溴酸盐标准溶液(2.2.2. 2))于50 mL容量瓶中,用纯水(2.2.2. 1))定容,混匀,4℃密封、避光保存。
2.5. 标准曲线的绘制
2.5.1. 配制标准溶液系列
吸取溴酸盐标准使用溶液(2.4)吸取溴酸盐标准使用溶液0 mL、0.2 mL、0.5 mL、1.0 mL、2.0 mL、3.0 mL、4.0 mL于100 mL容量瓶中,加纯水至刻度,混匀。此标准系列溶液中(溴酸盐)的浓度分别为0 µg/L、2.0 µg/L、5.0 µg/L、10.0 µg/L、20.0 µg/L、30.0 µg/L、40.0 µg/L标准系列溶液要求现用现配。
2.5.2. 标准溶液系列的测定
分别吸取相应体积的标准系列溶液注入离子色谱仪测定,记录溴酸盐的峰面积或峰高。以溴酸盐的峰面积或峰高对溴酸盐的浓度绘制标准曲线,并计算回归方程。校准曲线的相关系数应不小于0.999,否则需重新绘制校准曲线。
2.6. 样品的前处理
2.6.1. 样品的采集和保存
按GB 19106-2013的规定要求采集和保存样品,用500 mL带磨口塞的棕色瓶采集次氯酸钠样品(应混匀样品),立即带回实验室,制备试样溶液A,保存于500 mL带磨口塞的棕色瓶中。
2.6.2. 样品预处理
试液A的制备:使用移液管准确移取20 ml样品于50 ml烧杯中称量,精确至0.01 g定容至500 mL棕色容量瓶。
检测样品的制备:准确移取试液A 1.0 mL稀释至500 mL容量瓶。使用10 mL注射器,吸取检测样品经过Ag柱,再经过H柱,最后过0.2 µm滤膜,收集于5 mL样品管,上机检测分析。
3. 实验结果
3.1. 定量检出限的确定
本实验中采用的是定量检出限,计算方法参照GB/T 27417-2017中规定:按照信噪比法评估LOD (检出限),以2倍信噪比确定可靠检出最小浓度,LOQ (定量限)以10倍LOD来表示(表1)。

Table 1. Quantitative detection limit data
表1. 定量检出限数据
S/N为工作曲线最低点信噪比,C为工作曲线最低点的浓度。
计算公式为:LOD = 2 × C/(S/N),LOQ = 10 × LOD。考虑仪器稳定性,将溴酸盐定量限定为2.0 μg/L;样品检测限:一般检测样品不需要浓缩处理,因此样品检测限与定量检出限一致。
3.2. 检测范围
适用于次氯酸钠中溴酸盐的离子色谱法测定,检测色谱图详见图1。
在使用integrion高压离子色谱仪及AS-19-4 μm分析柱进行溴酸盐的检测,并且进样量为500 μL时,本方法的最低检测质量浓度为:溴酸盐2.0 μg/L;适宜的检测范围 [10] 为:溴酸盐2.0 μg/L~40.0 μg/L。
3.3. 溴酸盐的精密度
分别选取含溴酸盐的低、中、高标准溶液,测定6次,测得其浓度(单位:μg/L),见下表2。

Table 2. The precision data of bromate
表2. 溴酸盐精密度数据
精密度的计算公式为:
结果表明:低浓度的相对标准偏差为1.57%,中浓度相对标准偏差为0.64%,高浓度相对标准偏差为2.05%,结果表明:重复性良好,满足精密度的要求 [11] 。
如图2所示,溴酸盐的浓度于峰面积呈良好线性关系,浓度(X, g/L)为横坐标,峰面积(Y, μs)为纵坐标,线性回归方程为Y = −0.00085 + 0.00130 X,相关系数为0.9992。

Figure 2. The linear diagram of bromate
图2. 溴酸盐的线性图
3.4. 溴酸盐的准确度
采用溴酸盐有证标注物质进行检测,结果均在其证书的不确定度范围内,见下表3。

Table 3. The accuracy data of bromate
表3. 溴酸盐准确度数据
有证物质盲样结果为:9.7 ± 0.9 μg/L (k = 2),符合准确度要求。
3.5. 样品保存条件
通过原液在常温条件下保存测试(见表4)。实验结果表明:溴酸盐7天后检测浓度明显增加,不适合作为样品保存。试液A通过0℃~4℃及常温保存条件对比(见表5),实验结果表明:试液A在常温及0℃~4℃保存时,待测样品的溴酸盐无明显变化,可长期保存分析,较适合作为样品检测。

Table 4. The influence of the bromate concentration kept in stock solution
表4. 原液保存下溴酸盐浓度随时间变化的影响

Table 5. The influence of the bromate peak area over time kept in test solution A at 0˚C ~4˚C and normal temperature
表5. 0℃~4℃与常温下以试液A保存下溴酸盐峰面积随时间变化的影响
3.6. 样品的预处理
通过次氯酸钠试样过不同前处理小柱后进行测定,分析目标物溴酸盐的影响程度,通过检测对比发现见图3,次氯酸钠中溴酸盐分别单过H柱和串联Ag柱H柱后对溴酸盐的检测稳定性及干扰峰的影响变化,从对比图谱中可以分析得到,串联Ag柱H柱后溴酸盐的检测稳定性及干扰峰的影响变小,同时降低检测样品中氯化物含量过高对溴酸盐检测峰的影响。
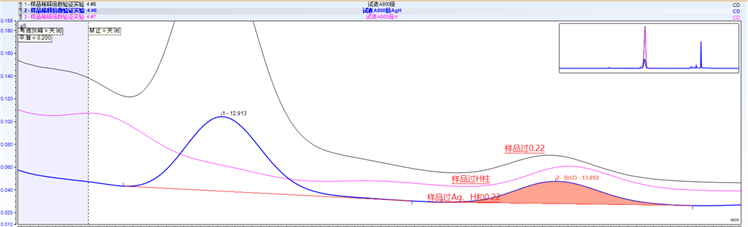
Figure 3. Comparison diagram of pretreatment analysis
图3. 预处理分析对比图
3.7. 样品测定的干扰
3.7.1. 有机物的影响
使用总有机碳(TOC)进行样品分析,通过TOC分析试液A稀释500倍后结果,证明稀释样品中无有机物(谱图如下:图4为TOC拟图)。
3.7.2. 溴乙酸的影响
溴乙酸对检测样品溴酸盐的影响。通过虚拟柱软件模拟分析被测物质组分发现溴乙酸与溴酸盐在所选分析柱上存在干扰影响,通过实验对比纯物质溴乙酸与标准物质溴酸盐及被测样品检测分析对比,我们发现在此方法条件下溴乙酸与被测组分分离度良好,不存在干扰(见图5、图6)。
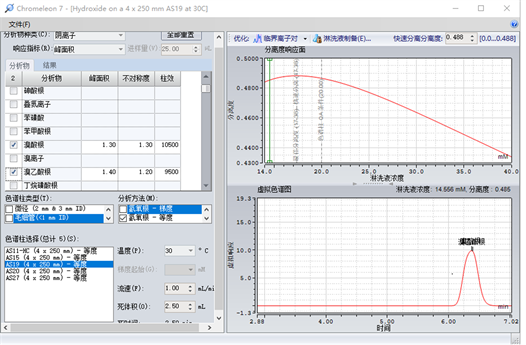
Figure 5. Analysis of substances to be tested by virtual column software simulates
图5. 虚拟柱软件模拟分析被测物质组分
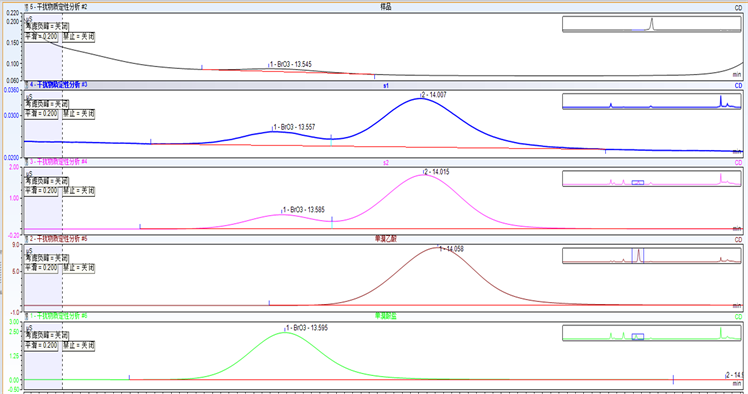
Figure 6. Detection analysis and comparison charts on the pure bromoacetic acid, standard substance bromate and tested sample
图6. 纯物质溴乙酸与标准物质溴酸盐及被测样品检测分析对比图
3.8. 样品稀释倍数的影响
通过对次氯酸钠样品的不同稀释倍数的测定,分析不同稀释倍数对目标物的干扰情况以及对仪器的影响,选取合适的稀释倍数。结果分析表明:① 1000倍及800倍溴酸盐含量过低,稀释倍数过高;② 500倍及400倍下溴酸盐含量位于线性中点比较合适,考虑分析样品特性选取稀释倍数500倍作为检测最后使用倍数,如样品含量过高可适当提高稀释倍数(见表6)。

Table 6. Data on the effect of sample dilution ratio on bromate
表6. 样品稀释倍数对溴酸盐的影响数据
3.9. 样品的回收率
下表中,次氯酸样品为试样稀释500倍后的溶液进行加标回收测定(单位:mg/L),见表7。

Table 7. The data of the recovery for the samples
表7. 样品回收率数据
此次对次氯酸钠中溴酸盐加标回收的确认,溴酸盐的样品浓度回收率为106.0%,在相关线性范围内,满足样品回收的要求。
4. 结论
本文优化了次氯酸钠检测的前处理过程,将其制备成试液A后稀释500倍,接着将待测溶液依次通过Ag柱、H柱和0.2 µm滤膜后进高压离子色谱仪进行检测。对次氯酸钠的成分进行除杂和净化,有效地保护了离子色谱。实验过程中,采用AS-19-4 μm耐高压阴离子色谱柱,以8 mmol的淋洗液浓度进行等度淋洗,在流速1.0 mL/min、柱温30℃、500 uL定量环的色谱条件下,使用ADRS-600 (4 mm)阴离子电解再生抑制器进行检测。实验结果表明:在使用该前处理和检测方法下,次氯酸钠中溴酸盐可以达到很好的分离效果,不受其他杂质的影响,且检测数据稳定,检出限低至0.0020 mg/L,线性回归方程为Y = −0.00085 + 0.00130 X,相关系数为0.9992,多次测定相对标准偏差(RSD)在0.64%~2.05%,重现性良好。最后对样品进行加标回收检测,平均回收率为106%。由此得出,本实验对次氯酸钠的溴酸盐检测方法简便高效、灵敏度高、线性条件良好,可以用于日常水质检测的使用中,有利于次氯酸钠工艺的改造升级,也为次氯酸钠的源头监控提供了新的思路。
参考文献