1. 引言
迷迭香(Rosmarinus officinalis),是双子叶花卉纲、唇形科迷迭香属花卉,迷迭香全株均具有较为广泛的药用以及食品、化妆品用途,原产于中欧和非洲以北的地中海沿岸,后引入我国并有大规模的种植。迷迭香中含有丰富的药用资源 [1],蕴含的酚类是其主要的成分,属于酚酸类的鼠尾草酚、鼠尾草酸、绿原酸、咖啡酸类都是工业生产与应用广泛的天然抗氧化剂 [2]。水溶性成分迷迭香精油具有清除自由基、蛋白质和酯类的抗氧化作用 [3],迷迭香精油中的樟脑成分、α-蒎烯类具有抗菌的功效 [4]。迷迭香中的五环三萜类成分齐墩果酸及熊果酸的含量在近年来的研究提取、分离中被广泛关注,两者拥有多种生物活性,可以护血管、降血脂、降压、护肝、护肾、抗焦虑、调控免疫 [5]。特别是近年来,有关于熊果酸、齐墩果酸的抗肿瘤活性和延缓衰老的研究成为热点,两者目前主要来源为天然药物提取。但由于齐墩果酸与熊果酸均为五环三萜型的同分异构体,仅29、30位之间的甲基位置差异,很难将二者完全分离,检测二者的色谱条件不理想、分离度较差 [6] [7] [8] [9]。此外,新版药典 [10] 中的色谱条件分离效果也不太理想。有研究报道 [11] 利用HPLC法测定一些中草药中两种三萜酸的含量,代琪 [12] 等、孟文静 [13] 等分别对木瓜和枇杷叶中的齐墩果酸、熊果酸进行了HPLC的含量分析,但有关迷迭香药材中齐墩果酸、熊果酸的分析方法以及应用情况却尚未见详尽研究。本实验开发了一种新的色谱方法,分离并测定了迷迭香中两者的含量,获取了从天然植物中提取更高含量的齐墩果酸和熊果酸的新途径,并为迷迭香药物开发质量分析和控制、迷迭香药材中提取分离齐墩果酸和熊果酸工艺研究提供可靠的检测方法和科学依据。
2. 实验部分
2.1. 仪器与试剂
UV1900双光束紫外可见分光光度计(上海佑科),日立高效液相色谱仪(Primaide Primaide 1410 UV检测器,1210自动进样器,1310柱温箱),安捷伦色谱分析柱(ZORBAX SB-C18, 250 mm × 4.6 mm, 5 μm),SHIMADZU AUY120电子天平(岛津公司),SB-3200 DT型超声波清洗机(频率40 KHz,超声功率180 W,加热功率400 W,新芝公司)。
齐墩果酸对照品(B20954,含量HPLC ≥ 98%,上海源叶生物科技公司),熊果酸对照品(B21403,含量HPLC ≥ 98%,上海源叶生物科技公司),迷迭香药材(购于安徽毫州药材市场);乙腈试剂与甲醇试剂(色谱级,赛默飞公司),实验室自制超纯水。
2.2. 对照品溶液的配制
分别精密称取25.00 mg的两种标准对照品,少量甲醇配成溶液后倒入25 mL容量瓶中,加甲醇至刻度线,摇匀,制成各为1.00 mg/mL的对照品溶液。
2.3. 供试液的制备
精密称定迷迭香粉末0.50 g,精密加甲醇10.00 mL,混合均匀后称量,50℃下超声1 h后,冷却到室温,甲醇溶剂补足重量,抽滤,取滤液备用,滤渣中重新加入10.00 mL甲醇溶液,重复上述条件超声处理,合并两次滤液,过0.45 μm的微孔滤膜,即得。
2.4. 检测波长的选择
双光束紫外可见分光光度计测定熊果酸、齐墩果酸标准品溶液和迷迭香提取液紫外吸收曲线(图1),显示最大吸收波长都在206 nm处,设定206 nm为工作波长。
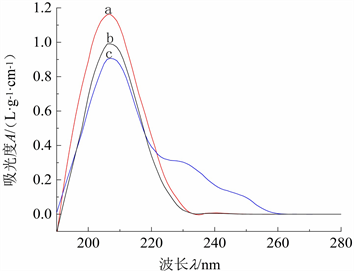
Figure 1. Ultraviolet wavelength scanning Diagram. (a) Oleanolic acid; (b) Ursolic acid; (c) Rosmarinus officinalis extract
图1. 紫外波长扫描图。(a) 齐墩果酸;(b) 熊果酸;(c) 迷迭香提取液
2.5. 色谱条件的确定
《中国药典》中还未收录迷迭香药材。依据《中华人民共和国药典》2020版第一部木瓜中齐墩果酸、熊果酸含量测定项的方法 [14],选择用甲醇–冰醋酸–水–三乙胺、甲醇–乙腈-0.5%醋酸铵溶液、乙腈-0.2%醋酸水溶液、乙腈-0.2%乙酸铵水溶液、乙腈-0.1%氨水等体系,对熊果酸、齐墩果酸组分色谱过程的流动相进行了检测筛选。
3. 结果与讨论
3.1. 流动相的确定
试验结果表明,甲醇–冰醋酸–水–三乙胺(65:0.1:34.85:0.05)为流动相(图2),测定波长206 nm,柱温16℃~18℃,在此色谱条件下的齐墩果酸和熊果酸分离度小于1.5。甲醇–乙腈-0.5%醋酸铵溶液(12:67:21)为流动相(图3),检测波长为 206 nm,此色谱条件下的齐墩果酸和熊果酸分离度不好;乙腈-0.2%醋酸水溶液(88:12) (图4)、乙腈-0.2%乙酸铵水溶液(83:17) (图5),分离度均低于1.5,齐墩果酸和熊果酸分离不佳。

Figure 2. Methanol-glacial acetic acid-water-triethylamine (65:0.1:34.85:0.05)
图2. 甲醇–冰醋酸–水–三乙胺(65:0.1:34.85:0.05)

Figure 3. Methanol-acetonitrile-0.5% ammonium acetate solution (12:67:21)
图3. 甲醇–乙腈-0.5%醋酸铵溶液(12:67:21)
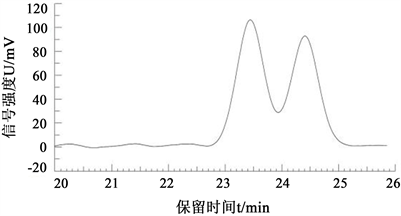
Figure 4. Acetonitrile-0.2% acetic acid aqueous solution (83:17)
图4. 乙腈-0.2%醋酸水溶液(83:17)
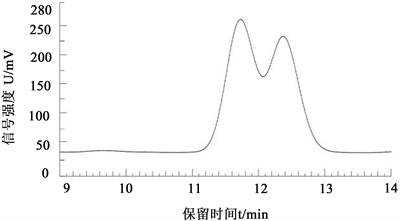
Figure 5. Acetonitrile-0.2% ammonium acetate aqueous solution (83:17)
图5. 乙腈-0.2%乙酸铵水溶液(83:17)
乙腈–氨水–磷酸体系,经多次实验,结果基线平稳,再现性好,可用于检测植物中熊果酸、齐墩果酸,并发现pH对分离起着至关重要的作用。对比于pH = 6.8、7.0、7.4、7.8的色谱过程,pH ≤ 7.0时,齐墩果酸和熊果酸并不能得到有效分离;pH处于碱性时,两物质成离子化状态,有利分离,在pH = 7.4和7.8时,分离效果相同,但色谱分析柱的pH耐受范围一般为2~8之间,设定pH为7.4。考察不同质量分数的氨水(0.05%, 0.1%, 0.15%, 0.2%)时,0.05%氨水分离度达不到规定要求,0.1%~0.2%的浓度分离度和理论塔板数基本相同,选择质量分数为0.1%的氨水溶液。调节流动相比例,最后确定的色谱条件为乙腈-0.10%氨水(65:35) (磷酸调pH = 7.4),流量为1.2 mL/min,基线平直稳定,齐墩果酸的出峰时间约为13.767 min;熊果酸的出峰时间约为15.033 min (图6),且峰形较好,理论塔板数大于5000,分离度为1.81,达到完全分离。对迷迭香样品提取液进行检测,液相色谱图如图7所示。
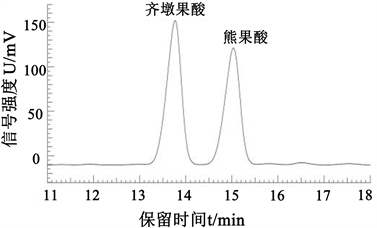
Figure 6. Chromatogram of mixed solution of oleanolic acid and ursolic acid reference substance
图6. 齐墩果酸、熊果酸对照品混合液色谱图
3.2. 标准曲线及线性关系
精密吸取齐墩果酸、熊果酸两种标准品溶液混匀,置于5 mL容量瓶中,甲醇溶液定容,分别吸取混合液并制成不同浓度梯度的标准品溶液。取10 μL进样检测,经线性回归处理,所得齐墩果酸和熊果酸的回归方程式依次为Y = 6283.2X + 284028 (R2 = 0.9992);Y = 5455.8X + 154524 (R2 = 0.9994),实验结果表明,齐墩果酸浓度在97.00~970.00 μg/mL (如图8所示)、熊果酸浓度在52.75~1055.00 μg/mL范畴内有着较好的线性关系(如图9所示)。
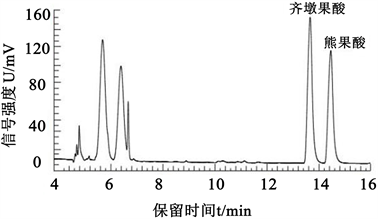
Figure 7. Chromatogram of Rosmarinus officinalis extract
图7. 迷迭香提取液色谱图
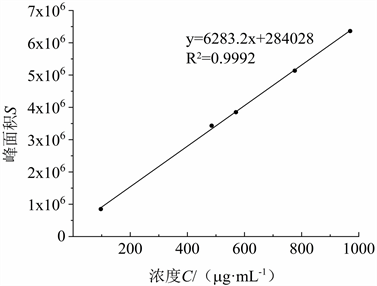
Figure 8. Standard curve of oleanolic acid
图8. 齐墩果酸标准曲线图
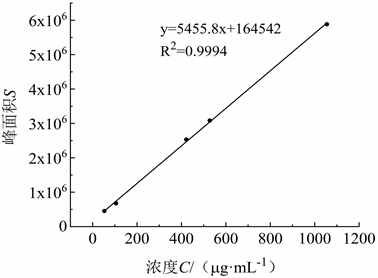
Figure 9. Standard curve of ursolic acid
图9. 熊果酸标准曲线图
3.3. 迷迭香中熊果酸和齐墩果酸含量测定
精密称定迷迭香粉末0.50 g,精密加入15.00 mL甲醇溶剂,混匀称量,50℃下超声一小时后,放冷,补足比量,过滤后,得续滤液备用,再取上层滤渣重新加入5.00 mL甲醇溶液并重新于相同条件下超声处理,再重复第一次操作后,经证明滤渣中已无齐墩果酸和熊果酸,合并上述两次滤液,过0.45 μm的微孔滤膜,进样检测,色谱图如图9所示,迷迭香粉末中含有齐墩果酸1.54%,含有熊果酸2.97%,含量与文献 [15] 报道基本吻合。
3.4. 精密度实验
吸取以上两个对照品混合溶液0.10 mL,置于1 mL容量瓶中,补液得混合标准液。精密吸取混标10 μL后,于上述色谱条件要求下重复进样5次,记录峰面积。齐墩果酸和熊果酸的RSD分别为0.472%和0.717%,RSD均 < 3.00%,精密度良好。
3.5. 稳定性试验
取供试品,间隔0 h、2 h、4 h、8 h、12 h、24 h进样,进样量均为10 μL,记录峰面积。齐墩果酸RSD = 0.24%,熊果酸RSD = 0.61%,试验证明供试品溶液在24小时内稳定。
3.6. 重复性试验
称取迷迭香粉0.50 g,制备供试品,设定色谱条件,记录峰面积,齐墩果酸RSD = 1.60%,熊果酸RSD = 2.60%,试验结果表明方法的重现性良好。
3.7. 回收率试验
称取已知含量的迷迭香粉,共九份,然后精密加入齐墩果酸和熊果酸对照品溶液,按照2.3.2项的制备工艺制备供试品溶液,精密吸取10 μL,注入高效液相色谱仪,设定色谱条件,记录峰面积,并计算加样回收率。齐墩果酸RSD = 1.96%,熊果酸RSD = 1.93%,实验结果表明回收率良好,见表1、表2。

Table 1. Recovery rate test of oleanolic acid
表1. 齐墩果酸加样回收率试验


Table 2. Ursolic acid sample adding recovery test
表2. 熊果酸加样回收率试验
4. 讨论
1) 二者同分异构体的结构,使得分离及检测时选择合适的色谱条件难度极大,文献报道 [16] 中的高效液相色谱条件分离度小于1.5,而本研究所确定的高效液相色谱条件分离度大于1.5,且通过对方法性能及可靠性的考察,适用于不同种药材中齐墩果酸、熊果酸的含量分析。
2) 通过本方法的液相色谱条件,分离并测定了迷迭香药材中齐墩果酸、熊果酸的含量,实验结果表明,迷迭香中含有齐墩果酸约1.54%,熊果酸约2.97%,相较于市场上主要从枇杷叶中提取所得的两种物质,迷迭香中有更多的含量。
3) 化学性质很相似的齐墩果酸和熊果酸经过离子化途径,改变二者在流动相中原本相似的性质,实现了两种同分异构体的柱分离途径。
4) 本实验还比较了甲醇、乙醇、异丙醇等提取溶剂中齐墩果酸及熊果酸的溶出效果,得出了最佳溶出条件,即取40目磨碎的迷迭香粉0.50 g于甲醇溶剂中,料液比为1:30,在50摄氏度下超声提取1个小时,此优化条件下可以确认齐墩果酸、熊果酸的在迷迭香的含量,为后续大规模提取及含量分析提供实验数据基础条件。
齐墩果酸与熊果酸是三萜酸同分异构体,提纯分离难度很大,而两者又几乎同时出现在一种植物中,一般的分离手段无法将两者分开,增加了植物资源的利用难度。目前齐墩果酸、熊果酸的含量分析方法包括紫外分光光度法、薄层扫描法、液质联用法以及本文中所应用的HPLC法,紫外分光光度法存在分辨度低等问题,薄层色谱法存在定量不准确等问题,液质联用成本则较高,实验条件要求严苛。HPLC法定量分析化学物质已经有较为成熟的研究基础,HPLC的优势在于分离以及定量,随着科技的发展,HPLC已经可以与许多复杂的定性定量设备联用,且实验过程简便、快速,弥补了HPLC无法准确定性的缺点。本实验利用HPLC法检测,操作简单、方法稳定可靠,可快速检测迷迭香中两种化学成分的含量,经实验证明该方法同样适用于其它富含齐墩果酸、熊果酸的植物中的分离检测,且结果准确。
参考文献
NOTES
*通讯作者。