1. 引言
癌症作为人类健康的重大威胁之一,对人们的身心健康产生了重大影响。为了克服癌症带来的危害,人们采用各种方法对其进行研究探索 [1] [2] [3]。前药策略,因其能够显著提高化疗药物的药代能力、药学和药效特性,在癌症治疗中获得了更多的关注 [4] - [9]。尤其是将具有刺激响应性能的控制单元修饰到前药上,不仅能显著提高药物的载药效率,还能获得具有肿瘤微环境响应性能的前药系统,智能释放抗癌药物,实现癌细胞治疗效果 [10] [11] [12] [13] [14]。与正常的组织细胞不同,肿瘤组织具有独特的物理化学特性,比如肿瘤细胞内具有较高浓度的过氧化氢,这主要是由于细胞内氧化还原动态失衡,从而导致细胞出现氧化应激态,过度产生活性氧(ROS),其浓度远高于正常细胞(约100倍),高浓度的ROS会导致细胞的永久死亡 [7] [15]。值得注意的是,为了维持细胞内氧化还原的稳定,即使是癌细胞也会产生更多的谷胱甘肽(GSH,内源性三肽)作为抗氧化剂来清除活性氧以避免氧化失衡 [7] [15]。由于高浓度的ROS,癌细胞内的GSH浓度也相应的高出正常细胞7~10倍 [15]。此外,研究表明,GSH不仅参与癌细胞的分裂增殖,还对细胞的多种生物过程起到至关重要的作用,比如:外源性物质的解毒过程与细胞的周期进程 [7]。因此,利用癌细胞内高浓度的GSH设计具有GSH响应性能的调控单元在癌症治疗中具有潜在的应用价值。
喜树碱作为一种天然抗癌药物,其衍生物已被广泛应用于各种癌细胞治疗。10-羟基喜树碱(HCPT, 10-Hydroxycamptothecin)抗癌机制与喜树碱相似,被认为是喜树碱衍生物中抗癌效果最好之一,其主要通过抑制拓扑异构酶来缓解DNA的扭转 [7] [16]。由于HCPT具有很强的荧光发射能力,因此,我们认为基于HCPT构筑具有GSH响应机制的前药分子不仅能通过HCPT的GSH刺激响应性荧光指示肿瘤组织的位置,实时追踪药物释放过程,还能作为前药分子,显著提高载药效率,实现癌细胞的有效治疗。
为此,我们通过取代反应设计合成了具有GSH响应性能的HCPT前药分子(DNS-HCPT)。在前药分子DNS-HCPT中,2,4-二硝基苯磺酰基(DNS)通过取代反应与HCPT共价相连,且由于DNS的吸电子效应致使HCPT自身荧光发生猝灭,但是在高浓度的GSH作用下,DNS会发生分子内重排并从DNS-HCPT上脱离,将HCPT释放出来,此时的HCPT不仅能高效治疗肿瘤组织,还能通过自身的荧光实现肿瘤组织的定位与诊断。GSH刺激响应释放结果表明,DNS-HCPT前药分子不仅能有效释放前药HCPT用于治疗癌细胞,其GSH响应后的荧光变化还可用于追踪药物释放过程及肿瘤位置,在肿瘤治疗与诊断中具有潜在价值(图1)。

Figure 1. GSH responsive illustration of 10-hydroxycamptothecin prodrug (DNS-HCPT)
图1. 10-羟基喜树碱前药分子(DNS-HCPT)的GSH响应示意图
2. 实验部分
2.1. 试剂与仪器
10-羟基喜树碱(HCPT, 99%)、2,4-二硝基苯磺酰氯(DNS, 98%),安耐吉化学;三乙胺(TEA)、碳酸氢钠、无水硫酸钠、二氯甲烷(DCM)、石油醚(PE)、乙酸乙酯(EA),分析纯,南京化学试剂有限公司;薄层层析硅胶,300~400目,山东青岛海洋。
Bruker 400 MHz核磁共振仪,瑞士Bruker公司;Hitachi F-7000荧光光谱仪,日本日立公司;IKA RV 10旋转蒸发仪,德国IKA公司;WFH-203B暗箱台式三用紫外分析仪,上海精密仪器仪表有限公司。
2.2. 10-羟基喜树碱前药分子(DNS-HCPT)的合成
合成路线如图2所示:

Figure 2. Synthesis route of DNS-HCPT
图2. DNS-HCPT的合成路线
将10-羟基喜树碱(0.93 g, 2.55 mmol)溶解在100 mL的二氯甲烷中,加入0.8 g的三乙胺,冰浴降温20 min,接着将溶有2,4-二硝基苯磺酰氯(0.8 g, 3 mmol)的50 mL二氯甲烷恒压滴加至反应液中,滴加时间超过1.5 h,滴加结束,继续搅拌反应3 h。反应结束,反应液用饱和碳酸氢钠洗涤三次,收集有机相,用无水硫酸钠干燥过夜。过滤收集滤液,直接硅胶拌样,以石油醚/乙酸乙酯(v/v = 1:3)作为流动相,通过柱层析纯化得黄色固体产物DNS-HCPT (0.91 g, 1.53 mmol, 60%)。
2.3. 10-羟基喜树碱前药分子(DNS-HCPT)的核磁测试
在纯化得到目标产物DNS-HCPT后,以DMSO-d6作为溶剂,通过Bruker 400 MHz核磁共振仪对DNS-HCPT的氢谱、碳谱进行检测分析(图3和图4),数据和图如下:1H NMR (400 MHz, DMSO-d6, 298 K) δ (ppm): 9.16 (d, J = 2.4 Hz, 1H), 8.72 (s, 1H), 8.58 (dd, J = 8.4, 2.0 Hz, 1H), 8.31 (d, J = 8.8 Hz, 1H), 8.25 (d, J = 8.8 Hz, 1H), 8.04 (d, J = 2.8 Hz, 1H), 7.66 (dd, J = 9.2, 2.4 Hz, 1H), 7.35 (s, 1H), 5.43 (s, 2H), 5.30 (s, 2H), 1.86~1.81 (m, 2H), 0.87 (t, J = 7.2 Hz, 3H).13C NMR (100 MHz, DMSO-d6, 298 K) δ (ppm): 172.9, 157.2, 154.3, 152.1, 150.4, 148.7, 147.1, 147.0, 145.5, 134.2, 132.3, 132.3, 131.5, 131.0, 128.7, 128.0, 125.3, 121.7, 121.1, 120.1, 97.6, 72.8, 65.7, 50.7, 30.7, 8.2.

Figure 3. 1H NMR spectrum (400 MHz, DMSO-d6, 298 K) of DNS-HCPT
图3. DNS-HCPT的氢谱(400 MHz, DMSO-d6, 298 K)

Figure 4. 13C NMR spectrum (100 MHz, DMSO-d6, 298 K) of DNS-HCPT
图4. DNS-HCPT的碳谱(100 MHz, DMSO-d6, 298 K)
3. 结果与讨论
3.1. DNS-HCPT的GSH刺激响应性研究
根据相关文献报道 [17] [18],前药分子DNS-HCPT中的2,4-二硝基苯磺酰基(DNS)部分对GSH具有显著的刺激响应性,可以使DNS-HCPT中的DNS重排离去,接下来首先对DNS-HCPT的GSH刺激响应性进行研究。
首先,配制0.2 mM的DNS-HCPT水溶液(含少量DMSO助溶),通过荧光光谱检测发现几乎没有荧光信号,此时在365 nm激发下也观察不到任何荧光,说明此时前药分子DNS-HCPT非常稳定,HCPT不能被释放出来(图5和图6)。然而,当向DNS-HCPT溶液中加入0.2 mM的GSH溶液后,1 min后可以检测到荧光强度为828 (545 nm处),说明HCPT被释放出来了,并且随着时间的增加,荧光强度越来越强,8 min后甚至可以达到2288 (545 nm处),说明前药分子DNS-HCPT具有明显的GSH刺激响应性(图5)。
更为重要的是,通过8 min的GSH刺激响应释放,我们可以观察到显著的黄色荧光,说明大部分前药HCPT被释放出来了,相较于GSH刺激响应释放前,荧光强度足足提高了48倍(图6)。上述荧光实验表明前药分子DNS-HCPT不仅具有显著的GSH刺激响应性能,其释放的前药分子HCPT还能够被用于追踪识别肿瘤组织的高浓度GSH环境,同时对癌细胞进行治疗,在肿瘤的诊治结合中具有潜在的价值。
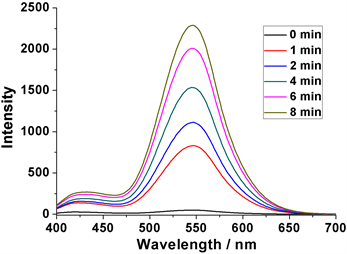
Figure 5. Fluorescence spectra of DNS-HCPT (0.2 mM) with GSH (0.2 mM) in different time
图5. DNS-HCPT (0.2 mM)在GSH (0.2 mM)作用下不同时间段的荧光图谱

Figure 6. Fluorescence spectra of DNS-HCPT (0.2 mM) with 0.0 and 0.2 mM GSH
图6. DNS-HCPT (0.2 mM)在0.0和0.2 mM GSH作用下的荧光谱图
3.2. DNS-HCPT的释放研究
在确定前药分子DNS-HCPT的GSH刺激响应性能后,接着对DNS-HCPT (0.2 mM)的GSH刺激响应释放进行了深入研究。如图7所示,在没有GSH的情况下,前药分子DNS-HCPT能够一直保持稳定,几乎没有任何的HCPT荧光信号能够被检测到。然而,当加入0.1 mM的GSH后,可以发现HCPT的荧光信号显著增强,随着时间的增加逐渐达到平衡,说明DNS-HCPT在GSH的作用下成功地释放出了前药分子HCPT。值得注意的是,随着GSH浓度从0.1 mM增加到0.2 mM和0.5 mM,HCPT的释放量也显著地从48%增加到了80%和90%,说明该前药分子具有很好的GSH刺激响应性能。这些释放结果说明,DNS-HCPT不仅具有显著的GSH刺激响应性能,在高浓度GSH下还能高效地释放前药分子HCPT,在癌细胞的诊治中具有重要价值。
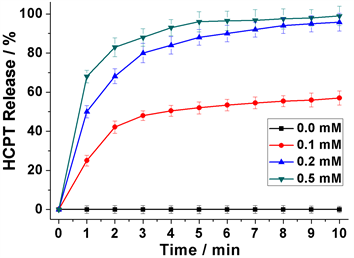
Figure 7. Time-dependent HCPT release at different GSH concentrations
图7. DNS-HCPT (0.2 mM)在不同GSH浓度下的释放曲线
3.3. DNS-HCPT的释放机理研究
谷胱甘肽(GSH)是一种谷氨酸、半胱氨酸和甘氨酸形成的含有巯基的三肽(R-SH)。文献表明 [5] [7] [8],当加入GSH后,R-SH中的巯基会进攻DNS,发生取代反应,同时DNS中的磺酰基会进行重排,最终以SO2的形式离去,而GSH通过巯基最终被修饰到磺酰基的位置,从而把前药HCPT给释放出来,实现GSH的刺激响应释放(图8)。

Figure 8. GSH release mechanism of DNS-HCPT
图8. DNS-HCPT的GSH释放机理
4. 结论
我们以10-羟基喜树碱(HCPT, 10-Hydroxycamptothecin)作为前药分子,通过取代反应在HCPT的10-羟基位置成功修饰了2,4-二硝基苯磺酰基(DNS),得到了具有诊治结合功能的喜树碱前药分子(DNS-HCPT)。由于DNS的分子内抑制作用,前药分子DNS-HCPT不发射荧光,但是在谷胱甘肽(GSH)的作用下,DNS-HCPT不仅能将前药分子HCPT快速地释放出来,其释放的HCPT还能发射出很强的黄色荧光,这样显著的荧光变化可被用于肿瘤组织的追踪与识别。更为重要的是,HCPT作为喜树碱衍生物中抗癌效果最好之一,DNS-HCPT释放的HCPT还能被用于癌细胞的治疗。因此,该前药分子DNS-HCPT在癌细胞的诊断与治疗中具有潜在的应用价值。
基金项目
本项目由国家自然科学基金(No. 22075152)支持。
NOTES
*通讯作者。