摘要: 采用水热法和共沉淀法分别制备了MnCeO
x@MgO核壳催化剂和MnCeMgO
x复合金属氧化物催化剂,通过催化活性评价和催化表征考察了MnCeO
x@MgO催化剂和MnCeMgO
x复合金属催化剂上同步脱除氮氧化物(NO
x)和氯苯(CB)的构效关系。活性测试结果表明,MnCeO
x@MgO核壳催化剂的催化活性强于MnCeMgO
x复合金属氧化物催化剂,且MnCeO
x@MgO核壳催化剂具有更宽的活性温度窗口。其中NO
x和CB在MnCeO
x@MgO核壳催化剂上的转化率分别在250℃和350℃达到77%和84%,NO
x和CB在MnCeMgO
x复合金属催化剂的转化效率分别为62.6% (200℃)和89% (350℃)。MnCeO
x@MgO催化剂的活性与其物化结构、表面活性氧物种比值和过渡金属活性组分的形态有关。MnCeO
x@MgO核壳催化剂的平均孔径和Olatt/Oads比值均大于MnCeMgO
x复合金属催化剂,与催化活性成正相关。催化剂中活性组分分别为Mn
2+、Mn
3+、Mn
4+、Ce
3+。
Abstract:
MnCeOx@MgO core-shell catalyst and MnCeMgOx composite catalyst were prepared by hydrothermal method and coprecipitation method, respectively. Structure-activity relationship in simultaneous removal of NOx and chlorobenzene (CB) on MnCeOx@MgO and MnCeMgOx catalysts was investigated by catalytic activity test and characterization. The results show that the activity of MnCe-Ox@MgO catalyst is higher than that of MnCeMgOx catalyst. For MnCeOx@MgO core-shell catalyst, the conversion of NOx and CB was 77% and 84% at 250˚C and 350˚C, respectively. For MnCeMgOx composite catalyst, the conversion of NOx and CB was 62.6% and 89% at 200˚C and 350˚C, respectively. The activity of MnCeOx@MgO catalyst is related to its physicochemical structure, surface active oxygen species ratio and the morphology of transition metal active components. Both average pore size and Olatt/Oads ratio of MnCeOx@MgO catalysts are higher than those of MnCeMgOx catalysts, which were positively correlated with the catalytic activity. The active components in MnCeOx@MgO catalyst are Mn2+, Mn3+, Mn4+, Ce3+ respectively.
1. 引言
垃圾焚烧过程中产生的NOx与CVOCs (如氯苯、多氯联苯类等)是PM2.5与臭氧的关键前驱体。催化氧化技术在氧气存在下加热后可完全分解气态污染物,具有容量大、实时性好等优点,是一种有效的VOCs去除方法。目前,氨选择性催化还原(NH3-SCR)技术在脱硝领域内应用十分广泛,是一种十分有效的去除氮氧化物的方法。在多污染协同控制过程中,NOx还原与CVOCs氧化的活性温度窗口是否一致以及催化剂是否具有同步脱除NOx和CVOCs的能力也十分重要 [1]。SCR技术中使用的主要催化剂是贵金属、分子筛和过渡金属催化剂。贵金属(如铂)催化剂对SCR和VOC氧化具有良好的催化活性 [2]。然而,这些催化剂的应用范围受到其高成本和暴露于卤代烃后失活的限制 [3] [4] [5]。沸石催化剂因其丰富的表面酸性被广泛应用于去除NOx,同时金属离子交换沸石催化剂已经被应用于同时去除CVOCs与NOx,其中根据研究表明Cu/ZSM5催化剂在同步去除二氯苯和NOx中表现出高活性,但是会促进了某些多氯化合物的形成 [6] [7]。过渡金属催化剂因其低廉的成本、丰富的地球资源和多种多样的物理化学性质而得到广泛的应用。一些金属氧化物如Co、Mn和Ce氧化物作为SCR反应的氧化还原中心,这是由于金属离子的价态变化导致了电子和氧的良好迁移 [6]。Mn/Ce催化剂由于其高的氧存储/释放能力和可变的氧化还原状态,已经被广泛应用于NOx与VOCs的协同去除。根据现有研究,Mn/Ce催化剂在同步去除NOx和VOCs中具有较好催化活性和较宽的活性温度窗口 [8] [9]。然而,这种良好的氧化还原能力导致SCR过程的N2选择性较低,另一个显著的缺点是Mn/Ce催化剂对氯化化合物的抵抗力较低 [10]。
因此,为了提高NOx和氯苯的脱除效率,我们研制出一种核壳催化剂MnCeOx@MgO,并比较分析了MnCeOx@MgO催化剂和MnCeMgOx复合金属氧化物催化剂的催化性能及物化性质。通过催化活性评价和催化表征对其构效关系进行研究。
2. 实验部分
2.1. 催化剂制备
2.1.1. MnCeOx@MgO核壳催化剂制备
将15 g乙酸锰(南京化学试剂股份有限公司,99%)、6.53 g乙酸铈(南京化学试剂股份有限公司,99%)和90 ml乙二醇(南京化学试剂股份有限公司,99.9%)的混合溶液加入到装有100 ml氨水(南京化学试剂股份有限公司,25%)、90 ml乙醇(沧州卓亚化工有限公司,95%)和30 ml去离子水的圆底烧瓶中,在120℃下连续搅拌2 h,离心洗涤后在60℃下干燥12 h,得到锰铈复合氧化物。将得到的锰铈复合氧化物和11.1 g氯化镁(寿光市邦泽化工有限公司,≥99%)加入50 ml乙二醇中,超声波处理30 min后,取悬浮液,继续超声波处理15 min,装入内衬特氟龙高压釜,加热至130℃保持24 h,将溶液洗涤并干燥,将产物置于马弗炉内,450℃高温煅烧4 h,得到MnCeOx@MgO。
2.1.2. MnCeMgOx复合金属氧化物催化剂制备
将15 mmol Ce(NO3)3∙6H2O (上海麦克林生化科技,99.5%)添加到300 ml去离子水中,并放入500 ml三颈烧瓶中。剧烈搅拌10 min后,将125 ml NaOH (南通润源环保科技有限公司,99.9%)水溶液(0.4 M)快速加入上述溶液中,随后在N2 (杭州航翔气体有限公司,99.99%)下剧烈搅拌10 min。之后,将含有MgCl2 (3.75 mmol)和Mn(NO3)3 (寿光市邦泽化工有限公司,≥99%)的125 ml混合溶液(15 mmol)快速注入到形成的均匀溶液中。在N2保护下,将上述浆料在室温(25℃)下保持60 min。通过离心分离最终产物,并用水/乙醇洗涤几次。最后,将获得的粉末在真空烘箱中于40℃干燥过夜,并在马弗炉中于450℃煅烧4 h。
2.2. 催化活性评价
协同脱除NOx和氯苯活性和稳定性测试装置为连续流的常压固定床反应装置。本实验中使用液相吹脱法向反应体系中通入氯苯,通过调节吹脱N2流量和水浴温度来控制通入反应气中氯苯的量。各气源(载气氮气、吹脱氮气、氨气、一氧化氮和氧气)的进气量通过质量流量计来控制,待载气氮气、氨气和氧气进入混合反应罐混合均匀后裹挟氯苯吹脱气进入到预热罐中预热,在进入反应床层前经过四通阀与氨气混合,然后进入催化剂反应床,与催化剂表面充分接触并反应。进口气体中,NO浓度600 ppm,NH3为600 ppm,氯苯为100 ppm,O2浓度为5 vol.%及N2作为平衡气体,总气量为1.5 L/min,空速为40,000 h−1。管路均使用加热带进行保温。固定床反应器采用石英材质的玻璃管,内径为1 cm。通过K型热电偶实时测量反应床层实际温度。催化剂装填在石英管中,每次测试前装填2.2 ml的催化剂。图1为装置反应示意图。采用GC9790 II气相色谱仪(浙江福立分析仪器股份有限公司)对反应进出口气体中的氯苯、CO和CO2的浓度进行在线检测。进出口气体中的NOx、NO、NO2、浓度由红外烟气分析仪在线检测,红外烟气分析仪配备有红外检测模块和进气管道。
2.3. 催化表征
采用美国麦克公司ASAP2460型物理吸附仪对N2吸附解吸进行分析,在液氮温度(−196℃)下采用氮气吸附法来测定样品孔结构的数据,样品测定前在300℃下抽真空7 h。
使用德国ZEISS Sigma 300型号的扫描电子显微镜对催化剂形貌进行观测。将催化剂研磨成粉末后,超声10 min,乙醇分散制样,在扫描电镜下观察样品形貌。
XRD衍射用阶梯扫描的方式,将样品研磨至粉末状,取100 mg样品进行压片,将压片后的样品装填在Panalytical X’Pert’3 Powder粉末X射线衍射仪上采集Cu/Kα辐射源,2θ为10˚~80˚,扫描速度为2˚ min−1。
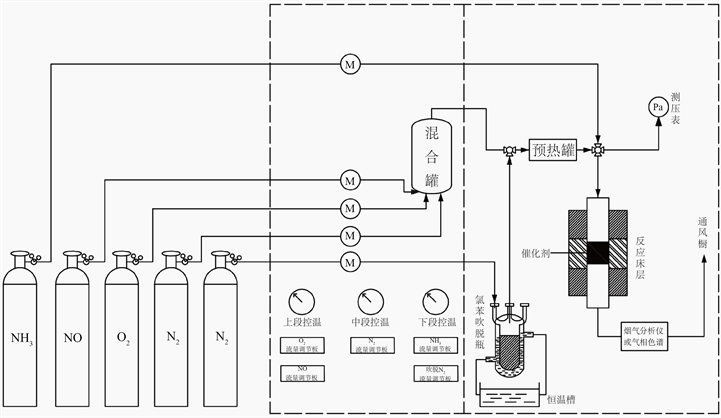
Figure 1. Schematic diagram of collaborative removal reaction unit
图1. 协同脱除反应装置示意图
采用XPS分析样品表面的各元素价态及其相对含量比例,仪器为美国PHI公司的Thermo Scientific,采用条件为铝/镁靶,高压12.0 kV,真空优于5 × 10−7 Pa。以C 1 s = 284.8 eV为基准进行结合能校正,采用XPSPeak4.1软件进行分峰拟合。
3. 结果与讨论
3.1. 催化活性
图2比较了MnCeOx@MgO催化剂和MnCeMgOx复合金属氧化物催化剂的活性。两种催化剂的NOx转化率随着温度的升高均呈“抛物线”状,而CB转化率与温度大致成正相关。MnCeOx@MgO催化剂在250℃时,最高NOx转化率为77%。在350℃时,最高CB转化率为84%。MnCeMgOx复合金属氧化物催化剂在200℃时,最大NOx转化率为63%。在350℃时,最大CB转化率为89%。根据催化测试结果,可以发现MnCeOx@MgO催化剂在250℃~300℃时,对同步去除NOx与CB都具有较高催化活性。相比之下,MnCeMgOx复合金属氧化物催化剂在同步去除NOx与CB时的活性温度窗口较窄,由此可见,MnCeOx@MgO催化剂具有更宽的活性温度窗口,对于NOx与CB具有更好的同步脱除效果。
3.2. 催化表征
表1比较了两种催化剂的比表面积、孔容和平均孔径。可以看出,与MnCeMgOx复合金属催化剂相比,以MgO碱金属作为壳,MnCeOx为核的MnCeOx@MgO核壳催化剂的比表面积有一定程度下降(从150.04 m2/g下降至48.94 m2/g),同时其孔容也有所下降(0.24 cm3/g下降至0.11 cm3/g),而两种催化剂的平均孔径大小为MnCeOX@MgO (9.35 nm) > MnCeMgOx复合金属氧化物催化剂(6.27 nm)。结合催化活性结果,得到催化剂的活性与催化剂的物化结构(比表面积、孔容和平均孔径)有一定的相关性,与比表面积和孔容成负相关性,与平均孔径成正相关性。催化活性较好的MnCeOx@MgO催化剂具有更大的平均孔径,这有利于增大与反应气体的接触,提高催化活性。图3与图4分别为MnCeOx@MgO和复合金属氧化物催化剂的孔径分布与等温吸附曲线。样品孔径大多在2~50 nm之间,为介孔材料。等温吸附曲线均为IV类,滞后环均为H4型。
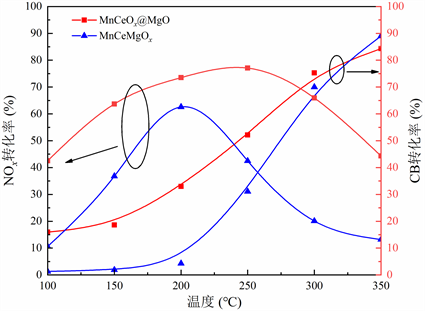
Figure 2. Catalytic activity of MnCeOx@MgO and MnCeMgO
图2. MnCeOx@MgO和MnCeMgO的催化活性

Table 1. Specific surface area, pore volume and average pore diameter of catalysts
表1. 催化剂的比表面积、孔容与平均孔径

Figure 3. Pore size distribution diagram and isothermal adsorption curve of MnCeOx@MgO catalyst
图3. MnCeOx@MgO催化剂孔径分布与等温吸附曲线
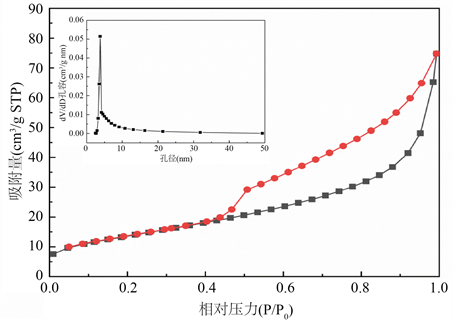
Figure 4. Pore size distribution diagram and isothermal adsorption curve of MnCeMgOx catalyst
图4. MnCeMgOx催化剂孔径分布与等温吸附曲线
图5通过SEM观察了MnCeOx@MgO和MnCeMgOx复合金属催化剂的微观形态。图5(a1),图5(a2)为MnCeOx@MgO催化剂,可以看出催化剂有一粒粒类似石粒的团状物覆盖在表面,密集的小石粒之间形成大小不一孔道结构,主要为介孔,与BET的结果一致,有利于暴露更多的活性位点,提高催化活性。图5(b1),图5(b2)为MnCeMgOx复合金属催化剂,从SEM谱图看出,催化剂表面布满了大量不均匀的絮状颗粒。




Figure 5. SEM spectrum of MnCeOx@MgO (a1~a2) and MnCeMgOx (b1~b2) catalysts
图5. MnCeOx@MgO (a1~a2)和MnCeMgOx (b1~b2)催化剂的SEM谱图
图6为MnCeOx@MgO与MnCeMgOx催化剂的XRD谱图。MnCeOx@MgO催化剂中Mn主要以Mn3O4晶型存在(PDF#75-1560),其主要的衍射峰2θ = 18.1˚的晶面为(101),2θ = 32.7˚的晶面为(103),2θ = 36.2˚的晶面为(211),2θ = 38.3˚的晶面为(004),2θ = 44.5˚的晶面为(220),2θ = 64.8˚的晶面为(400)。催化剂中Ce主要以CeO2晶型存在(PDF#81-0792),其主要的衍射峰2θ = 29˚的晶面为(111),2θ = 48.1˚的晶面为(220),2θ = 56.4˚的晶面为(311)。根据PDF卡片(PDF#65-2975), MnCeMgOx催化剂中Ce主要以CeO2晶型存在,其主要的衍射峰2θ = 28.6˚的晶面为(111),2θ = 33.4˚的晶面为(200),2θ = 47.6˚的晶面为(220),2θ = 56.5˚的晶面为(311)。根据PDF卡片(PDF#75-1560),催化剂中的Mn以Mn3O4晶型存在,其衍射峰为2θ =32.7˚为(103)晶面,相较于MnCeOx@MgO催化剂,MnCeMgOx复合金属氧化物催化剂中部分属于CeO2和Mn3O4的衍射峰消失。
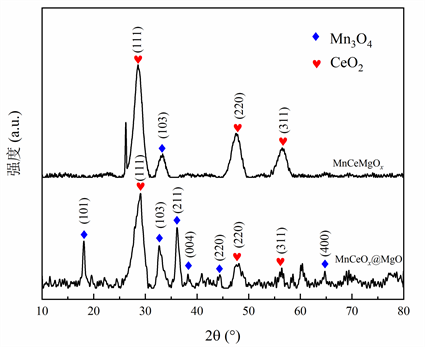
Figure 6. XRD spectrum of MnCeOx@MgO and MnCeMgOx catalysts
图6. MnCeOx@MgO与MnCeMgOx催化剂的XRD谱图
通过XPS对两种催化剂表面O、Mn、Ce元素的价态及相对含量进一步分析。图7为MnCeOx@MgO催化剂和MnCeMgOx复合金属氧化物催化剂的O 1 s谱图。催化剂表面氧物种包括晶格氧(Olatt)和表面吸附氧(Oads),结合能范围分别为 528.5~529.5 和532~533 eV [11] [12]。Olatt和Oads被认为是活性氧物种,会对于NH3-SCR和VOC氧化的活性起重要作用 [13]。两种催化剂的Olatt结合能相近在 529.5 eV左右,Oads结合能相近在531.6 eV左右。表2罗列了2种催化剂的O 1 s分析结果,与MnCeMgOx催化剂相比,MnCeOx@MgO催化剂的Oads/Olatt比例更高,由于Oads在NH3-SCR和VOC氧化起到更重要的作用 [14],因此MnCeOx@MgO催化剂在同步去除NOx与CB中表现出更好的催化活性。
从图8的Mn 2p的谱图可知,两种催化剂表面上Mn以Mn2+、Mn3+和Mn4+的形式存在 [14],对于MnCeOx@MgO和MnCeMgOx催化剂,Mn元素在催化剂上的价态比例分别为Mn4+:Mn3+:Mn2+ = 45.0:28.9:26.1与Mn4+:Mn3+:Mn2+ = 31.0:32.5:36.5 (见表2)。图9的Ce 2p谱图可见,两种催化剂表面上Ce以Ce4+、Ce3+形式存在 [15] (见表2)。结合能为903.4与885.1 eV的峰可归因于Ce3+,其余的六个峰则可以归于Ce4+。Ce3+/Ce4+在MnCeOx@MgO和MnCeMgOx催化剂上的比例分别5.6和4.9。为Mn4+和Ce3+离子的相对含量较高通常反映了其在低温下的优异催化性能,因为前者对氯代芳香族化合物和NO的催化转化具有良好的氧化还原性能 [15],而后者已被用作催化剂中氧空位的指示剂 [16],因此MnCeOx@MgO对于同步脱除NOx和氯苯表现出更好的催化活性。
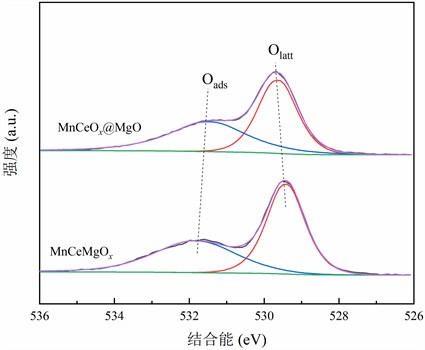
Figure 7. O 1 s spectrum of catalysts
图7. 催化剂的O 1 s谱图
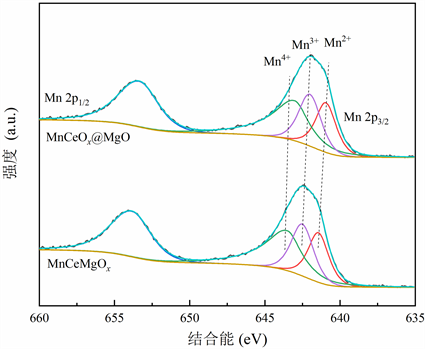
Figure 8. Mn 2p spectrum of catalysts
图8. 催化剂的Mn 2p谱图

Table 2. XPS results of MnCeOx@MgO and MnCeMgOx
表2. MnCeOx@MgO和MnCeMgOx的XPS结果

Figure 9. Ce 2p spectrum of catalysts
图9. 催化剂的Ce 2p谱图
4. 结论
与MnCeMgOx催化剂相比,由于MnCeOx@MgO催化剂具有较大平均孔径(9.35 nm)和活性氧物种比值(Oads/Olatt = 0.88)与较高含量Mn4+ (Mn4+/Mntotal = 45%)和Ce3+ (Ce3+/Ce4+ = 5.6),在同步去除NOx与氯苯的过程中,展现出更好的催化性能。在250℃时,MnCeOx@MgO催化剂最高NOx转化率为77%,在350℃时,最高CB转化率为84%,相比于MnCeOx@MgO的催化剂具有更宽的活性温度窗口。
基金项目
本论文得到国家级大学生创新创业训练计划项目(202011842010)资助。
NOTES
*通讯作者。