1. 引言
糖尿病足(diabetic foot, DF)是糖尿病患者踝关节以远的皮肤及其深层组织破坏,常合并感染和(或)下肢不同程度的动脉闭塞症,严重者累及肌肉和骨组织 [1]。糖尿病足是糖尿病患者致残、致死的主要原因之一,也是造成社会沉重负担的重大公共卫生问题。据估计,全球每20秒钟就有一例糖尿病患者截肢 [2]。长期原因不明发热的患者,其病因主要分为感染性疾病、肿瘤性疾病、免疫性疾病、其他原因和诊断不明 [3]。临床中糖尿病足溃疡患者感染发生率高,40%~70%的足溃疡患者就医时已经发生了感染,也是糖尿病足患者发热最常见原因 [4]。糖尿病患者长期处于高血糖状态,机体免疫应答能力失调,常合并免疫系统疾病,所以当糖尿病足患者发热时,若与足部创口情况不相符,应积极筛查免疫相关疾病。本文报告1例糖尿病足合并反复发热,最终临床诊断糖尿病足合并类风湿性关节炎的诊治过程。
2. 现病史
患者男,62岁,因“发现血糖升高13年,右足破溃10天”于2021年09月29日入院。糖尿病病史13年,不规律降糖药物治疗,血糖控制不详。10天前,患者无明显原因出现右足第二趾肿胀,初未重视,自行处理(具体不详)。后开始发热,伴有寒战,体温最高38.5℃,第二趾远端渐发黑,近端发白,就诊于当地医院,效果不佳,仍持续发热。遂来我院就诊。发病以来,神志清,精神差,大小便正常。近期体重未见明显变化。既往史:自诉体健。个人史:吸烟史30年,约30支/日,未戒烟;否认饮酒史。家族史:否认家族性遗传病史。
3. 体格检查
T:38.3℃,P:112次/分,R:20次/分,BP:120/47 mmHg。营养良好,正常面容。心肺腹(−),病理征阴性。右足足背动脉搏动减弱。右足足背发红、肿胀、皮温明显升高,第2趾颜色发黑、破溃,远端可见坏死组织,伴明显恶臭。右侧小腿肿胀、发红、皮温升高,(图1(A)、图1(B))。评估Wagner分级为4级。
4. 入院后查血常规
WBC 8.03 × 109/L,中性粒细胞百分比58.4%,中性粒细胞4.68 × 109/L,Hb92 g/L;CRP 89.79 mg/L;ESR 130 mm/h;肝功:ALB 25 g/L;电解质:钠121.7 mmol/L,钙1.77 mmol/L,磷0.29 mmol/L,镁0.54 mmol/L;血凝:纤维蛋白降解产物8.29 mg/L,纤维蛋白原6.48 g/L,凝血酶原时间17.30 S,D-二聚体2.85 mg/L;HbA1 c 11.4%;肾功、心肌酶谱及降钙素原均未见明显异常。分泌物培养:大肠埃希菌。双下肢动脉血管彩超示:双下肢动脉硬化伴斑块形成。双侧下肢静脉血管彩超示:右下肢肌静脉内径增宽。心脏彩超及心电图均未见明显异常。
5. 入院诊断
1) 2型糖尿病糖尿病足Wagner4级糖尿病周围血管病变;2) 轻度贫血;3) 低蛋白血症。
6. 诊疗经过
创面愈合过程见图1和图2。监测体温变化见图3。入院后予胰岛素泵降糖,血糖波动于8~14 mmol/L;白蛋白补充蛋白质;阿司匹林肠溶片抗血小板聚集,阿托伐他汀钙片调脂稳斑。入院第2天患足清创见第二趾远端发黑,近端水肿,坏死,予远端坏死趾去除,并送病理,可闻及臭味,双氧水、碘伏、生理盐水反复冲洗,近端沿第2趾中间剪开纵行切口,未见明显脓液;完善血培养检查后,予以亚胺培南Q6抗感染治疗,其体温稍有下降但一直偏高,下午体温达39.5℃,先后予以物理降温、赖氨匹林及地塞米松治疗后体温渐恢复正常范围内。动态复查血常规及血沉指标(表1)。入院第3天复查炎症指标处于上升状态,但患者最高体温较前下降,换药见足部创口较前明显好转;继续亚胺培南抗感染治疗。查右足X片(图4)示:右足第2趾中末节趾骨缺如,右足第4、5近节趾骨、右足第5跖骨远端骨质密度减低。此后体温处于正常范围。第7天血、尿及粪培养回报阴性;换药见右足第2趾近端存留骨质去除,未见明显脓液,少量出血,调整抗生素亚胺培南Q12,监测体温正常。但入院第10天下午体温再次升高,最高体温达38.8℃,予以地塞米松治疗后体温趋于正常。之后13天内未再出现发热。

Figure 1. (A) and (B) Basic conditions of diabetes foot patients at admission on September 29, 2021 (The first day of admission); (C), (D) The second day of admission
图1. (A) (B) 糖尿病足患者入院时足部基本情况2021-09-29(入院第1天);(C) (D) 入院第2天
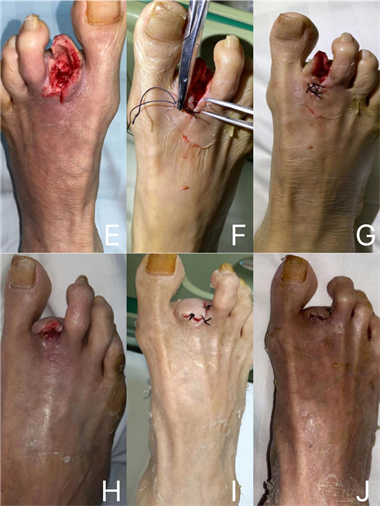
Figure 2. (E) Day 5 of admission; (F) and G were admitted on day 10; (H), (I) and (J) were the recovery of affected feet on the 20th, 30th and 40th day of admission
图2. (E) 入院第5天;(F)和(G)入院第10天;(H) (I) (J)依次为入院第20天、第30天及第40天患足恢复情况
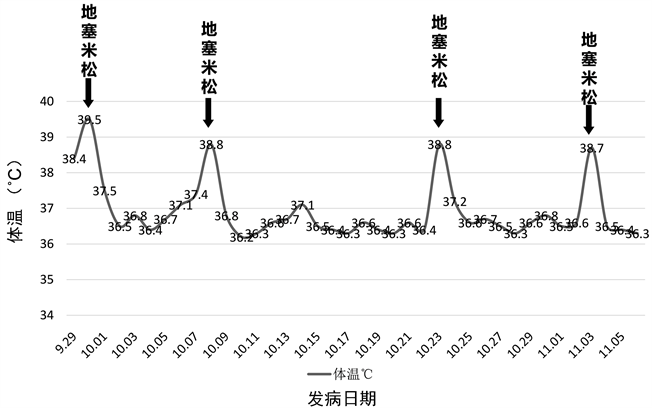
Figure 3. Temperature monitoring after admission
图3. 患者入院后监测体温情况

Table 1. Laboratory test results during hospitalization
表1. 患者住院期间实验室检验结果
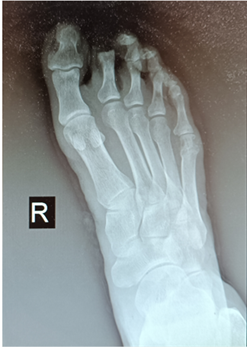
Figure 4. X-ray examination results of the patient’s right foot at admission
图4. 患者入院时右足X线检查结果
在第25天换药见右足第2趾近端缝合处已愈合,予以拆线,远端继续清创,无明显分泌物。其分泌物培养(−)。当天下午14:40左右患者再次出现发热,体温38.8℃,予物理降温及地塞米松降温后体温趋于正常,但复查炎性指标仍较高。综上,患足创面渐愈合,但仍反复发热,且CRP、血沉一直较高,对激素反应好,不排除与免疫系统疾病相关。积极完善自身抗体系列、免疫功能组合、血管炎五项、磷脂三项、抗环瓜氨酸多肽(CCP)抗体、风湿三项等检查。期间再次出现发热,最高体温39℃,予物理降温及地塞米松降温后体温降至正常。
第37天相关结果回报,自身抗体系列、免疫功能组合、血管炎五项、磷脂三项抗体及结核感染T-SPOT均阴性,抗环瓜氨酸多肽(CCP)抗体>200 U/mL,风湿三项:抗O12.7 units/mL,C-反应蛋白198.0mg/L,类风湿因子409 units/mL,风湿免疫科会诊诊断为类风湿性关节炎炎症反应综合征,予以塞来昔布、艾拉莫德片控制症状后,监测体温恢复正常,无关节疼痛,换药见右足第2趾远端创口接近愈合,予以出院。出院1月后电话回访知患者监测体温一直处于正常范围,未再出现发热,无关节肿痛等现象,患足恢复可,可自行下地行走。
7. 讨论
目前糖尿病慢性并发症已经成为糖尿病患者致残、致死的主要原因。大约四分之一的糖尿病患者在他们的一生中会出现糖尿病足溃疡(DFU)。DFU是糖尿病并发症中病情最严重,治疗费用最高,其约占整个糖尿病医疗费用的三分之一,大大增加了社会和家庭的负担。研究表明,感染是DFU的独立危险因素 [5]。DFU患者感染的相关危险因素包括长期血糖控制不佳、高龄、糖尿病史长、足溃疡分级较高、溃疡存在时间长(>30 d)、下肢血管病变严重、保护性感觉丧失、肾功能不全、赤脚步行史等 [6]。本病例中患者长期血糖较高、年龄较大、糖尿病史大于10年且Wagner分级为4级等危险因素,感染发生可能性较大,其入院时出现高热,在外院使用抗生素(具体不详),足部感染较重,炎性指标较高,随即入院经验性给予亚胺培南抗感染治疗,监测患者体温仍反复升高,而其足部创面逐渐趋于愈合,提示其发热原因不局限于足部感染,通过积极完善相关检查,临床科室会诊后诊断为糖尿病足合并类风湿性关节炎。
类风湿性关节炎(rheumatoid arthritis, RA)是一种以侵蚀性、对称性多关节炎为主要临床表现的慢性、全身性自身免疫性疾病。其确切发病机制不明确,多认为是遗传和环境因素共同作用的结果。糖皮质激素(glucocorticoid,GC)具有强大的抗炎作用,能诱导黏附因子、一氧化氮、组织相容性复合体等因子的表达 [7],迅速缓解关节肿痛和全身炎症,也是临床中常用的抗类风湿药物。但也有研究发现,合并2型糖尿病的RA患者疾病活动度更高,糖皮质激素使用可能是其危险因素 [8]。本例患者发现血糖升高13年,足部破溃10天入院,监测血糖明显高,予以胰岛素泵调控血糖,反复发热,予以物理降温及赖氨匹林降温对症治疗其体温仍持续升高,使用地塞米松后患者体温逐渐降至正常,一方面考虑糖皮质激素能显著抑制炎症反应,使体温正常,另一方面糖皮质激素通过其多重免疫调节作用降低了机体的免疫防御能力,出现多次发热,同时掩盖了患者自身关节肿痛的症状,从而掩盖了类风湿性关节炎疾病的进展与治疗。
RA与糖尿病在发病机制上可能具有部分共同通路 [9]。当RA患者疾病活动时,可分泌大量的炎症性细胞因子(IL-6、TNF-α等),介导细胞内炎症反应的信号转导,从而使胰岛素信号转导通路受阻,引起胰岛β细胞数量减少或功能缺陷,导致胰岛素分泌减少,机体处理血糖能力下降,甚至出现血糖异常,而糖尿病足其长期血糖调节异常,免疫力低下,更容易引起RA [10]。且CRP在RA患者中高表达。一项研究招募了100名连续的非糖尿病RA患者和100名年龄和性别匹配的非炎症性疾病对照显示,与健康对照组相比,血清高敏感CRP (hsCRP)在RA患者高表达(5.79 [2.40~10.19] mg/L vs 1.82 [0.88~3.16] mg/L,P < 0.001) [11]。CRP通过激活MAPK信号通路或干扰IRS/PI3K/AKT信号通路(胰岛素受体底物/磷脂酰肌醇3激酶/AKT) [12] 来调节胰岛素信号通路,从而刺激胰岛素抵抗。
关于2型糖尿病,一项对共19,709名参与者的10项前瞻性研究进行的meta分析显示,IL-6水平与2型糖尿病风险之间存在显著的剂量–反应相关性(相对风险,[RR] 1.31, 95%CI 1.17~1.46)。该研究基于22组40,735名参与者的结果,也发现CRP水平的升高与2型糖尿病风险的增加显著相关(RR 1.26, 95%CI 1.16~1.37) [13]。此外,在炎症性多关节炎患者中,胰岛素抵抗与类风湿因子(RF)和抗瓜氨酸蛋白抗体(ACPA) [14] 的存在密切相关。这些发现表明,慢性系统性炎症在RA和2型糖尿病的发病机制中起着重要作用。
越来越多的证据表明,糖尿病患者很容易感染类风湿性关节炎。Tentolouris A.等人证明,与无糖尿病 [15] 的患者相比,已有糖尿病的老年患者更容易发生RA。另一项研究发现,糖尿病患者的女性(20~44岁)更容易患RA [16]。对2535例RA患者进行流行病学问卷调查,其中498例(19.7%)与糖尿病 [16] 共病。糖尿病患者很容易感染RA的原因可能有三个:首先,糖尿病的长期慢性低度炎症可能会系统地导致RA。其次,高血糖环境影响结缔组织的基质成分,加强ROS介导的组织损伤。第三,晚期糖基化终末产物(AGEs)是高糖环境中的代谢产物,在结缔组织中积累。AGEs改变了细胞外基质的结构和功能以及细胞活力,导致软骨损伤和纤维性RA [17]。Arias等人还发现,糖尿病合并RA患者的空腹血糖、总胆固醇和低密度脂蛋白胆固醇(LDL-C) [18] 水平较高。
糖尿病足以下肢的血管和神经病变为主,但大部分患者入院治疗时已发展为糖尿病足溃疡,常伴有感染、贫血、低蛋白血症、心功能不全等营养状态和重要脏器功能的异常,这些异常不仅阻碍足部溃疡的愈合,甚至危及患者的生命。DFU的治疗主要集中在避免下肢截肢。治疗重点是:1) 积极控制感染,2) 诊断及评估可能的血运重建,3) 减轻伤口压力,4) 彻底清创和高级护理改善伤口环境。本例患者存在周围血管病变,伴有感染、贫血、低蛋白血症,通过抗血小板聚集、调脂稳斑、补充白蛋白及抗感染等,同时控制血糖,局部清创、减压、去除坏死组织及缝合等,并嘱绝对卧床,避免患足着地受重力作用,患者入院后10天左右足部创面局部感染基本控制,肉芽组织生长,40天后足部创面愈合良好。
8. 结论
从本例患者的诊疗经过可见,在治疗过程中反复发热,且与足部感染创面不符,提示临床医师糖尿病足患者的发热,不能忽略免疫方面等因素,及时筛查,及时治疗,避免误诊误治,阻止病情的进一步恶化。并且需重视对患者全身情况的改善,调控血糖、血压、血脂,加强营养、彻底清创及抗感染等综合性的治疗,关注患者精神心理方面,达到局部、全身及心理的三合一。
NOTES
*通讯作者。