1. 引言
3,4-二硝基呋咱基氧化呋咱(DNTF)是一种重要的低熔点含能材料,分子中不含有氢元素,流散性好,感度低,高能量密度、低特征信号而被广泛使用于熔铸基炸药载体,可以取代TNT作为液相载体。DNTF的综合性能优于奥克托今(HMX),具有较好的热稳定性,能量大,密度高,安全性好 [1] [2] [3],将DNTF取代硝铵改性双基推进剂中的RDX可以改善推进剂的综合性能 [4]。
在过去的十多年中,氢作为清洁,高效的能源载体引起了广大学者的关注。金属氢化物作为储氢材料之一,因其优异的容积效率和安全性使其成为新能源领域的热门研究对象 [5] [6]。金属氢化物MgH2是一种相对廉价的储氢材料,储氢量为7.6% [7],大约在287℃发生热分解,具有较高的热稳定性,在含能材料领域内具有较大的应用潜力,将MgH2放进含能材料中其主要作用体现为促进含能材料的热分解过程,提高其能量水平 [8]。Hradel等 [9] 对含有MgH2的TNT的炸药性能进行研究,研究发现MgH2可以提高TNT的做功能力。勒丽美等人通过氧弹量热法和DSC法测试得到DNTF中加入5%的氢化镁后体系燃烧热提高了6.5% [10]。任晓宁等人研究了DNTF与不同催化剂体系的热分解,研究认为PbO、h-Cu、己二酸铜、硬酯酸铅均能催化DNTF的分解,催化效果很明显,DNTF有望成为推进剂中的氧化剂 [11]。JIN Limei通过ARC法测试研究了MgH2对硝化棉(NC)的热分解特性的影响,发现MgH2能提高NC的分解速度,催化了NC的热分解 [12]。刘磊力等用MgH2催化高氯酸铵(AP)的热分解,结果表明MgH2可以显著降低AP的分解温度,增大AP的表观分解热,对AP的热分解过程有显著的催化作用 [13]。在AP/Al/HTPB复合推进剂中,MgH2通过催化AP的分解起到降低推进剂的热分解温度作用,同时推进剂反应热得到增强 [14]。
综上所述,MgH2在含能材料领域中具有巨大的应用潜力,但是目前关于MgH2对低熔点含能材料DNTF热分解特性影响鲜有报道。DNTF是一种不含有氢元素的炸药,而MgH2是种富含氢元素的炸药,MgH2可有效弥补DNTF缺氢的不足,提高体系的能量。为此,本研究拟对不同配比的DNTF与MgH2进行研究,配比分别为98:2、96:4、94:6、92:8,对不同配比的DNTF/MgH2进行差式扫描量描量热法进行测定,通过热分解动力学和热力学进行分析,研究MgH2对DNTF分解过程的影响,为以后混合含能材料的配方设计提供参考。
2. 实验
2.1. 实验材料
MgH2和DNTF均由西安近代化学研究所提供。DNTF为白色颗粒状固体,带有少量结晶水、熔点约为110℃,分子式为C6N8O8,氧平衡值为−20.5%,属于负氧平衡炸药,其分子结构式如图1所示。MgH2为灰色粉末状固体。

Figure 1. Molecular structure of DNTF
图1. DNTF的分子结构图
2.2. 测试条件与仪器
差示扫描量热法(DSC):所用仪器为上海精密仪器公司生产DSC-A型差示扫描量热仪,在产品测试前,用高纯的In、Sn和Zn对仪器的测量温度进行标定。采用密封坩埚法,试验用试样量约0.5 mg;升温速率分别设定为5℃/min,10℃/min,15℃/min,20℃/min。
2.3. 实验步骤
MgH2使用之前需用石英研磨棒研磨成粉末状,DNTF使用前先放置在烘箱内2 h,烘箱内温度为50℃,去除DNTF中含有的少量水分,然后研磨成粉末状。然后将DNTF于MgH2按照不同配比进行实验。使用密封坩埚进行实验,防止DNTF出现挥发导致放热量测试不准。DNTF与MgH2之间的质量比分别按照:98:2 (DM1),96:4 (DM2),94:6 (DM3),92:8 (DM4)、90:10 (DM5)四种比例测试,实验所用坩埚为完全密封坩埚,防止DNTF因加热挥发质量损失导致热分解过程无法被准确测定出来。升温速率分别采用5℃/min,10℃/min,15℃/min,20℃/min。
3. 实验结果及分析
3.1. 实验测试结果
如下图所示为不同比例的DNTF/MgH2的DSC测试结果。当加热温度为110℃左右时,DNTF出现一个熔融吸热峰,这是DNTF的熔融过程,当温度升高时,分子热运动的动能加快,导致结晶被破坏,分子由固相变成液相。DNTF是一个易挥发物质,如果将DNTF放置在敞口坩埚上进行加热,则DNTF不会出现第二个分解放热峰。如下图2所示为DNTF:MgH2 = 98:2的测试比例图,升温速率为10℃/min,在敞口环境中只出现了第一个熔融峰温,随后由于DNTF的挥发性,导致DNTF来不及发生热分解就已经挥发完毕,这也说明了使用密封坩埚的必要性。
如下图3~8所示,熔融吸热峰的面积均较小,吸收的热量也较小;然后是分解放热峰,分解放热峰的面积相较于吸热峰较大。当升温速率提高时,熔融峰温向高温区移动,但变化较小,都约为110.0℃,但当升温速率为20℃/min时,熔融峰温有较大提高,约为116.0℃;而放热峰面积随着升温速率的提高而增大,放热峰温大小也随之向高温区移动。当DNTF中加入MgH2后,分解放热峰发生了降低,这说明MgH2促进了DNTF的热分解。

Figure 2. Test results of sealed crucible and open crucible
图2. 密封坩埚和敞口坩埚环境条件下的测试结果

Figure 3. DSC curves of DNTF at different heating rates
图3. DNTF不同升温速率下的DSC曲线

Figure 4. DSC curve of DNTF and MgH2 with mass ratio of 98:2
图4. DNTF与MgH2的质量比为98:2的DSC曲线

Figure 5. DSC curve of DNTF and MgH2 mass ratio of 96:4
图5. DNTF与MgH2的质量比为96:4的DSC曲线

Figure 6. DSC curve with DNTF and MgH2 mass ratio of 94:6
图6. DNTF与MgH2的质量比为94:6的DSC曲线
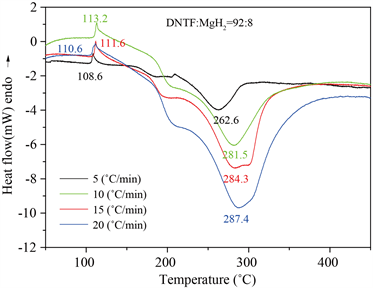
Figure 7. DSC curve with mass ratio of DNTF to MgH2 at 92:8
图7. DNTF与MgH2的质量比为92:8的DSC曲线
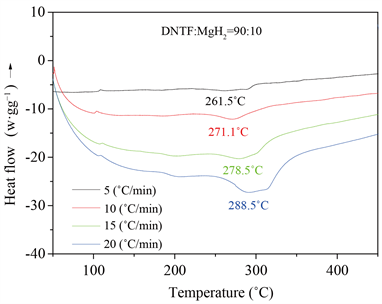
Figure 8. DSC curve with DNTF and MgH2 mass ratio of 90:10
图8. DNTF与MgH2的质量比为90:10的DSC曲线
3.2. 热分解动力学研究
如下表1所示为四种不同升温速率下的试样对应分解峰温以及采用Kissinger法 [15] 和Ozawa法 [15] 计算得到的表观活化能E和指前因子A,它们是重要的热分析动力学参数,kissinger法和ozawa法都是基于DSC曲线的第一分解放热峰温度进行计算,计算方程如下公式(1) (2)所示:
(1)
(2)
Tp——DSC曲线第一分解放热峰的峰顶温度(K),
R——气体常数(8.314 J/(K∙mol),
Β——线性升温速率(K/min),
——反应动力学函数,
A——指前因子(1/s),
EK——Kissinger法计算的表观活化能(kJ/mol),
E0——Ozawa法计算的表观活化能(kJ/mol)。

Table 1. Decomposition peaks and activation energies of DNTF/MgH2 at different heating rates
表1. DNTF/MgH2在不同升温速率的分解峰温和活化能
表观活化能指活化状态分子与普通分子之间的能量之差。过渡态理论认为反应物经过过渡态而转变为产物,过渡态分子较反应物分子高出的能量叫做活化能。活化能越小,反应越容易发生,热安定性也就越差。随着MgH2的比例逐渐上升时,混合物的分解峰温也逐渐降低,通过kissinger法和ozawa法计算出的活化能也逐渐降低,这说明MgH2促进了DNTF的热分解反应,使得更多的反应物分子变成活化分子,这也增大了反应速率。当DNTF处于液态时,MgH2附着在DNTF表面上促进DNTF发生热分解,当MgH2含量较少时,DNTF表面与MgH2能结合的反应活性位点尚未饱和,此时MgH2含量越多,反应活性越大,热分解反应越容易发生,活化能也就越低。当DNTF表面的反应活性位点被MgH2饱和后,继续增加MgH2后对DNTF分解影响较小,分解反应活化能不再降低。
MgH2的比例由8%上升到10%时,分解峰温略微降低,活化能几乎不变。这表明混合物的热安定性与MgH2并不是简单的线性关系,当MgH2的含量较大时,DNTF/MgH2的热安定性趋于稳定。
3.3. 热分解热力学研究
热爆炸临界温度Tb是评价含能材料热安全性的重要指标 [16]。可以通过张–胡–谢–李方程计算得到。Tb越小,热安全性越差。可以通过公式(3)和(4)计算得到;通过公式(5) (6) (7)可以计算出活化焓∆H≠、活化吉布斯自由能∆G≠、活化熵∆S≠。
(3)
(4)
(5)
(6)
(7)
式中:a、b、c——常数,Tp0——升温速率β趋向于0 K∙min−1时的放热峰温(K),Tp——升温速率β = iK∙min−1时的第一放热峰温。Tb——热爆炸临界温度(K),KB——玻尔兹曼常数1.3807 × 10−23 J∙K−1,h是普朗克常数,数值为6.626 × 10−34 J∙S,R——理想气体常数,8.314 J/K∙mol,∆S≠——活化熵,J∙K−1∙mol−1,∆H≠——活化焓,kJ∙mol−1,∆G≠——活化自由能,kJ∙mol−1。

Table 2. Thermal decomposition parameters and thermodynamic calculation results of DNTF/MgH2
表2. DNTF/MgH2的热分解参数以及热力学计算结果
热爆炸临界温度Tb的大小顺为:DNTF > DM1 > DM2 > DM3 > DM4 > DM5,DNTF/DM1/DM2/DM3的Tb很接近,DM4的Tb值比DNTF的Tb值降低了63.9 K。这说明当MgH2的含量增加到8%时,DNTF的热安全性发生了很大的降低。
熵代表了系统的混乱度,熵增则表明系统混乱度增加。ΔS≠表示过渡态的活化络合物的混乱度和反应物之差,ΔS≠大于0则表示活化络合物的混乱度比反应物的大,反应位点的活泼性也越高。由表2可知,活化熵的大小比较为DNTF > DM1 > 0 > DM2 > DM3 > DM4 > DM5,DNTF的ΔS≠略微大于DM1,由此可知当MgH2的比例在2%时,DNTF活化络合物的活泼性改变较小。当MgH2的含量在4%以上时,活化熵小于0,此时过渡态的活化络合物的混乱度较低,反应位点的活泼性较低。活化焓表示反应物到活化络合物过程中标准焓的增量。过渡态理论认为,活化焓数值大于零活化过程是吸热的,活化吉布斯自由能数值大于零则表示正向的活化反应为非自发反应。DNTF以及和MgH2的混合物的ΔH≠和ΔG≠皆大于零,这说明混合物正向活化反应皆是吸热且非自发反应。
4. 结论
1) MgH2对DNTF的熔融吸热过程没有影响;MgH2可以显著促进DNTF的热分解过程,降低DNTF的分解放热峰温,通过放热峰温计算出的分解活化能和指前因子也得到降低。
2) 随着MgH2含量增加,MgH2对DNTF的热分解促进作用也逐渐增强。当MgH2的含量大于8%时,DNTF的热安全性发生很大降低,在实际应用中应该控制MgH2的用量。