1. 引言
大蝎子草[Girardinia diversifolia (Link) Friis]来源于荨麻科蝎子草属大蝎子草的全草或根部 [1]。其功效有祛风解表、利气消痰、清热解毒 [2] [3],常被用于咳嗽痰多,水肿,外用治疮毒,根鲜用捣烂外敷,治骨折,还用于治疗中风不语、跌打损伤、皮肤瘙痒 [4]、肝损伤、肾炎、前列腺肥大、肿瘤以及血管栓塞性等心血管疾患 [5] [6]。经调查研究,大蝎子草为苗药红禾麻的一种来源,其产量和用量远超于红禾麻的另一基源珠芽艾麻,大蝎子草为一种少数民族常用药,但对其研究尚浅,仍有待发掘。
植物多糖的来源较广泛,不同种的植物多糖的分子构成及分子量各不相同,有些植物多糖如淀粉、果胶、纤维素等早已经成为人们日常生活中不可缺少的一部分。多糖具有调节免疫 [7]、抑制肿瘤 [8]、延缓衰老、抗疲劳作用 [9]、抗氧化 [10]、保肝、护肝 [11] 等多种作用。经研究发现大蝎子草含有一定量的多糖,但对其多糖提取工艺研究方面甚少,因此,本实验采用响应面法对其水溶性总多糖提取工艺进行优化,也为大蝎子草药材质量标准的完善提供一定的参考依据。
2. 仪器与材料
2.1. 试验药材与试剂
试验用大蝎子草均产自贵州贵阳,经贵州中医药大学魏升华教授鉴定为荨麻科蝎子草属植物大蝎子草[Girardinia diversifolia (Link) Friis]的干燥全草。葡萄糖(天津市科密欧化学试剂有限公司,批号:20200110)、硫酸(重庆万盛川东化工有限公司,批号:20210101)、苯酚(双林化工试剂厂,批号:20201005)、无水乙醇(重庆川东化工(集团)有限公司,批号:20210801),蒸馏水,超纯水均由贵州中医药大学药物分析实验室提供。
2.2. 仪器
数字控温电热套(天津市泰斯仪器有限公司,98-I-C);超声波清洗器(昆山市超声仪器有限公司,KQ-100E);电子天平(上海蒲春计量仪器有限公司,JE2002);高速冷冻离心机(赛默飞世尔科技有限公司,Thermo ST16R);紫外分光光度计(日本岛津,UV2501PC);旋转蒸发仪(上海亚荣生化仪器厂,RE2000A);数显恒温水浴锅(常州普天仪器制造有限公司,HH-4);电子分析天平(瑞士梅特公司,XS205)。
3. 实验方法与结果
3.1. 标准曲线的绘制
精确称取干燥恒重的无水葡萄糖50.30 mg,置于50 mL容量瓶中,以蒸馏水溶解并定容至刻度线,摇匀,精密吸取5 mL,置于50 mL容量瓶中,加蒸馏水至刻度线定容,摇匀。即得到浓度为0.1006 mg/mL的葡萄糖对照品溶液。
分别精密吸取上述葡萄糖对照溶液0.2 mL、0.4 mL、0.6 mL、0.8 mL、1.0 mL、1.2 mL置于带塞的试管中,加入蒸馏水定容至2 mL,摇匀,各加入1 mL 5%苯酚溶液摇匀后,迅速加入5 mL浓硫酸,摇匀,沸水浴显色20 min,待冷却至室温。以相应的显色剂为空白对照,在483 nm波长下测定吸光度,以吸光度A为纵坐标(Y),以浓度C为横坐标(X)绘制葡萄糖标准曲线。
其线性回归方程为
,R2 = 0.9993,表明了该线性方程在葡萄糖浓度在0.00252~0.01509 mg/mL范围内与吸光度有良好的线性关系。
3.2. 大蝎子草水溶性多糖提取
准确称取大蝎子草药材5 g,以相应的比例加入蒸馏水,浸泡相应的时间,再按相应的时间提取两次。滤液合并,真空浓缩至50 mL。精密吸取浓缩液1 mL加入4 mL无水乙醇,混匀,冷藏24 h,离心,倒出滤液,再用80%乙醇分别进行洗涤滤渣两次。得到的粗多糖滤渣用蒸馏水溶解并定容至10 mL,即得到大蝎子草水溶性多糖溶液,作为供试品溶液,按“3.1”项下方法测定吸光度并计算待测液中水溶性总多糖含量。总多糖含量公式:
(1)
式(1)中:W为大蝎子草总多糖含量(mg/g);C为总多糖的浓度(mg/mL);V为待测液体积;X为稀释倍数;M为大蝎子草质量(mg)。
3.3. 方法学考察
1) 精密度试验按“3.1”项下方法测定葡萄糖对照品溶液吸光度6次,计算RSD为0.02 %,表明精密度良好。
2) 稳定性试验按“3.2”项下方法提取总多糖后,分别在0 min、30 min、60 min、90 min、120 min、150 min时按“3.1”项下方法测定吸光度值,计算的RSD为0.03%,表明大蝎子草总多糖提取液在150 min内稳定性良好。
3) 重复性试验按“3.2”项下方法提取6份样品溶液,计算其总多糖含量RSD为0.03%,表明该方法重复性良好。
4) 加样回收率试验精密称取5 g已知含量大蝎子草干燥药材6份,标准品加入量与所取供试品含量之比为1:1的比例加入葡萄糖标准品,按“3.2”项下方法制备待测液溶液,并计算回收率,平均回收率为101.46%,RSD为1.81%。
3.4. 单因素考察
按“3.2”项提取多糖溶液的方法,分别对浸泡时间、料液比、提取时间进行单因素试验。浸泡时间设置5个水平:20 min、40 min、60 min、80 min、100 min;料液比设置5个水平:1:10 g/mL、1:15 g/mL、1:20 g/mL、1:25 g/mL、1:30 g/mL;提取时间设置5个水平:30 min、60 min、90 min、120 min、150 min。按“3.1”项进行显色,在483 nm的吸收波长下测定吸光度并计算其大蝎子草多糖含量。每个样品平行3次。
3.4.1. 浸泡时间对总多糖含量的影响
经浸泡时间考察可知(如图1)随着浸泡时间的延长黔产大蝎子草的水溶性多糖含量呈先增后减的趋势,当浸泡时间到达40 min时,黔产大蝎子草的水溶性多糖含量达到了7.71 mg/g,随着浸泡时间继续增加其多糖含量开始降低。根据试验的结果,选择提取黔产大蝎子草水溶性多糖最好的浸泡时间为40 min。

Figure 1. Effect of soaking time on total polysaccharide content
图1. 浸泡时间对多糖含量的影响
3.4.2. 料液比对多糖含量的影响
经料液比考察可知(如图2),随着料液比的增大黔产大蝎子草的水溶性多糖含量呈先增后减的趋势,料液比为1:15 g/mL时,黔产大蝎子草的水溶性多糖含量达到了8.47 mg/g,在料液比大于1:15 g/mL之后其多糖含量开始降低,根据试验的结果,选择提取黔产大蝎子草水溶性多糖最好的料液比为1:15 g/mL。
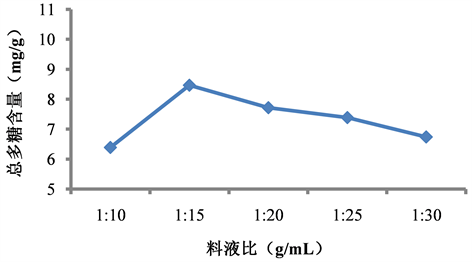
Figure 2. Effect of solid-liquid ratio on total polysaccharide content
图2. 料液比对多糖含量的影响
3.4.3. 提取时间对多糖含量的影响
经提取时间考察可知(如图3),随着提取时间的增加黔产大蝎子草的水溶性多糖含量呈先增后减的趋势,提取时间为90 min时,大蝎子草的水溶性多糖含量达到了10.24 mg/g,在提取时间大于90 min之后其多糖含量开始降低。根据试验的结果,选择提取黔产大蝎子草水溶性多糖最好的提取时间为90 min。
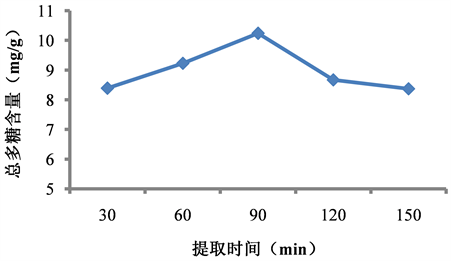
Figure 3. Effect of extraction time on polysaccharide content
图3. 提取时间对多糖含量的影响
3.5. 响应面法优化设计
响应面法是一种实验寻优的方法,根据单因素考察试验的结果,利用软件Design-Expert8.0.6进行响应面试验。采用Box-Behnken来设计三因素三水平试验,以浸泡时间(A)、料液比(B)、提取时间(C)为变量因素,大蝎子草水溶性总多糖含量(Y)为响应值,优化大蝎子草水溶性多糖的提取工艺。
3.5.1. Box-Behnken试验因素与水平
在单因素试验基础上,用 Design-Expert8.0.6软件来设计三因素三水平试验,得出Box-Behnken试验因素与水平见表1。

Table 1. Factors and levels of the experiment
表1. 设计实验因素与水平
3.5.2. 响应面方案及结果
根据表1 Box-Behnken试验因素与水平,采用Box-Behnken来设计提取黔产大蝎子草水溶性多糖的最优试验,Box-Behnken设计方案与试验结果见表2。利用Design-Expert8.0.6软件对各因素进行二次回归拟合,二次回归模型的方差分析结果见表3。

Table 2. Design and results of Box-Behnken experiment
表2. Box-Behnken试验设计和结果
根据上述单因素试验结果,利用Design-Expert8.0.6软件对试验结果进行回归分析,得到多元二次回归方程为:

Table 3. Results of variance analysis
表3. 方差分析结果
注:*表示差异显著(P < 0.05),**表示差异极显著(P < 0.01)。
经响应面方差分析(表3)可知,本实验建立回归模型的P < 0.0001,极显著,失拟项P = 0.5257 > 0.05,不显著,表明该模型对黔产大蝎子草水溶性多糖提取的影响显著性极高;模型相关系数R2 = 0.9823,表明该模型的拟合情况良好,98.23%的试验值可以利用该模型来进行预判;变异系数为1.92%,表明了该试验的误差小,该模型可以用于黔产大蝎子草水溶性多糖的提取含量进行预判。一次项A、B、C其P值得大小为B > A > C,A、C项表示极显著(P < 0.01),B项不显著(P > 0.05);交互项AB、AC、BC其P值的大小为AB > BC > AC,AC、BC项极显著(P < 0.01),AB项不显著(P > 0.05);二次项A2、B2、C2其P值得大小为C2 = A2 = B2 < 0.0001,A2、B2、C2项均表示极显著(P < 0.01)。根据F值的大小可以推断各因素对总多糖提取量的影响程度为:C > A > B。
3.5.3. 响应面分析
各因素之间的交互作用对提取黔产大蝎子草水溶性多糖含量的影响见图4~6。曲面越陡峭,等高线越密集呈椭形时,表示两因素间的交互作用越显著。从图中可以看出,浸泡时间和料液比(AB)、浸泡时间和提取时间(AC)及料液比和提取时间(BC)的响应面图开口是向下的,存在一个最高点。等高线图呈椭圆形,表明各种因素的交互作用对黔产大蝎子草水溶性多糖含量的影响极显著(P < 0.01)。
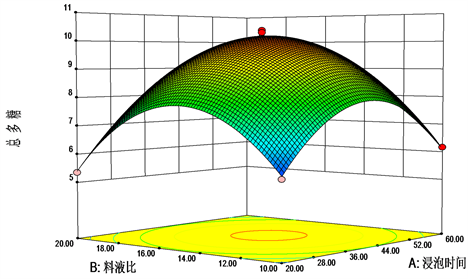
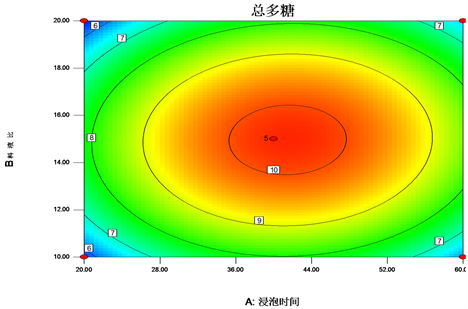
Figure 4. Response surface and contour diagram of the effects of soaking time and solid-liquid ratio on total polysaccharide content
图4. 浸泡时间和料液比对总多糖含量影响的响应面和等高线图


Figure 5. Response surface and contour diagram of the effects of soaking time and extraction time on total polysaccharide content
图5. 浸泡时间和提取时间对总多糖含量影响的响应面和等高线图
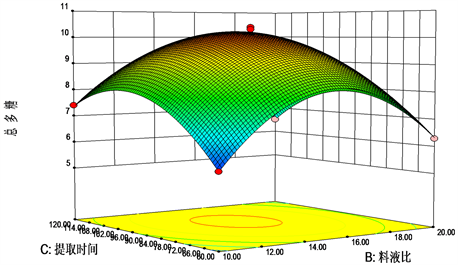
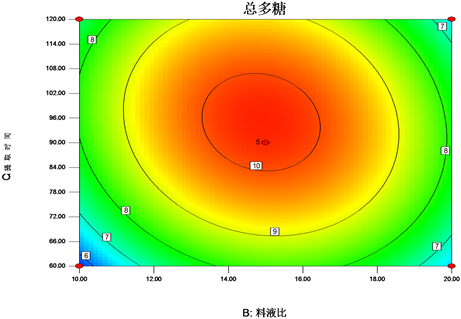
Figure 6. Response surface and contour diagram of solid-liquid ratio and extraction time on total polysaccharide content
图6. 料液比和提取时间对总多糖含量影响的响应面和等高线图
3.6. 验证试验
通过Design-Expert8.0.6软件对响应面结果的分析,得到黔产大蝎子草水溶性多糖的最佳提取工艺为:浸泡时间53.43 min,料液比1:15.03 g/mL,提取时间90.33 min,在该条件下,黔产大蝎子草水溶性多糖含量的预测值为9.46 mg/g。为方便实际操作,将预测的工艺条件调整为浸泡时间53 min,料液比1:15 g/mL,提取时间90 min。在本次调整的预测条件下,进行3次验证试验。选择三批不同的药材,平行测定3次,按“3.2”项下方法提取多糖溶液与“3.1”项下方法进行显色,在483 nm的吸收波长下测定吸光度并计算其多糖含量,得出实际的验证试验的多糖含量为10.60 mg/g,较预测值大,RSD值为0.08 %,表明该模型可以运用到黔产大蝎子草水溶性多糖的提取工艺。
4. 结论
研究了浸泡时间、料液比及提取时间对黔产大蝎子草水溶性多糖提取的影响。根据单因素考察试验的结果,利用Design-Expert8.0.6软件和Box-Behnken来设计三因素三水平试验,采用响应面分析法建立黔产大蝎子草水溶性多糖提取工艺的二次回归模型,并分析各因素对响应值的影响。试验得出黔产大蝎子草水溶性多糖提取的最佳工艺为:浸泡时间53 min,料液比1:15g/mL,提取时间90 min,在该条件下,实际得到大蝎子草水溶性多糖的含量为10.60 mg/g。
5. 讨论
本实验前期考察了超声提取、冷浸提取和加热回流三种提取方法,结果表明,回流提取所得多糖含量较高,说明大蝎子草多糖易溶于热水,初步可判定大蝎子草多糖分子量小,分支程度低,可能存在大量低聚糖,具体详细成分仍有待研究。根据多糖不溶于高纯度醇的性质,本实验采用水提醇沉的方式进行提取大蝎子草总多糖,并利用苯酚–硫酸法进行测定。
与常用的均匀设计、正交设计、星点设计等方法比较,Box-Behnken响应面法采用多元线性和二次项模型拟合能提高实验精确度并预测最佳点。在单因素试验中,随着浸泡时间的增加,总多糖呈现了一种先增加后降低的趋势,可能原因为在一定量的溶剂里,随着浸泡时间的增加,水溶性多糖会不断地溶解出来,随着时间继续增长,药材里的其它水溶性成分也会溶解出来,导致多糖含量的降低;在单因素料液比考察中,料液比达到一定高度时,总多糖含量下降,可能原因为在提取黔产大蝎子草水溶性多糖时,太低的料液比不能使黔产大蝎子草药材与溶剂有充分的反应,料液比过高,其它的水溶性杂质也会溶出从而抑制了多糖的溶出 [11] [12];在单因素提取时间的考察中,随着提取时间的增加,总多糖仍呈现出一种先增后减的趋势,可能原因为随着时间的延长可以提高多糖的提取含量,但时间过长则会使多糖的结构改变,从而降低含量 [13]。
时至今日,国内外对多糖的研究越来越被重视,不仅因为多糖含有丰富的药理活性成分且作用十分显著。本实验所用的黔产大蝎子草药材中含有大量的多糖资源,且尚未发现响应面法对大蝎子草总多糖进行工艺优化的文献及报道,故本实验采用响应面法对其优化,以浸泡时间、料液比和提取时间为考察因素,实验结果表明,该方法稳定、重复性好、操作便捷、简单易行,该实验可为大蝎子草质量标准的建立奠定基础。
基金项目
国家重点研发计划(2019YFC1712500);贵州省科技计划项目(黔科合后补助[2020]3003);贵州中医药大学科研创新和探索专项(2019YFC171250102)。
参考文献
NOTES
*通讯作者。