1. 引言
恶性高血压是由原发性高血压和继发性高血压引起的一组临床综合征。又称加速型恶性高血压或恶性期高血压。它是最严重的动脉性高血压,通常涉及心脏、大脑、肾脏和其他实质器官,是至少有三种不同的靶器官同时受损(肾脏、心脏、大脑、微血管)的疾病 [1]。恶性高血压的重要病理特征之一是在急骤异常升高的血压的打击下,出现血管内皮功能障碍、小动脉坏死或纤维化,肾脏是主要受累靶器官。据报道,如果不治疗,预期寿命将不到24个月,治疗后5年生存率为90% [2]。慢性肾功能不全和终末期肾病是众多恶性高血压病人的结局,最终进入维持透析或肾移植 [3]。本研究纳入10年间,252例恶性高血压患者,通过详细分析病因、起病时的状态、治疗药物的选择,肾功能的转归情况,探讨不同治疗方式对病人肾脏预后的影响。
2. 对象和方法
1) 研究对象选自2010年6月至2020年6月间在青岛大学附属医院肾内科接受治疗的307例恶性高血压患者,恶性高血压诊断标准 [2] [4]:① 血压在短时间内迅速升高,舒张压(DBP) ≥ 130 mmHg;② 伴眼底出血或视乳头水肿(即Keith-Wagener分级III或IV级)或DBP虽未≥130 mmHg但出现急性靶器官损害伴眼底改变(眼底病变Keith-Wagener分级为III或IV级,即眼底出血及棉絮状渗出,伴或不伴视乳头水肿)。排除标准:① 年龄 < 18岁;② 随访次数 < 3次(54例);③ 就诊时为肾移植状态(1例);④ 近1月使用过肾素血管紧张素系统抑制剂及醛固酮抑制剂,共252例患者纳入本研究,70例患者就诊时可明确诊断为尿毒症(ESRD),182例患者为急性起病。本研究经青岛大学附属医院伦理委员会批准(QYFYWZLL26469)。
2) 研究方法与临床资料:收集患者基本资料包括年龄、性别、收缩压(SBP)、舒张压(DBP)、心脏射血分数(LVEF%)等情况。收集实验室数据包括肾小球滤过率(eGFR)、肌酐、尿素氮、24小时尿蛋白、肾素、血管紧张素I、血管紧张素II、醛固酮、钾离子、脑钠肽(BNP),蛋白尿通过24小时尿液收集来评估,肾素–血管紧张素系统使用酶联免疫法测定。估计的eGFR是根据慢性肾病流行病学合作(CKD-EPI)方程计算。研究终点为长期维持性透析治疗或eGFR < 15 ml/(min∙1.73 m2)或死亡。血压达标是依据2012年、2021年KDIGO指南及2018年欧洲高血压指南,推荐血压控制目标为≤130/80 mmHg,达到血压控制目标视为血压达标。
3) 统计学分析统计分析采用SPSS21.0和Graphpad Prism 8.0软件。对计量资料分布情况进行正态性分析,计量资料符合正态分布的用均数±标准差(
)表示,计量资料符合正态分布及方差齐性的两组间比较,采用独立样本t检验;若符合正态分布但方差不齐,组间比较采用U检验,非正态分布的计量资料用M(Q25, Q75)描述,组间比较采用Kruskal Wallis秩和检验;计数资料采用例(%)表示,组间比较采用c2检验;Fisher的精确检验比较两组透析患者间的疗效;采用Kaplan-Meier生存曲线、Log-rank检验比较两组患者之间肾脏生存率的差异。P < 0.05视为差异有统计学意义。
3. 结果
3.1. 一般资料
182例急性起病的患者中,单纯药物治疗组172例:RASI组137例,其中58人使用了血管紧张素受体阻滞剂(ARB),79人使用了血管紧张素转换酶抑制剂(ACEI)。单纯药物治疗组未使用RASI组(N-RASI) 35例,患者入院时肌酐高于265 μmol/L,使用钙离子阻滞剂(CCB)、肾上腺素能受体阻滞剂等其他类型降压药物或者联合使用。10例患者符合急症透析的指征,初始eGFR < 15 ml/(min∙1.73 m2),但其肾脏大小起病就诊时正常,透析治疗的同时选择使用RASI联合。其中腹膜透析组(PD) 6例,血液透析组(HD) 4例。下表为初诊急性起病的182例患者入院时基础资料(表1)。

Table 1. Clinical data of hospitalized patients with malignant hypertension
表1. 恶性高血压入院患者的临床资料
3.2. 临床资料
在恶性高血压患者中,单纯药物使用RASI治疗组(N = 137)、单纯药物治疗未使用RASI组(N = 35)、急性起病采取血液透析和腹膜透析组(N = 10)三组患者RAAS系统皆有明显的激活。之间无显著差异。详见下表2:

Table 2. RAAS activation in three groups
表2. 三组患者RAAS激活情况
注:RASI组与N-RASI组比较,#P < 0.05。
对于仅用药物治疗的患者,因为起点的血清肌酐与eGFR有差异,故以eGFR的变化值ΔeGFR作为指标评估在随访期内使用RASI组与未使用RASI组肾功能的变化。可见治疗达到6个月时eGFR达到比较明显的改善(∆eGFR 9.65 ± 10.79 mml/(min∙1.73 m2)),而N-RASI组在6个月时的eGFR却减少了−2.62 ± 5.11 ml/(min∙1.73 m2)。3年后RASI组呈现出更加明显的肾功能改善∆eGFR为18.26 ± 16.84 ml/(min∙1.73 m2),4年后为25.66 ± 12.30 ml/(min∙1.73 m2)。详见图1:
 (a)
(a)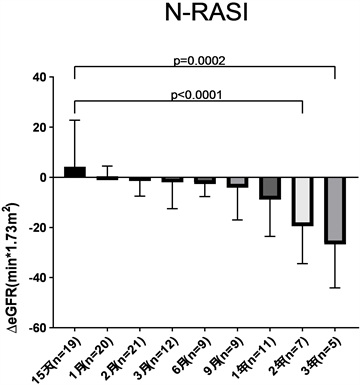 (b)
(b)
Figure 1. (a) Changes in eGFR levels (∆eGFR) at different treatment time points in patients using RASI (ACEI/ARB) since initial treatment. (b) Changes in eGFR levels (∆eGFR) at different treatment time points in patients without RASI
图1. (a) 自初治开始使用RASI (ACEI/ARB)的患者在不同治疗时间点eGFR水平变化(∆eGFR)。(b) 未使用RASI的患者在不同治疗时间点eGFR水平变化(∆eGFR)
急性起病MHT患者肾脏大小正常(肾脏长轴左侧为10.9625 ± 1.03 cm,右侧为10.9375 ± 1.34 cm)。接受腹膜透析和血液透析治疗后肾功能恢复情况,详见图2。共有10例患者接受透析。6例腹膜透析,4例血液透析。通过分析发现,6例接受腹膜透析的患者,治疗前后血清肌酐改善明显,由1018.62 ± 429.47 μmol/L降为193.82 ± 81.92 μmol/L,两年内全部拔管脱离了腹膜透析。4例血液透析患者仅有2人脱离透析,1例进入长期维持性血液透析,1例透析1年后死亡。采用Fisher的精确检验评价两组疗效,P = 0.133,腹膜透析脱离透析的几率为100%,血液透析脱离透析的几率为50%。
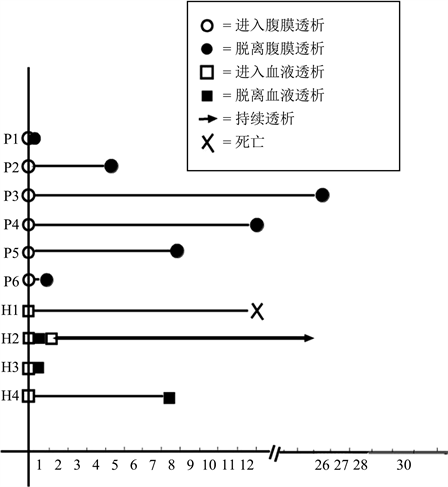

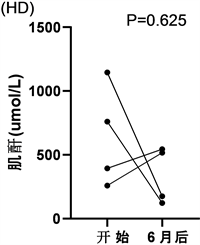
Figure 2. Dialysis timeline of 10 dialysis patients: from start to end. (PD) observation on the curative effect of peritoneal dialysis patients after 6 months. (HD) observation on the curative effect of hemodialysis patients after 6 months
图2. 10例透析患者的透析时间线:从开始到结束。(PD) 腹膜透析患者6个月后的疗效观察。(HD) 血液透析患者6个月后的疗效观察
在使用RASI患者中,对血压控制达标与否进行Kaplan-Meier生存分析,共有105患者进入分析。其中65例患者血压达标,1例进入肾脏替代治疗,1例死亡,全因死亡率为1.5%。40例未达标患者,其中7例进入终末期肾脏替代治疗,19例达到ERSD,3例死亡,全因死亡率为7.5%。其两者之间的肾脏生存率存在统计学差异,P < 0.0001 (图3)。
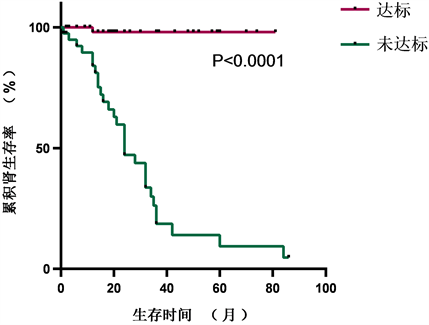
Figure 3. Renal survival analysis of patients with and without standard blood pressure based on RASI
图3. RASI使用基础上血压达标患者与未达标患者的肾生存分析
4. 讨论
肾素、血管紧张素II (AngII) [5] 和醛固酮等活性肽在人体有重要的生物学作用 [6] [7]。肾素–血管紧张素系统在恶性高血压患者中的激活在人类和实验动物中已被证实。肾–肾上腺相互作用异常导致肾素和醛固酮分泌过多。突然激活异常升高的肾素和醛固酮被认为是一种血管毒素。原发性疾病的进展、焦虑、突然过度激动的情绪都会激活交感神经系统,引起血管收缩,同时肾素血管紧张素醛固酮系统进一步激活。除血压急骤升高,损害多脏器外,RAAS激活可以直接导致肾间质纤维化 [8] 和肾小管萎缩 [9]。血管紧张素II (ANG)通过刺激转化生长因子(TGF-β1)介导上皮–间充质转分化(EMT)并引起肾间质纤维化,EMT使肌成纤维细胞增多导致肾间质纤维化 [10]。恶性高血压患者肾毛细血管数明显低于非恶性高血压患者 [11],肾脏会处于持续缺血状态,肾小血管的收缩,进一步加重肾缺血,刺激RASS激活,形成恶性循环。RAAS阻断剂可抑制肾纤维化过程中TGF-β1的表达 [12],抑制上皮–间充质转分化(EMT),抑制肾间质纤维化发生 [13]。大量数据支持RASI能有效延缓慢性肾脏疾病的进展 [9] [14]。
本研究中,RAAS阻滞剂,包括ACEI和ARB是主要的治疗药物 [15] [16] [17],以短效卡托普利最常用最关键。在一般慢性肾脏病中,血肌酐高于3 mg/dl (265 μmol/L)时不建议再使用ACEI和ARB,以防止高钾血症和GFR进一步下降 [18]。但是侯凡凡教授研究发现,ACEI与常规降压治疗一起,根据需要,对慢性肾功能不全高血压患者具有肾保护作用 [19]。Quach K等人证明螺内酯不会增加透析依赖患者的血清钾水平 [20]。本研究中对急性起病的恶性高血压患者,在血清肌酐达到1000 μmol/L以上依然长期持续应用RASI,达到了很好的肾脏结局。对肾素血管紧张素醛固酮系统明显活跃的双肾无缩小的急性起病患者,血清肌酐不应成为限制RASI使用的条件,而需要在仔细的滴定中用到最大量。必要时可以配合容量波动小的腹膜透析治疗一段时间。
RASI联合腹膜透析在需要透析治疗的急性起病恶性高血压患者中体现出优势,见图2。腹膜透析因机体可以通过腹腔淋巴管吸收液体,不仅有着对血流动力学影响较小的优势,还可以改善肾脏灌注,因此对肾功能起到了较好的保护作用,并通过腹膜透析排除过量的钠、水、代谢废物,降低血压。与RASI一起,使患者血压稳步得到控制。在我们的研究中6例患者最后全都顺利地脱离了腹膜透析,与血液透析相比具有优势。
我们选择短效ACEI (卡托普利)作为最重要的基础治疗方案,依据血压情况调整剂量及用法。从小剂量6.25 mgtid开始逐渐滴定增加,最大剂量用至50 mgtid,在RAAS明显激活的状态下表现出良好的治疗反应。RAAS的激活是RAAS阻断剂启动的重要标准。本研究观察到,治疗时间越长,疗效越显著。治疗达到6个月时eGFR达到比较明显的改善,3年后RASI组呈现出更加明显的肾功能改善,持久应用,获益最大。血清肌酐值在短时间内急剧升高的患者,出现透析指征,需要透析支持。我们研究发现,腹膜透析可以很好地保护肾功能,配合RASI持续治疗之后全部最终脱离透析。从恶性高血压患者肾脏受损的病理生理本质上看,腹膜透析既可以清除毒素,又不会引起肾脏灌注的剧烈波动,在以缺血致病的恶性高血压患者中肾功能恢复会比血液透析更有优势。我们在使用RASI的基础上对血压控制达标与否进行肾脏生存分析,血压控制达标的患者的预后明显优于未达标者(P < 0.0001)。
综上所述,RASI是治疗恶性高血压患者的首选用药。治疗时间越长,疗效越好,肾功能改善的程度越大。血清肌酐在短时间内急剧升高的恶性高血压患者,若符合急症启动透析的要求,建议首选腹膜透析联合RASI治疗,可保证病人的肾脏灌注及血流动力学的稳定,有助于肾功能恢复。
基金项目
国家自然科学基金(81770699);青岛市科技局成果转化计划科技惠民专项(15-9-2-90-nsh);青岛市卫生健康委员会优秀学科带头人培养计划。
NOTES
*通讯作者Email: gqx99monash@163.com