1. 引言
近些年,随着生活水平提高,人类愈发注重环境保护,其中解决水资源污染是环境保护最亟待解决的问题之一 [1]。各类水污染中工业废水污染危害大、处理难、花费高。目前,研究最多的是利用半导体TiO2作为催化剂对工业污水进行降解,将水中对环境危害较大的有机污染物氧化成危害较小或者无危害的CO2和H2O。TiO2是一种n型半导体材料,其中用于光催化氧化领域的主要是锐钛矿型(Anatase) TiO2和金红石型(Rutile) TiO2 [2],但Anatase型TiO2和Rutile型TiO2的带隙能均≥3.0 eV,且光生载流子易复合,大大降低了TiO2在太阳光下的催化活性。为解决TiO2对可见光利用率低、光生载流子复合率高的缺陷,人们尝试通过贵金属沉积、离子掺杂、半导体耦合、有机物修饰等手段对纳米TiO2催化剂进行改性 [3]。一方面减小其禁带宽度,另一方面捕获光生电子。
由于制备方式不同,TiO2材料可制备成纳米级别的粉体、管阵列、线、纤维、片等多种形貌 [4]。粉体具有较大比表面积,且较易掺杂改性,但制备成本较高,不易回收。纳米TiO2纤维常用静电纺丝法制得,操作工艺简单,产品形貌整齐,但设备要求高,难以大批量生产,实现工业化 [5]。而TiO2纳米管阵列可以通过电镀法制备,操作简单、价格低廉、实验进度可控且不会造成二次污染,有望在提高TiO2催化性能的基础上简化生产工艺,降低成本,促进TiO2半导体材料在光催化氧化领域的工业化进程。
2. 实验部分
2.1. 试剂与仪器
钛片(99.5%,上海代远金属制品有限公司),氢氟酸,六水合硫酸镍,乙二醇(AR,西陇化工股份有限公司),氟化铵(AR,西陇科学股份有限公司),冰醋酸(AR,上海展云化工有限公司),葡萄糖(AR,国药集团容生制药有限公司),氯化亚锡(AR,太仓市周氏化学品有限公司),乙二胺四乙酸二钠(AR,天津市登峰化学试剂厂),无水乙醇(AR,上海凌峰化学试剂有限公司)。
可见分光光度计(V-1200,天津宗科科技有限公司),X射线单晶衍射仪(D8ADVANCEC, Broker AXS公司),透射电镜(TEM,JEM-2100F型,日本电子株式会社)。
2.2. 实验方法
2.2.1. TiO2纳米管阵列的制备
将钛片(2 × 2.5 × 0.5 cm)用金相砂纸打磨光亮除去氧化层,浸入2% HF溶液化学除油,洗涤干燥。取一定量的NH4F、H2O溶于乙二醇,分别制备质量分数为0.5%和10%的混合溶液,配置成有机电解液。以预处理过的钛片作为为阳极,碳棒为阴极,外加电压30 V,在有机电解液中进行阳极氧化2 h。随后放入马弗炉450℃焙烧3 h,得到一次阳极氧化的TiO2纳米管。超声清洗20 min,除去一次沉积的TiO2纳米管,再次用有机电解液阳极氧化1 h,最终得到规整的二次阳极氧化制得的TiO2纳米管阵列/Ti。
2.2.2. 掺杂非金属碳元素
以0.02 g/mL的葡萄糖溶液为有机碳源,将二次阳极氧化制得的TiO2纳米管阵列与葡萄糖溶液放入高压反应釜中,160℃下反应24 h。管式炉450℃,氮气氛围保护焙烧固碳,得到TiO2-C/Ti。
2.2.3. 电镀沉积NiSn合金
称量0.2376 g NiCl2·6H2O,0.1896 g SnCl2,0.6724 g乙二胺四乙酸二钠,在水中搅拌溶解,调节pH为10左右,以铂电极为阳极,TiO2-C为阴极,外加电压2.5 V,电镀7 min,得到NiSn/TiO2-C/Ti。
2.3. 结构表征与性能测试
2.3.1. 电极的表征
采用TEM观察NiSn/TiO2-C/Ti电极表面形貌。利用XRD进行晶体结构的测定和表征,CuKα射线,λ为0.15418 nm,工作电流40 mA,工作电压40 kV。
2.3.2. 电极的光电化学性能测试
以10 mg/L的甲基橙溶液为目标降解物,55 W氙灯作光源进行光电催化降解实验,探究pH、电压、光源等对降解效果的影响。
通过紫外–可见分光光度计测定甲基橙溶液降解前后的吸光度,通过吸光度的改变计算其降解率,降解率计算公式如下:
Η——降解率,C0——溶液起始浓度,Ct——t时刻溶液溶度,A0——溶液起始吸光度,At——t时刻溶液吸光度。
3. 结果与讨论
3.1. XRD测试结果
图1为在钛片上生长出的TiO2、TiO2-C、NiSn/TiO2-C的XRD谱图。NiSn/TiO2-C催化剂在2θ为25.3˚,37.8˚,48.1˚附近的特征峰为TiO2锐钛矿型(101),(004),(200)的特征衍射峰 [6]。在2θ为53.9˚和62.8˚附近的特征峰为金红石型(211),(002)的特征衍射峰 [7],2θ为25.3˚附近的特征衍射峰更尖锐,表明电极表面TiO2中锐钛矿相与金红石相并存,而锐钛矿相的占比更多。混相结构之间会形成异质结,更利于光生载流子分离,从而提高电极的光电催化性能。

Figure 1. XRD patterns of the obtained sample (A) TiO2/Ti; (B) TiO2-C/Ti; (C) NiSn/TiO2-C/Ti
图1. 样品的XRD图(A)TiO2/Ti;(B) TiO2-C/Ti;(C) NiSn/TiO2-C/Ti
图中可以明显看出TiO2样品在掺杂完C和NiSn合金后,锐钛矿型TiO2特征衍射峰发生明显偏移,这可能是所掺离子进入到TiO2晶格中取代了部分氧原子和钛原子所致 [8]。在XRD谱图中未能明显看到非金属C和NiSn合金的特征衍射峰,可能是因为掺杂的量太少或者C和NiSn合金的结晶性不好,仪器检测不出。
3.2. TEM结果分析

Figure 2. TEM images of the NiSn/TiO2-C/Ti
图2. NiSn/TiO2-C/Ti的TEM
Ni-Sn/TiO2-C/Ti电极的TEM图如图2所示,TiO2为管状结构,有明显的开口端,排列较为规整,管内径约为80~100 nm,管壁厚约为10 nm,说明通过二次阳极氧化法可以制得规整的管状纳米TiO2。管状结构使纳米TiO2具有较大的比表面积,使得与电极接触的目标降解物增多,并提供了电子传输轨道,促进电子转移到催化剂表面,有利于光电催化降解,从而提高电极的光电降解性能 [9]。图中未能明显看到C和NiSn合金颗粒,可能是因为掺杂量较少且颗粒小。
3.3. 电极光电性能测试的结果
以10 mg/L甲基橙溶液为目标降解物,NiSn/TiO2-C/Ti为阳极,铜棒为阴极,溶液pH、外加电压、外加光源、电源等为变量,进行降解实验。
3.3.1. 溶液pH对电极光电降解性能的影响
由图3可知,pH为2与pH为3时NiSn/TiO2-C/Ti电极光电降解效果差不多,对10 mg/L甲基橙溶液催化90 min后的降解率分别为97.7%和97.4%。当pH为4时催化效果明显降低,可能是因为强酸性条件下,甲基橙呈醌式结构,比其在中性、弱酸性条件下更容易降解,并且酸性条件下,NiSn/TiO2-C/Ti电极表面带正电荷,更易吸附甲基橙进行降解 [10]。

Figure 3. Time curve of degradation rate under different pH conditions
图3. 不同pH条件下的降解率时间曲线图
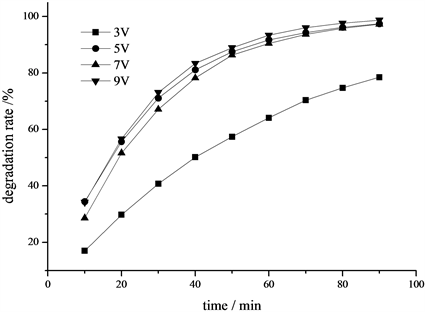
Figure 4. Time curve of degradation rate under different applied voltage
图4. 不同外加电压下的降解率时间曲线图
3.3.2. 外加电压对电极光电降解性能的影响
由图4可知,电压越大,光电降解效果越好,当外加电压分别为5 V、7 V、9 V时,NiSn/TiO2-C/Ti电极对甲基橙溶液的降解率均在97%以上。当电压降为3 V时,降解效果明显下降,仅为78.5%,可见电压是影响催化剂催化活性的一大重要因素。另外,当电压提高至9 V时,降解效果没有明显提高,因此从能耗角度出发,该实验光电降解最适合的外加电压为5 V。
3.3.3. 光、电对催化剂的影响
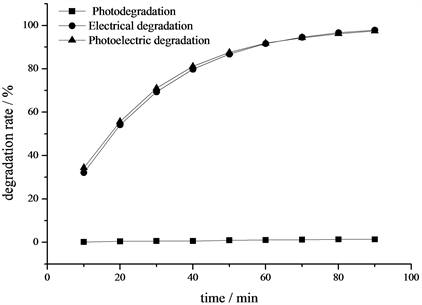
Figure 5. Time curve of photodegradation, electrolysis and photodegradation rate of NiSn/TiO2-C/Ti electrode
图5. NiSn/TiO2-C/Ti电极光解、电解、光电降解率时间曲线图
图5表明,光电催化降解效果与单纯电催化降解效果相差不大,说明该实验主要是电催化。电催化一方面加速了有机物氧化降解的过程,另一方面,由于外加偏压形成了内置电场,使电子从半导体转移到外电路,促进光生电子空穴对的分离,进而提升催化性能 [11]。单纯光解效果最差,几乎为零,猜测原因可能是钛片表面TiO2纳米管量较少,并且纳米TiO2被固定在钛片基底上,与溶液和光的接触较少。
3.3.4. 掺杂对催化剂性能的影响

Figure 6. Time curves of photodegradation rate of different electrodes
图6. 不同电极光电降解率时间曲线图
图6表明,NiSn/TiO2-C/Ti电极对甲基橙的降解效果最好,90 min后降解率达97.4%,TiO2-C/Ti效果次之,90 min后光电降解率为32.1%,远远低于NiSn/TiO2-C/Ti电极的催化效果。而单纯TiO2/Ti电极对甲基橙溶液的降解效果最差,仅为10.7%,甚至低于纯Ti光电降解的效果。这可能是因为TiO2为半导体,其导电性不如纯钛片,致使其光电降解效果最差。通过高压水热反应在TiO2管阵列中掺杂了非金属碳元素。一方面C可取代TiO2晶格中的O,使晶格发生畸变,产生更多活性位点;另一方面,通过掺杂非金属碳元素提高了半导体TiO2的导电性;二者皆能够提高TiO2的光电降解效果。在C/TiO2的基础上电镀NiSn合金,金属的掺杂在TiO2的价带和导带中引入杂质能级,缩短了TiO2的禁带宽度,提高了电极对可见光的利用率。由于金属和非金属的协同作用,大大提高了电极的光电降解效果。
3.4. 催化剂的重复使用情况
经过测试发现,NiSn/TiO2-C/Ti电极重复使用10次后,降解率保持95%以上,表明该电极的稳定性较好。
4. 结论
1) 以钛片为基底通过阳极氧化制备TiO2可以将催化剂固定在钛片基底上,解决了粉体催化剂不易回收且造成二次污染的问题,通过高压水热反应和电镀法成功在TiO2上负载了金属和非金属,获得新型电极;
2) NiSn/TiO2-C/Ti电极的制备工艺简且便易操作,光电降解时未见金属存在脱落情况,在多次使用后,电极的降解效果依旧,具有良好的光电稳定性与抗毒性,电极的光电催化活性大大提高;
3) 光电降解与单纯电降解效果相差不大,所以该催化剂即使在夜间也能高效工作;
4) NiSn/TiO2-C/Ti电极的最适降解条件为可见光照射下,外加电压5 V,溶液pH为3。