1. 引言
池塘底质中的氮、磷等因为扰动等原因释放至水体中,加重水体负荷导致富营养化 [1],生产上常采用生物法、化学法和物理法原位改良养殖池塘底质。种植小白菜、添加生石灰、暴晒均可以降低池塘底泥中营养物质的含量,且小白菜可有效降低水中TP含量,修复效果最佳 [2]。水生植物在原位改良养殖池塘环境中具有重要作用。研究发现:沉水植物矮慈姑可阻止底泥向水中释放氮磷,使水中氮磷维持在较低浓度 [3];种植莲藕可提高微生物对底质有机污染物的降解能力,能吸收底泥里一定量的TN、TP [4];投放漂浮植物或放置植物浮床可有效降低加州鲈塘底泥中TOC、TN、TP含量,以及水体中
-N和TN含量 [5] [6] [7];覆盖面积30%的菹草和螺蛳组合能大幅降低养殖池塘水中TN、TP、
-N和
-N浓度 [8];空心菜生态浮床对富营养化池塘水体的净化效果较好 [9]。湿地植物绿狐尾藻(Myriophyllum elatinoides Gaudich),环境适应力较强,具有强耐污性和耐寒性,水下部分可过冬,同时与水葫芦等外来植物相比生态竞争力不强,生物入侵能力较低,被广泛应用于人工湿地处理畜禽污水中并取得良好效果,但目前在淡水养殖池塘环境改良中的应用及其效果如何尚不清楚。
前人研究发现:罗非鱼精养池塘沉积物中有机质、总氮和总磷产污系数值高于草鱼主养池塘,其变化范围分别为11.068~17.680 kg/m2、0.084~0.151 kg/m2和0.025~ 0.053 kg/m2,高于草鱼主养池塘 [10] [11];广西罗非鱼养殖排污系数为76.69 g/kg,高于福建省的66.33 g/kg [12]。调查发现,广西罗非鱼主养区南宁市的池塘底泥中氮磷污染较为严重,可能是导致池塘水体富营养化的主因 [13]。为探究湿地植物绿狐尾藻在淡水养殖池塘环境改良中的作用,本研究以广西大学水产基地冬闲期罗非鱼养殖池塘水和底泥为材料,在室内模拟构建淡水池塘养殖环境,开展种植绿狐尾藻、抛洒改底型微生态制剂与施用生石灰三种方式对水质和底质营养物质影响的试验。通过测定、比较实验期内水体中
-N、
-N、TP、TN、CODMn等和底泥中TCs、TNs、TPs营养物质含量变化,找出改良效果较好,适宜的改底方法,为消减罗非鱼池塘养殖环境污染提供科学参考。
2. 材料与设计
2.1. 实验设计
实验于2019年1月27日至2019年4月2日在广西大学水产养殖教学基地大棚内进行。利用12个45 cm × 32 cm × 30 cm的塑料箱,每箱内铺置约4 cm经充分搅拌混匀的池塘底泥,水深约25 cm。实验用绿狐尾藻、底泥和水样采自广西大学水产教学基地罗非鱼养殖池塘,试验用水和底泥营养物质情况详见表1。实验分为4组,每组设3个平行,分组情况见表2。实验期间改底型微生态制剂和生石灰仅在起始时抛洒一次,改底型微生态制剂购自江西调水人生态环境工程有限公司,按产品说明取5 g/m2使用,每个平行洒入0.72 g;生石灰组每平行抛洒28 g [14];绿狐尾藻2~3株一起种于箱内四周底泥中,保持种植点的行距相等。采样间隔中向试验箱内添加蒸馏水补充蒸发流失的水分 [15]。

Table 1. Nutrient content of water and mud samples in simulation experiment
表1. 模拟实验供试水样和泥样的营养物质含量

Table 2. Experiment grouping and processing
表2. 试验分组及处理情况
2.2. 样品采集与分析
实验期间分别于第22 d、44 d、66 d采集水样和泥样,水样采集、运输、保存和管理参照《国家环境保护标准》(HJ493-2009)执行;用管状竹筒分别于实验箱四周采集底质沉积物样品,剔除植物、石头等杂质后,风干研磨过筛 [16];实验结束时,每箱随机选取5株绿狐尾藻,用粗滤纸吸干水分测量鲜重,用直尺测量株长 [17],随后风干研磨过筛,分装待测。水样、沉积物和植株样品测定项目和方法见表3。分别用温度计(杭新TP600)、溶氧仪(雷磁JPB-607A)和pH计(力辰科技pH-100A)于现场测定水体温度、DO和pH。
2.3. 数据处理和统计分析
实验数据用Office Excel 2018进行处理分析。用SPSS 20.0进行单因素方差分析法(One-Way ANOVA),比较各组间的差异显著性,P < 0.05表示差异水平显著;利用Office Excel 2018做图。

Table 3. Determination indexes and methods of water, mud and plant samples
表3. 水样、泥样和植株样测定指标和方法
绿狐尾藻氮、磷含量采用以下公式计算:
AN = Qd × CN × 10−2
AP = Qd × CP × 10−2
式中,AN和AP分别为单位面积内的植株氮磷含量(kg/m2);Qd为植株干质量,g/m2;CN为植株干物质中全氮含量(%);CP为植株干物质中全磷含量(%)。
3. 结果
3.1. 绿狐尾藻植株生物量及氮磷含量
至实验结束,每箱平均收获约301.5 g绿狐尾藻,增重219 g,增重率约为265.5%。实验期间绿狐尾生长状况良好,未发现植物死亡情况。
实验前后绿狐尾藻植株氮磷含量见表4。实验期间,绿狐尾藻氮移除量约为1.05 × 10−3 kg,磷移除量约为0.51 × 10−3 kg。

Table 4. Nitrogen and phosphorus contents of Myriophyllum elatinoides Gaudich
表4. 绿狐尾藻植株实验前后氮磷含量
3.2. 各组底质中总碳、总氮和总磷的含量变化
3.2.1. 各组底质中总碳含量变化
如图1所示:实验期间D、S两组和CK组底质中总碳含量均呈先升高后降低的趋势,D、S两组和CK组在实验期间均无显著性差异(P > 0.05)且它们两组间无显著性差异(P > 0.05);H组底质中的总碳含量呈先缓慢降低后升高再缓慢降低趋势,第22 d显著低于CK、D和S组(P < 0.05),第44 d和其余三组间无显著性差异(P > 0.05),实验结束时显著大于其余三组(P < 0.05)。最终H组总碳含量增加了9.91%,CK组去除率为5.60%,D组去除率为10.93%,S组去除率为2.41%。
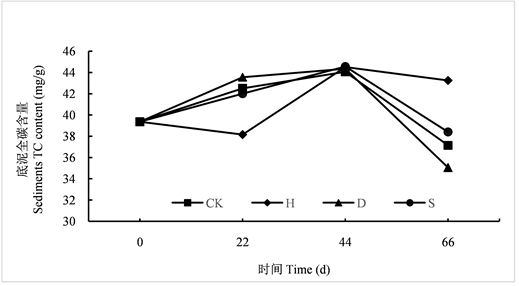
Figure 1. Changes of total carbon content in sediments of each group
图1. 各组底质总碳含量变化
3.2.2. 各组底质中总氮含量变化
如图2所示:实验期间,各组底质中总氮含量均呈先升高后降低的趋势,各组之间无显著性差异(P > 0.05),H组的总氮浓度一直低于D和S组。最终各组总氮含量均有所下降,H、D和S组的去除率分别为32.91%、27.85%和20.25%,CK组去除率为21.52%。H组对底质中总氮的净化效果最佳。
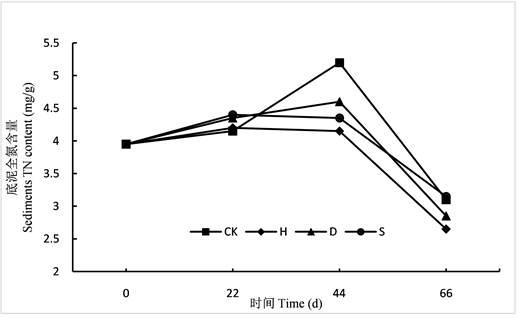
Figure 2. Changes of total nitrogen content in the sediments of each group
图2. 各组底质总氮含量变化
3.2.3. 各组底质中总磷含量变化
如图3所示:实验期间,H和D组底质中总磷含量一直呈降低趋势,CK和S组呈先降低后升高再降低趋势,H和D组含量试验期间均小于CK组,S组在约30 d后大于CK组。第22 d,四组之间均无显著性差异(P > 0.05);第44 d,H组显著小于其余三组(P < 0.05),D组显著小于CK组(P < 0.05),S组显著大于CK组(P < 0.05);第66 d,H组显著小于其余三组(P < 0.05),D组显著小于CK组(P < 0.05),S组大于CK组但无差异(P > 0.05)。最终H组底质中总磷含量去除率为28.05%,D组为17.90%,S组增加了1.23%,CK组去除率为7.08%。

Figure 3. Changes of total phosphorus content in sediment of each group
图3. 各组底质总磷含量变化
3.2.4. 小结
综上,实验期间H组底质中总氮、总磷含量降低且去除效果优于D和S组,总碳含量前期降低但后期增加;D组底质中总碳、总氮和总磷含量均有所降低,其中总氮和总磷的去除效果优于S组但劣于H组;S组底质中总碳、总氮含量降低,总磷含量上升。
3.3. 各组水质指标的变化
3.3.1. 各组水温、pH和DO变化
如表5所示:实验期间,水温范围为13.7℃~19.6℃。pH变化范围介于7.43~8.70之间,各组pH有不同程度上升,水质呈弱碱性;其中H组、D组和CK组的pH变化介于7.43至7.97之间,两两间均无显著性差异(P > 0.05);S组的pH值变化介于7.43至8.70之间,显著大于CK组(P < 0.05)。各组DO在1.0 mg/L~9.6 mg/L之间波动,先上升后下降,其中前44 d,DO均高于3.0 mg/L,第44 d四组都达到最大值;66 d时DO下降至3.7 mg/L以下,S组和H组的DO均高于3.0 mg/L,但D组和CK组低于2.0 mg/L。


Table 5. Changes of water temperature, pH and DO in each group
表5. 各组水温、pH和DO的变化
3.3.2. 各组水质
-N浓度变化
如图4所示:实验期间CK、H和D组水体中
-N浓度均呈先降低后升高趋势,S组呈先升高后降低趋势。试验过程中H和D组的
-N浓度一直低于CK组且H组低于D组,三组之间无显著性差异(P > 0.05);S组约60 d前显著大于其余三组(P < 0.05),第66 d和其余三组之间无显著性差异(P > 0.05)。
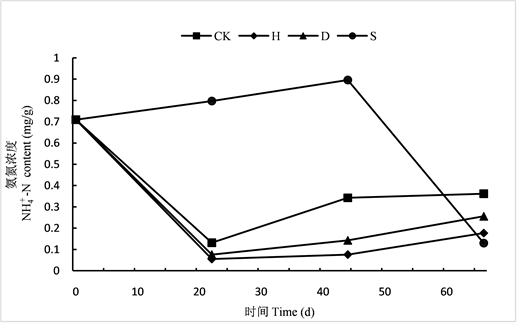
Figure 4. Changes of
-N content in water of each group
图4. 各组水质
-N含量变化
3.3.3. 各组水质
-N浓度变化
如图5所示:实验期间CK组水中的
-N浓度呈先大幅上升后大幅下降的趋势,H组呈缓慢上升趋势,D组呈先上升后缓慢下降趋势,S组呈先下降后大幅上升趋势。22 d前,H、D和S组均显著低于CK组(P < 0.05),三组间无显著差异(P > 0.05);第44 d,H组与D组都和CK组无显著差异(P > 0.05),S组显著高于CK组(P < 0.05);66 d后,S组显著大于其余三组(P < 0.05)。试验期间,H组的
-N浓度要小于D和S组,变化最为平稳,S组使水中
-N含量增加。
3.3.4. 各组水质TP浓度变化
如图6所示:实验期间CK、H和D组水中的TP浓度呈先降低后缓慢升高的趋势,S组水中的TP浓度呈先缓慢降低后大幅升高趋势。H、D两组变化趋势相似,总体上略低于CK组但两两间无显著差异且与CK组无显著差异(P > 0.05),S组试验间显著高于CK组(P < 0.05)。H和D组对水中TP影响不大,S组使水中TP浓度增加。

Figure 5. Changes of
-N content in water of each group
图5. 各组水质
-N浓度变化
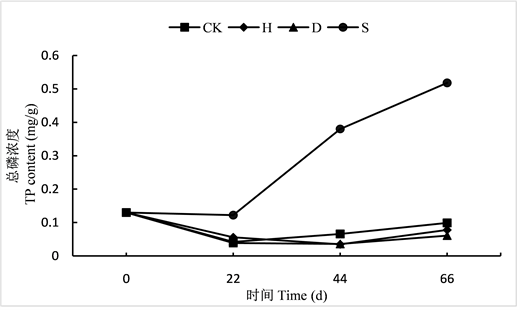
Figure 6. Changes of TP content in water of each group
图6. 各组水质TP含量变化
3.3.5. 各组水质TN浓度变化
图7所示:实验期间CK和D组水中的TN浓度呈先升高后降低又升高的趋势,H组呈先持续降低后升高趋势,S组呈先升高后降低趋势。试验22 d前,H组的TN浓度显著小于其余三组(P < 0.05),第44 d时,S组显著大于其余三组(P < 0.05),实验结束时CK与S组显著大于H与D组。实验期间,H组浓度整体小于其余各组,D组浓度变化介于H和S组之间。
3.3.6. 各组水质CODMn浓度变化
如图8所示:实验期间各组水中的CODMn浓度均呈先降低后升高的趋势,H组在试验中期前小于其余三组,在约60 d前小于CK组,D组试验期间一直小于CK组,S组在43 d后一直小于其余三组。试验期间,三个处理组的CODMn浓度均无显著性差异(P > 0.05),且与CK组也无较大差异(P > 0.05)。
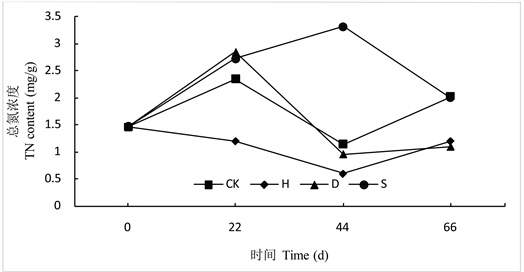
Figure 7. Changes of TN content in water of each group
图7. 各组水质TN含量变化
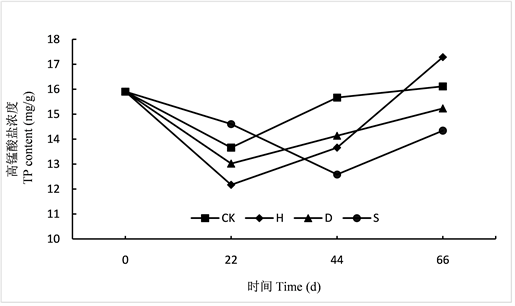
Figure 8. Changes of CODMn content in water of each group
图8. 各组水质CODMn含量变化
3.3.7. 小结
综上,实验期间H组的
-N、
-N和TN浓度整体小于其它实验组,TP和CODMn的变化不明显,H组水中的营养物质变化相对平稳,对水质影响最小;S组前中期的
-N和TN浓度显著大于其它组,S组使水中
-N和TP浓度上升,对水质影响最差;D组的营养物质浓度整体介于H组与S组之间。
4. 讨论
4.1. 不同底质改良方式对池塘底质营养物质的影响
池塘底质为化学物质储存地、多种生物栖息地和营养盐循环中心 [18],池塘环境变化时,底泥中的营养盐会经各种扰动释放造成污染。实验期间,种植绿狐尾藻后,H组底质中TN和TP含量均为最低,TP显著低于CK组(P < 0.05);植物的吸收为重要的除磷途径 [19],绿狐尾藻种植后可以改变底质吸附磷的能力,减少底泥中颗粒形态磷的悬浮 [20],绿狐尾藻在生长过程中也会改变磷的形态 [21],这些都促进了底泥中磷的去除。同时,绿狐尾藻生长过程中还可以改变底泥中脱氮微生物的群落结构,使此类微生物间的互作能力加强,达到较好的除氮效果 [22]。实验后期H组底质中TCs含量显著高于CK组,这与小白菜修复养殖池塘底质营养物的结果相似 [2],或是因为根系的生长致分泌物逐渐增加,使底泥中有机碳含量增加。抛洒微生态制剂后,D组的TN和TP实验期间持续低于CK组,可能是富含的菌群和分解因子提高了底泥微生物群落的代谢能力,对底质中的TN、TP有一定去除能力,但TC含量与CK组无显著差异。抛洒生石灰后,S组底泥中TP在实验期间高于CK组,可能与其遇水生成碳酸钙改变了底泥底泥pH值和通气条件,加速了有机质分解有关 [23]。生石灰会杀灭水中一些细菌和水生生物,导致微生物活性变弱,水生生物死亡后也会释放出体内的氮磷 [24] [25],这可能是S组去除底质营养物质能力较差的原因。
4.2. 不同底质改良方式对水体营养物质的影响
实验期间,绿狐尾藻组(H组)水体的
-N、
-N和TN浓度整体小于其它实验组;生石灰组(S组)的
-N和TP浓度都有显著增加,
-N和TN浓度在前中期都要高于其它实验组;微生态制剂组(D组)的营养盐浓度整体介于H组与S组之间,各组的CODMn浓度变化趋势一致,H组水中营养盐物质几乎无增加,原因可能是绿狐尾藻通过根系、茎叶吸收水中的营养物质,其复杂的根系也会调节水体微环境,利于微生物的硝化和反硝化作用,有效减少营养物的浓度 [26]。实验中H组对底质营养物也有较好的去除效果,绿狐尾藻综合修复效果最佳。D组中的底改型微生态制剂中含有专门的修复用特殊菌群,可提高水体细菌优势群落多样性,在微生物转化底泥营养物的同时,也能改善水体环境 [27]。S组对水质营养物质影响最大,生石灰改善底泥pH值和通气条件后,底泥持续释放出N、P元素,造成水中营养盐浓度增加。生石灰还可杀灭水体的有益菌如硝化细菌,使水体的硝化作用受到抑制 [24],影响氨氮的去除,同时被杀灭的水生生物经分解矿化后 [25],释放的营养盐也会对水体造成影响。
本实验中,绿狐尾藻对养殖池塘底泥中的氮磷有很好的去除效果,水质的影响最小。可在养殖池塘闲置期种植绿狐尾藻来改良池塘环境。
基金项目
国家现代农业产业技术体系广西创新团队建设项目(nycytxgxcxtd-08-03);广西科技创新驱动专项(桂科AA17204095-2)。