1. 引言
氢气与氧气在金属铂的催化下化合成水是从1840年 [1] 被发现开始研究至今的一种反应,由于反应物、产物及催化剂结构简单、性状普适,并且催化效果明显,该反应一直作为多相催化中的一个典型的模型氧化反应被学者们研究进而开发应用。 [2] [3] [4] 因为氢氧化合成水能够释放大量的热量,而催化剂的加入令反应容易发生,所以在催化燃烧及燃料电池等能源领域一直备受关注。同时,在产氢场景中,对氢气的消除也利用该反应的彻底性进行气相消氢,从而避免爆炸等危险的发生。当学界的焦点都在探索怎样利用该反应的高效性与彻底性时,在重水提氚领域,学者们正在研究氢氧复合怎样避免热量的聚集,令反应平稳、大量地进行,从而满足同位素分离过程中级联对大量氢氧复合反应的需求。
如图1所示,由于氢氧复合成水会放出大量的热,且反应速率会随着温度的升高而增大,在大量的氢氧复合反应中反应速率存在增大的风险,多放出的热量很可能会积累,导致反应器内温度升高,进一步增大反应速率,形成促进循环直至达到临界点燃状态 [5],发生燃烧甚至爆炸的安全事故,自身能使催化反应平稳发生的催化剂在重水提氚中意义重大。最早的疏水性催化剂概念由CRNL于1969年提出 [6],最初的研究用于氢同位素的分离,在七十年代中后期,逐步把疏水催化剂的研究成果用于氢氧复合,并于二十世纪八十年代开始发展成熟,广泛应用于国防科技与国民经济。 [7] [8] 在落后国外二十年的情况下,我国的氢氧复合研究经过迅速发展已能赶上世界前列,但由于催化剂制备技术的垄断,某些领域我国仍需用远高于成本的价格购买国外的催化剂。因此,自主研制出性能良好、符合操作环境要求的催化剂是打破国际垄断的关键因素。

Figure 1. Schematic diagram of hydrogen-oxygen recombined heat accumulation cycle
图1. 氢氧复合热量积累循环示意图
加拿大的ACEL公司已将自主研发的铂疏水催化剂应用到CECE流程中的氢氧复合中去,并达到工业示范规模。国际上主要运用涂覆型疏水催化剂 [9] [10],我国进行了程度颇深的反应器设计及工艺研究 [11],但疏水催化剂仍然需要高价采购俄罗斯门捷列夫化工大学研制的Pt-SDB [12]。
由于处于焦点盲区,用于常温氢氧复合的疏水催化剂Pt-SDB的国产化研究推进缓慢,只有中国原子能科学研究院在“从无到有”的阶段有所尝试。邵明昶 [13] 在逆流及反应气预混的实验条件下,对直接水冷式氢氧复合进行了等温活塞流的理想化处理,并根据文献 [14] 在氧气大大过量的情况下反应对氢气是一级的,求出实验体系中氢氧在水环境中疏水催化复合的表观活化能。本文作者 [15] 通过正交实验,确立了影响Pt-SDB催化性能的主要制备条件,本文以此为基础,采用浸渍法制备Pt-SDB,研究还原温度、浸渍静置时间与还原时间对催化剂性能的影响。
2. 主要实验原料、仪器及分析方法
2.1. 主要实验原料
氯铂酸,分析纯,国药集团化学试剂有限公司。
无水乙醇,分析纯,国药集团化学试剂有限公司。
聚苯乙烯二乙烯基苯(XSDB、NSDB),购买自南开大学化工厂,是一种球状、非极性大孔吸附树脂,该树脂是交联聚合物,具有较大的比表面积和适宜的孔径,并且能够大量生产。
本文所涉及的所有气体均产自北京华通精科气体化工有限公司。
2.2. 主要仪器
超声波清洗器,型号KQ-50E,产自昆山市超声仪器有限公司。
电热真空干燥箱,型号ZK-3 BS,产自天津市中环实验电炉有限公司。
开启式真空/气氛管式电炉,型号SK-G12123K-5-900,产自天津市中环实验电炉有限公司。
2.3. 主要分析方法
激光粒度分析(Laser Particle Size Analysis)是根据颗粒能使激光产生散射这一物理现象测试粒度分布的,当光束遇到颗粒阻挡时,一部分光将发生散射现象,散射角θ与颗粒的大小有关,某一角度的散射光强度代表该粒径颗粒的数量,从而得到粒度分布。本课题中使用日本HORIBA公司生产的LA-950型激光粒度分析仪对XSDB和NSDB载体进行干法粒度分析。
BET测试理论是根据三名科学家(Brunauer、Emmett和Teller)提出的多分子层吸附模型,并推导出单层吸附量Vm与多层吸附量V间的关系方程,即著名的BET方程。BET方程是建立在多层吸附的理论基础之上,与物质实际吸附过程更接近,因此测试结果更准确。本课题中使用美国康塔仪器公司生产的NOVA 4200e型全自动比表面积及孔径分布分析仪对两种载体进行孔分布的分析。
热重分析(Thermogravimetric Analysis, TG)是指在程序控制温度下测量待测样品的质量与温度变化关系的一种热分析技术,用来研究材料的热稳定性和组份。差示扫描量热法(Differential Scanning Calorimetry, DSC)与差热分析基本相同,但是定量更加准确、可靠。试样和参比物各自独立加热,随时保持两者的温度相同。如果样品发生相变或失重,它与参比物间将产生温度差时,系统提供功率补偿使两者再度保持平衡,而所要补偿的功率则相当于样品热量的变化。本课题采用德国耐驰公司的STA 449F3型差示扫描量热计,测试条件为:氮气流量60 mL/min,升温速率10℃/min。
3. SDB比较与选型
目前能够大量工业制备的小粒径SDB载体有两种型号——XSDB和NSDB载体,二者的物理性质为购买时随附的基本说明,更具体的结构细节需要通过粒度分析、孔分布测试、热重及差示量热扫描分析进行深入了解。
3.1. 载体的粒度比较分析
如图2所示为预处理后的两种SDB载体的粒度分析图组,可以看到XSDB载体的粒径整体大于NSDB载体。具体分析数据见表1,XSDB的粒径大约比NSDB大0.2 mm。
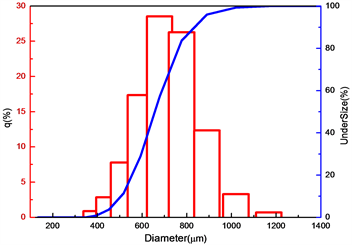 (a) XSDB的粒径分布图
(a) XSDB的粒径分布图  (b) NSDB的粒径分布图
(b) NSDB的粒径分布图
Figure 2. Comparison of the particle size distribution of the two carriers
图2. 两种载体的粒径分布比较图

Table 1. Comparison of particle size information of two carriers
表1. 两种载体的粒径信息比较表
3.2. 载体的孔分布比较
如图3所示为两种SDB载体的吸附等温线,与国际理论和应用化学联合会(International Union of Pure and Applied Chemistry, IUPAC)分类的6种吸附等温线对比,发现两种曲线均为IV型等温线,说明两种载体上的孔属于介孔(2~50 nm),且吸附质氮气与载体表面的作用力较强。
中间段出现吸附回滞环,其对应的是SDB载体中出现毛细凝聚的体系。在中等的相对压力,XSDB的等温线上升得较NSDB快,说明XSDB的毛细凝聚比NSDB较多。
XSDB和NSDB载体的回滞环上均有饱和吸附平台,反映孔径分布较均匀。根据与IUPAC分类的4种回滞环对比,发现XSDB载体的回滞环基本属于于H1型,而NSDB载体的回滞环是H1型稍倾向于H2型。H1型反映的是两端开口的管径分布均匀的圆筒状孔,H1型迟滞回线可在孔径分布相对较窄的介孔材料,和尺寸较均匀的球形颗粒聚集体中观察到。而H2型反映的孔结构复杂,可能包括典型的“墨水瓶”孔、孔径分布不均的管形孔和密堆积球形颗粒间隙孔等。其中孔径分布和孔形状可能不好确定,孔径分布比H1型回线更宽。
XSDB载体的回滞环起点在P/P0 = 0.4~0.6之间,说明一定是介孔;NSDB载体的回滞环不闭合,说明有微孔的存在。
 (a) XSDB的吸附等温线
(a) XSDB的吸附等温线 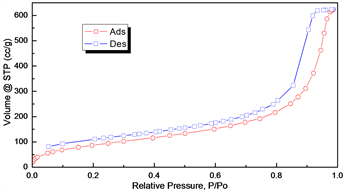 (b) NSDB的吸附等温线
(b) NSDB的吸附等温线
Figure 3. Comparison of adsorption isotherms of two carriers
图3. 两种载体的吸附等温线比较图
如图4所示为两种载体采用BJH法计算得出的吸、脱附支曲线。BJH法是一种根据毛细凝聚现象,也就是Kelvin方程,计算介孔分布的方法,以此还可以衍生出表面积、孔容等信息。由于两种载体的回滞环均类似于H1型且吸脱附支曲线明显不一致,所以采用脱附计算结果。由两张BJH法脱附支曲线比较发现,XSDB载体上的孔比NSDB载体尺寸较大且多,二者具体数据比较见表2。
 (a) XSDB的吸附支孔分布计算曲线
(a) XSDB的吸附支孔分布计算曲线 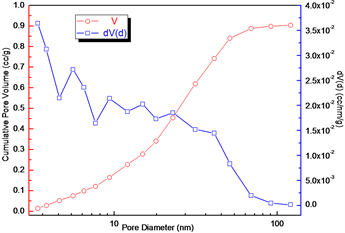 (b) NSDB的吸附支孔分布计算曲线
(b) NSDB的吸附支孔分布计算曲线  (c) XSDB的脱附支孔分布计算曲线
(c) XSDB的脱附支孔分布计算曲线  (d) NSDB的脱附支孔分布计算曲线
(d) NSDB的脱附支孔分布计算曲线
Figure 4. Comparison of the calculation curves of the adsorption and desorption branch pore distribution of two carriers
图4. 两种载体的吸脱附支孔分布计算曲线比较图

Table 2. Comparison of pore structure information of the two carriers
表2. 两种载体的孔结构信息比较表
3.3. 载体的热重及差示量热扫描比较分析
如图5与图6所示分别为XSDB与NSDB载体的热重及差示量热扫描曲线。XSDB载体的热重曲线

Figure 5. TG and DSC curves of XSDB
图5. XSDB的TG及DSC曲线图

Figure 6. TG and DSC curves of NSDB
图6. NSDB的TG及DSC曲线图
下降较均匀且不明显;NSDB载体的热重曲线呈S型下降,表明NSDB载体在测量温度范围内有较明显的结构变化。两种载体的差示扫描量热曲线更具体地呈现了二者的热稳定性,图中均存在代表吸热的峰,表明二者在测量温度范围内有不同程度的吸热熔融,从而导致结构变化:XSDB载体在180℃左右开始发生轻微的结构变化,到220℃左右变化达到最快;NSDB载体在210℃左右开始发生较明显的结构变化,到260℃左右变化达到最快。
3.4. 载体的综合比较分析与选择
通过之前对两种SDB载体的各种比较分析总结如表3所示,本文中所用的分析方法均显示出XSDB载体具有较好散热性,最终选用X型SDB载体进行随后的催化性能测定。

Table 3. Comparison of the analysis results of the two carriers
表3. 两种载体的分析结果比较表
4. 催化剂制备方法与性能测试方法
4.1. 催化剂制备方法
如图7所示为Pt-SDB催化剂制备流程。
1) 用无水乙醇将SDB树脂载体淋洗至流出液澄清,然后放置于110℃空气中干燥6 h,脱除上面吸附的有机溶剂等杂质,冷却至室温备用;
2) 采用氯铂酸的无水乙醇溶液作为前驱体,按照铂的质量分数为0.8%配制一定浓度的溶液,在超声仪中浸渍搅拌5分钟;

Figure 7. Schematic diagram of Pt-SDB preparation process
图7. Pt-SDB制备流程示意图
3) 静置若干天后,在一定温度下干燥一定时间;
4) 在氢气氛围中一定温度一定时间还原制得疏水催化剂Pt-SDB。
以表4中的实验条件为基础对影响催化剂性能较大的因素——还原时间、浸渍静置时间、还原时间——做控制变量的研究。

Table 4. Conditional settings of the basic experiment
表4. 基础实验条件设置表
分别设计三个因素的水平范围见表5,得到的催化剂样品Pt-SDB采用第二章的催化测试方法并进行TEM表征。

Table 5. Conditional design of controlled variable experiment
表5. 控制变量实验条件设计表
4.2. 催化剂性能测试方法
催化剂只能加快反应速率,不能改变最终平衡状态,即最终成分组成。但是若测试中反应气体通过催化剂的时间一定且很短,反应气在接触催化剂的时间内远不能达到平衡。这种情况下,某个时间点的转化率能够代表附近时段的反应速率的大小。若直接将装载催化剂的反应器暴露于室温空气中同时空速较小(约300 h−1),所有制得的样品催化氢氧复合反应的转化率均在1 h时间内迅速升高至趋近于100%,并且反应器温度在30 min内得到大幅提高,无法找到有效的衡量标准。所以需要测试装置在一定换热条件下,使反应器温度能够在一定温度附近小范围内变化,使转化率存在平台期,才能较直观地比较催化剂样品的催化活性及散热情况。
图8为针对Pt-SDB催化性能的测试装置示意图,本文沿用文献 [15] 中的测试方法,压缩过的原料混合气(1%氢气 + 5%氧气 + 94%氩气)经稳压器减压以1.0标升每分钟的气速30℃预热后由反应器(6 mm * 21 mm)底部进入。反应在30℃恒温条件下进行,间接换热。气体反应后从反应器顶部流出,经硅胶干燥水分进入分析系统,用气相色谱测定反应尾气中氢气的剩余浓度,然后放空。
该测试采用的主要仪器有:产自北京七星华创电子股份有限公司的气体质量流量控制器(型号CS200),产自南京先欧仪器制造有限公司的超高精度恒温水油槽(型号XOGH-20),和产自北京东西电子研究所的气相色谱仪(型号GC4000A)。其中气相色谱仪中色谱柱长10 m,内装5A分子筛;分析条件:柱箱温度60℃,热导池检测器温度100℃,载气为高纯氩气,流量用皂膜流量计测定为35 mL/min。
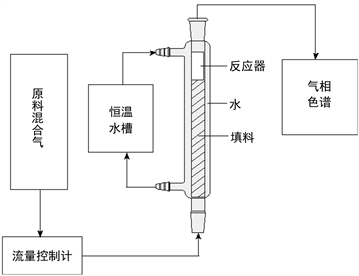
Figure 8. Schematic diagram of catalytic performance test device
图8. 催化性能测试装置示意图
5. 结果与讨论
5.1. 还原温度对Pt-SDB催化性能的影响
在其他制备条件一致的情况下,不同还原温度(Reduction-temperature, R)制得的样品Pt-SDB的催化测试结果见表6。

Table 6. Catalytic test data of samples at different reduction temperatures
表6. 不同还原温度样品的催化测试数据
如图9所示为不同还原温度制得样品的催化测试曲线及转化率和标准偏差随还原温度的变化曲线,样品R-190的催化活性最高,与正交实验结果相符。虽然样品R-190、R-200催化氢氧复合反应的稳定性也很好,但其转化率曲线没有下降阶段。
 (a) 催化测试曲线比较图
(a) 催化测试曲线比较图  (b) 转化率及标准偏差的变化曲线
(b) 转化率及标准偏差的变化曲线
Figure 9. Catalytic test results of samples at different reduction temperatures
图9. 不同还原温度样品的催化测试结果图
挑取样品R-160、R-190进行TEM表征比较。
如图10所示,样品R-190上的大尺寸Pt粒子明显比R-160更多,而且R-190上也有很多小尺寸Pt粒子,推测样品R-190的深孔内生长了Pt粒子。在实验范围内,还原温度越高,浅层Pt粒子生长越大。同时,在继续升高还原温度过程中会发生熔融包埋Pt粒子,从而导致催化效率以及稳定性的下降。
 (a) 样品R-160不同倍数的TEM图
(a) 样品R-160不同倍数的TEM图  (b) 样品R-190不同倍数的TEM图
(b) 样品R-190不同倍数的TEM图
Figure 10. TEM images of samples at different reduction temperatures
图10. 不同还原温度样品的TEM图
5.2. 浸渍静置时间对Pt-SDB催化性能的影响
在其他制备条件一致的情况下,不同浸渍静置时间(Standing-time, S)制得的样品Pt-SDB的催化测试结果见表7。

Table 7. Catalytic test data of samples with different standing time
表7. 不同浸渍静置时间样品的催化测试数据
如图11所示为不同浸渍静置时间制得样品的催化测试曲线及转化率和标准偏差随浸渍静置时间的变化曲线,样品S-1的催化测试曲线及结果明显有别于其余4个样品。可能由于浸渍静置1天时间太短,载体表面还有较多乙醇,110℃干燥时溶剂由孔内携带溶质向外蒸发,导致最终制得的催化剂Pt粒子的分布集中在浅层。而浸渍静置2天及更长时间载体表面的乙醇基本缓慢蒸发完,Pt粒子的分布没有太大改变。
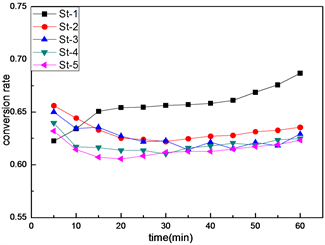 (a) 催化测试曲线比较图
(a) 催化测试曲线比较图 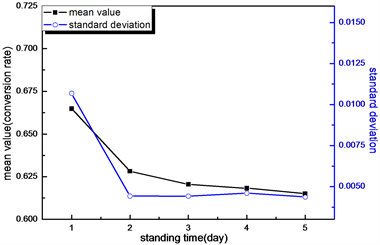 (b) 转化率及标准偏差的变化曲线
(b) 转化率及标准偏差的变化曲线
Figure 11. Catalytic test results of samples with different standing time
图11. 不同浸渍静置时间样品的催化测试结果图
挑取样品S-2、S-1进行TEM表征比较。
如图12所示,由于还原条件一致,样品S-1与S-2的浅层Pt粒子(尺寸相对较大)大小相近,但样品S-1的更多,说明样品S-1的深孔Pt迁移到了浅层。
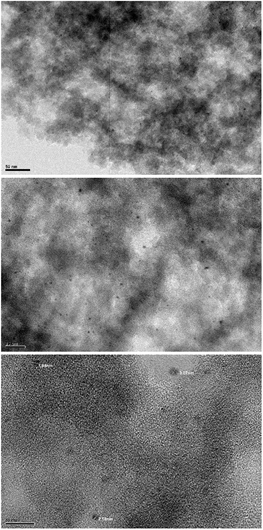 (a) 样品St-2不同倍数的TEM图
(a) 样品St-2不同倍数的TEM图  (b) 样品St-1不同倍数的TEM图
(b) 样品St-1不同倍数的TEM图
Figure 12. TEM images of samples with different standing time
图12. 不同浸渍静置时间样品的TEM图
5.3. 还原时间对Pt-SDB催化性能的影响
在其他制备条件一致的情况下,不同还原温度(Reduction-time, T)制得的样品Pt-SDB的催化测试结果见表8。


Table 8. Catalytic test data of samples with different reduction times
表8. 不同还原时间样品的催化测试数据
如图13所示为不同还原时间制得样品的催化测试曲线及转化率和标准偏差随还原时间的变化曲线,发现各样品催化测试曲线走势相近,随着还原时间的加长,样品催化氢氧复合反应的转化率和稳定性趋于良好。推测在实验范围内,还原时间越长,催化剂上浅层Pt粒子生长越大,但时间太久可能造成Pt粒子热迁移,导致其催化氢氧复合反应的稳定性下降。
 (a) 催化测试曲线比较图
(a) 催化测试曲线比较图 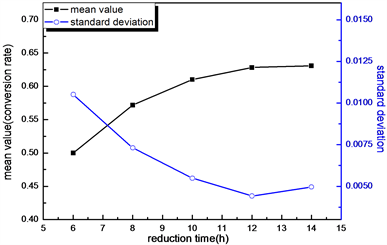 (b) 转化率及标准偏差的变化曲线
(b) 转化率及标准偏差的变化曲线
Figure 13. Catalytic test results of samples with different reduction times
图13. 不同还原时间样品的催化测试结果图
挑取样品T-12、T-6进行TEM表征比较。
如图14所示,样品T-12中的浅层Pt粒子(尺寸相对较大)比样品T-6中的浅层Pt粒子更大,进一步证明了之前“还原时间长,浅层Pt粒子生长越大”的推测。

 (a) 样品Rt-12不同倍数的TEM图
(a) 样品Rt-12不同倍数的TEM图 
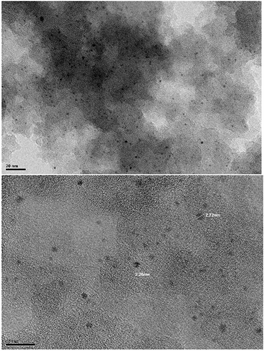 (b) 样品Rt-14不同倍数的TEM图
(b) 样品Rt-14不同倍数的TEM图
Figure 14. TEM images of samples with different reduction times
图14. 不同还原时间样品的TEM图
6. 结论
本文通过对两种SDB载体(N型与X型)的孔分布及热稳定性等分析,确定了X型更适合作为氢氧复合催化剂的载体使用,为后续工作缩小了研究范围。
同时,采用控制变量的方法,在Pt-SDB制备条件的基础上对影响氢氧复合疏水催化剂催化性能较大的三个制备条件——还原温度、浸渍静置时间、还原时间——分别进行单独研究。催化测试结果与TEM表征图比较在合理的推测下相互说明,得到一些结论:
1) 随着还原温度的提高,催化剂Pt-XSDB的浅层Pt粒子生长越大,但达到180℃以上时,载体会熔融包埋一部分深孔Pt粒子导致Pt的利用率下降;
2) 浸渍静置1天时间较短,干燥时浸渍液溶质被溶剂携带至载体浅层,导致其催化反应稳定性不佳,而浸渍静置2天后Pt在载体表面得到均匀分布;
3) 还原时间越长,催化剂上浅层Pt粒子生长越大,但时间太久可能造成Pt粒子热迁移,导致其催化氢氧复合反应的稳定性下降。
参考文献