1. 引言
气肿性肾盂肾炎(emphysematous pyelonephritis, EPN)是泌尿外科一种少见的特殊感染性疾病。它是指细菌入侵导致肾实质及其周围组织严重坏死性感染,细菌产生的气体使局部压力升高,大量细菌和毒素进入循环系统,极易发展为全身性脓毒血症,导致意识障碍和休克。现就山东中医药大学附属医院泌尿外科2018年收治的2例典型病例进行报道。
2. 临床资料
病例1:患者男性,62岁,因“阵发性恶心、呕吐,伴尿量减少4日余。”于2018年10月11日来我院急诊就诊。患者糖尿病病史10年余,血糖最高 > 20 mmol/L,平素口服格列美脲片、二甲双胍肠溶片控制血糖,未规律服药,未规律监测血糖。查体:右肾区叩痛重,腹部未见明显异常。辅助检查:测血糖 > 30 mmol/L。血常规白细胞19.42 × 109/L,中性粒细胞百分比95.6%,血小板计数1 × 109/L,CRP > 200 mg/l。降钙素原:48.97 ng/ml。动脉血气分析pH:7.28,Lac:1.8 mmol/L,
:9.5 mmol/L,BE:−15.18 mmol/L。血培养示:大肠埃希菌生长。CT检查提示:符合右肾急性气肿性肾盂肾炎并肾周感染(图1)。诊断:1) 右肾急性气肿性肾盂肾炎;2) 脓毒血症;3) 2型糖尿病;4) 糖尿病酮症酸中毒;入院后于局麻下行超声引导下右肾穿刺引流术。抽出少量陈旧性血性积液,并见气泡排出,味腥臭。但引流管内引流液体仍较少。复查CT示:符合右肾急性气肿性肾盂肾炎并肾周感染,较前变化不明显(图2)。考虑右肾基本无功能,最终经科室讨论后于全身麻醉下行3D腹腔镜下右肾切除术。术后病理见右肾已无肾盂肾盏结构,肾小球肾小管变性坏死,肾内被大量坏死组织及脓液填充(图3)。
患者经手术治疗后,后续予抗感染、控制血糖、补液支持治疗,患者一般情况逐渐好转。综合评价,一般情况恢复良好,感染得以控制,各生命体征均正常,复查CT术区无明显感染(图4),血常规、生化功能、电解质等基本正常,予以出院。随访6个月复诊患者恢复良好,未出现发热,无腰部疼痛不适症状,理化检查均在正常范围内。
病例2:患者女性,48岁,因“头晕、呕吐伴发热7天”于2018年12月15入住我院泌尿外科。院外未控制监测血糖,未服药物。查体:左侧肾区叩痛,余无明显异常。辅助检查:测血糖 > 20 mmol/L,血常规白细胞10.01 × 109/L,中性粒细胞百分比71.1%,血小板计数156 × 109/L,CRP61.9 mg/l。血培养示:大肠埃希菌生长。肝功、肾功、电解质、血气分析、尿常规等无明显异常。行腹部CT示:符合左肾气肿性肾盂肾炎(图5)。诊断:1) 左肾气肿性肾盂肾炎;2) 2型糖尿病。治疗上予以积极抗感染、控制血糖及对症支持治疗,治疗14天后停用抗生素,复查CT左肾积气较前明显好转,予以出院。1月后复查CT示左肾气肿已消失(图6)。随访6月未复发。

Figure 1. CT scan showed that the volume of right kidney increased significantly, the boundary between cortex and medulla disappeared, and no obvious renal parenchyma structure was found
图1. 患者入院CT示右肾体积明显增大,皮髓质分界消失,未见明显肾实质结构
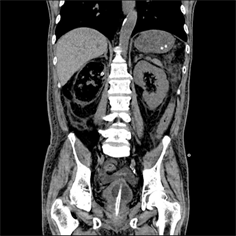
Figure 2. After right renal percutaneous drainage, there was no obvious decrease of gas in kidney
图2. 右肾穿刺引流术后,肾内气体未见明显减少
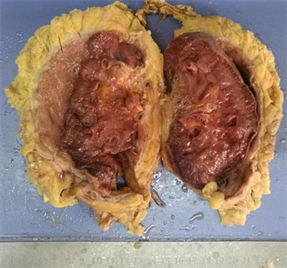
Figure 3. Postoperative pathological specimen
图3. 术后病理标本

Figure 4. CT scan after operation showed that the right renal fossa was filled with intestinal tube without obvious infection
图4. 术后CT复查示右肾窝被肠管填充,无明显感染

Figure 5. CT scan of the patient showed that the volume of left kidney was increased, and about 1.5 *1 cm emphysema could be seen on the upper and medial side of kidney
图5. 患者入院CT示左肾体积增大,肾上级偏内侧可见约1.5 *1 cm气肿

Figure 6. The upper emphysema of left kidney disappeared completely after one month treatment
图6. 治疗1月后复查左肾上级气肿完全消失
3. 讨论
3.1. 病因及发病机制
Kelly和MacCullum [1] 于1898年报告了第一例肾脏感染合并积气的病例,但直到1962年才由Schultz和Klorfein [2] 提出EPN的概念。EPN是一种累及肾实质及肾周的产气性急性坏死性感染疾病,20世纪70年代之前其死亡率高达78%,随着近20年来医疗技术的发展,其死亡率已降至21% [3]。
该疾病好发于女性,男女比例约为1:6,糖尿病是其发病最大诱因,约有95%病人有血糖控制不佳病史 [4]。在糖尿病患者中,组织内高葡萄糖与肾脏血供不足相关,进而促进了无氧酵解的过程。革兰阴性厌氧菌,如大肠杆菌,通过葡萄糖和乳酸的发酵产生大量的二氧化碳和氢气,积聚在炎症部位。Huang和Tseng对组织释放的气体进行分析,发现二氧化碳和氢气是其主要成分。同时还存在少量氨、甲烷和一氧化碳 [8]。EPN导致的死亡主要是由败血症及其并发症引起的。高达95%的EPN患者有既往有糖尿病史且血糖控制不佳。泌尿系统梗阻产生EPN的风险约为25%~40% [3]。本组2例患者既往血糖均控制不佳,入院时测血糖 > 20 mmol/L。此外,药物滥用、神经源性膀胱、酗酒、和解剖异常也是其致病因素,由泌尿系梗阻导致的EPN约占25%~40% [3]。本组2例患者血培养均为大肠埃希菌。大肠埃希菌是气肿性肾盂肾炎最常见的致病菌,在报道的病例中有70%的患者血、尿培养分离出此细菌 [5]。其他报道的致病菌还有肺炎克雷伯菌、奇异变形杆菌、D族溶血性链球菌和凝固酶阴性葡萄球菌等 [5] [6]。细菌产生的气体向内扩散至肾盂、输尿管或膀胱内,形成气肿性肾盂炎、输尿管炎、膀胱炎;向外扩散可至肾被膜下、肾周间隙和肾旁间隙,并可延伸至对侧腹膜后间隙,甚至沿腰大肌进入阴囊和精索 [7]。
3.2. EPN的分类
Huang和Tseng [8] 基于CT结果将EPN分为4级:1级,气体仅局限于集合系统;2级,气体局限于肾实质,而未延伸至肾周间隙;3A级,气体或脓肿累及肾周间隙;3B级,气体或脓肿累及肾旁间隙;4级,双肾气肿性肾盂肾炎或孤立肾气肿性肾盂肾炎。
3.3. 预后因素
虽然糖尿病是EPN的最常见致病因素,但它并不增加疾病的死亡风险 [9]。收缩压低于90 mmHg,意识障碍以及血清肌酐水平升高预示着较高的死亡风险。血小板减少和双侧EPN与不良的预后有关。与单纯应用抗生素相比,及早进行肾穿刺引流术或肾切除术能降低死亡率 [9]。
3.4. 临床表现
EPN早期无特异性临床表现,潜伏期数日至数月不等。早期临床症状类似于肾盂肾炎,包括食欲下降、寒战、发热、恶心、呕吐和腰痛等 [7] [10]。潜在临床表现为急性肾功能不全、酸碱平衡紊乱、高血糖、血小板减少和意识不清。严重EPN患者可能会出现感染性休克。肋脊角叩痛是最常见查体表现,此外肾区和阴囊的皮下捻发音在某些患者中也可触及 [3] [8]。实验室检查有70%~80%的患者血常规白细胞增多,而血小板减少症发生率为15%~20%。同时还可能有肌酐升高,肉眼或镜下血尿伴严重蛋白尿。因大部分患者有糖尿病,高血糖水平是一种共同表现 [3] [6]。
3.5. 诊断
EPN的诊断主要依靠影像学检查,临床症状及实验室检查无法做出确诊。超声和腹部平片诊断的准确率仅为69%和65%,因CT对于气体的检测优于其他影像学检查,且能够评估疾病进展程度,因此CT是诊断该疾病最可靠的方法之一 [4] [5] [8]。本组2例患者同样是依靠CT确诊,所以建议怀疑EPN的患者尽早行CT检查避免延误治疗时机。
3.6. 治疗
在确诊气肿性肾盂肾炎后,需及时行复苏、支持治疗,其目的主要是维持血流动力学稳定和保持呼吸通畅。基本的复苏措施包括氧气吸入、静脉输液、纠正酸碱平衡紊乱和经验性抗生素应用及控制血糖,建议血糖控制在10 mmol/L以下。EPN患者需保持收缩压在100 mmHg以上,若患者血流动力学不稳定,应立即予以扩容治疗 [3]。在一项针对对影响EPN患者死亡率危险因素的meta分析中指出:与100 mmHg以上的血压相比,收缩压为90 mmHg以下的患者死亡率明显升高 [3]。在细菌培养结果明确提示具体菌种之前,可经验性使用抗革兰阴性菌药物。常用抗生素包括β内酰胺酶抑制剂类、氨基糖苷类、喹诺酮类等,必要时使用碳青霉烯类药物;根据病情变化及细菌培养结果调整抗生素。此外,EPN患者可能需要透析形式的肾脏支持措施,肾脏支持治疗能有效降低患者死亡率。肾功能的恢复情况由肾实质损伤程度和其他并发的肾脏疾病共同决定 [3]。
EPN的外科治疗主要包括经皮肾穿刺引流术、肾切开引流术、肾切除术等。20世纪80年代以前EPN的外科治疗主要以开放性切开引流术、肾切除术辅以抗生素治疗为主 [10]。1986年,Huduson等 [11] 报道了一例EPN患者行经皮肾穿刺引流术,术后恢复良好。此后,经皮肾穿刺导管的发展使经皮肾穿刺引流治疗EPN成为可能,穿刺引流的引流管应使用至少为14 Fr猪尾巴引流管。经皮肾穿刺引流适用于气体较为局限且剩余肾实质仍有功能的患者 [4]。2014年Olvera-Posada等 [12] 对62例EPN患者的治疗进行分析,以保留肾单位为主的治疗方案占51.6%。气肿性肾盂肾炎的外科治疗由早期的急诊行患侧肾脏切除转变为经皮肾穿刺引流术。经皮肾穿刺引流结合内科治疗是创伤最小且效果最好的治疗方式,治愈率在30%~100%,病死率最低仅为13.5%。有脓肿或多个脓肿并不是经皮肾穿刺引流的禁忌症,因为不止一个导管可用于引流脓肿 [4]。从技术上讲,脓肿更容易进入,并且会显著降低剩余肾组织的压力。因此应首选经皮肾穿刺引流为治疗方案。引流管应一直保留到后续的治疗,必要情况下可以用抗生素溶液冲洗引流管 [3]。
然而不是所有EPN患者均可通过经皮肾穿刺引流术获得治愈。Huang等 [8] 的研究发现,糖尿病、血小板减少、急性肾功能衰竭、意识障碍、休克是EPN进展的危险因素。在1级和2级EPN(基于Huang分类)中,单独内科治疗或同时行肾穿刺引流,可获得良好的治愈效果。在3级和4级EPN患者中,内科治疗 + 肾穿刺引流在低于2个危险因素的患者中,治愈率达85%;而在大于2个危险因素的患者中,失败率为92%。在一项对行肾穿刺引流的118例患者统计中发现,15例(13%)需要行肾切除术,这些患者行肾穿刺引流后引流不畅,或者在影像检查中肾脏已无功能 [4]。存在2个及2个以上危险因素的EPN患者,患侧肾切除术应作为经皮肾穿刺引流失败后的替代治疗方案。开放肾切除术和腹腔镜肾切除术在治疗效果上没有差异,且腹腔镜手术恢复时间会更快 [3]。本组第1例患者存在糖尿病、血小板减少、右肾功能衰竭等3个危险因素,在行经皮肾穿刺后无明显液体引出,考虑与患侧肾脏已无功能、肾内已基本无正常组织结构、其内被坏死组织等填充有关,最终行肾脏切除术。因此,对于肾穿刺引流病情无明显改善或持续进展的患者及早行肾切除术是其最适治疗方案。
4. 结论
气肿性肾盂肾炎是一种罕见却极其凶险的泌尿系统感染性疾病,腹部CT是诊断和随访的首选影像学检查方法,早期诊断和治疗尤为重要。糖尿病患者出现寒战发热、腰痛伴泌尿系感染等症状时应考虑到气肿性肾盂肾炎的可能。一旦确诊,应尽早使用抗生素,同时严格控制血糖、纠正电解质紊乱、维持血流动力学稳定、营养支持和原发病治疗。若患者病情改善不明显,影像学检查提示脓肿较大或肾衰竭加重等应考虑行经皮肾穿刺引流术,必要时行肾切除术。