1. 引言
小麦(Triticum aestivum L.)是世界性的重要粮食作物,适应性广,较耐储藏,作为我国最重要的口粮之一,小麦产业发展直接关系到我国的粮食安全和社会稳定 [1] [2]。目前全球干旱、半干旱地区约占土地总面积36%,占耕地面积的43%,大多数国家都面临水资源危机,我国也不例外。就目前来看,干旱问题已然成为影响作物产量以及影响作物正常健康生长的一个相当重要的逆境因子 [3]。小麦是我国最主要粮食作物之一,种植面积相当广泛,而小麦大部分主产地处于这些干旱、半干旱地区,干旱是限制我国小麦产量的主要因素之一 [4]。所以小麦的抗旱性育种已经成为当前小麦育种不可忽视的问题。据研究,小麦在干旱的胁迫环境下会导致相对含水量、以及过氧化氢酶(CAT)、过氧化物酶(POD)活性的下降以及电导率、丙二醛(MDA)含量、脯氨酸含量、超氧阴离子产生速率的上升,引起了植株的光合速率的降低,造成植株干物质积累减少,同时干旱条件下活性氧(ROS)在体内积累,对植株造成损伤,消耗增多,最终导致了小麦产量的降低 [5] [6]。中国是全球人口最多的农业大国,农业可持续发展的重要性显而易见。在中国农业可持续发展中,提高农业资源转化率是核心问题,而其中的水资源又是关键 [7]。如何提高农业水资源的转化效率需要植(作)物抗旱性、抗逆性理论的支撑,这也是当前植物生理学、作物生理学和逆境生物学(stress biology)的中心问题,更是现在从分子水平上探索植物水分胁迫响应机理的国际分子生物学(molecular biology)前沿热点问题之一 [8] [9] [10]。小麦对非生物胁迫(abiotic stress)干旱的反应机制我们尚未完全了解,对于这一类相关研究是我们必须去做的事情。研究小麦对干旱胁迫的反应,会为以后的抗旱育种工作提供很大帮助。
随着气候条件的恶化,和降水的不平衡,我国大部分地区处在干旱和半干旱之间,水资源成为制约农业发展的一个主要因素 [11] [12]。小麦在我国属于主要种植作物,作为我国人民的主食,满足人体提供所需的蛋白质。干旱胁迫会对小麦造成严重的危害,在降水量不平衡的背景下,尤其是在缺乏降水的夏季,干旱往往伴随着高温的发生,直接后果是小麦产量的降低 [13]。干旱会通过破坏光系统稳定性从而抑制小麦叶片的光合作用,降低叶片的光合速率(Pn),而且在小麦生育进程的不同时期影响程度不同,其迫害程度随生育期的推进而更加严重。研究结果表明,干旱会降低小麦叶片的气孔导度,间接使CO2供应不足,光合速率下将。随着干旱程度增加,植物细胞渗透势升高,细胞含水量下降,水分的丧失导致植物细胞内叶绿素、胡萝卜素以及核酸和其他生物大分子分解 [14] [15] [16] [17]。导致细胞内的各种生理生化反应不能正常进行,最终细胞结构和内含物被破坏。干旱胁迫使光合机构被破坏,光合作用不能正常进行,光合速率显著下降,有机物质得不到积累,小麦的正常生长受到抑制 [18]。高温胁迫降低小麦抗氧化系统的活力 [19]。受到干旱胁迫时,植物会进行光呼吸和梅勒反应,从而过度累积过氧化氢(H2O2);另一方面逆境影响了植株体内多种氧化还原酶的活性,致使活性氧的积累等 [20]。根据研究,得出抗氧化物酶的活性随着干旱程度的升高显著降低,导致植物体内积累的活性氧得不到及时的清除,造成植物体内存在过量的H2O2 [21]。据研究证明干旱胁迫使得在植物体中起清除活性氧作用的过氧化物酶(POD)及超氧化物歧化酶(SOD)和抗坏血酸过氧化物酶(APX)的活性显著降低 [22]。但不同阶段、不同程度的高温胁迫对抗氧化系统的影响有所不同。研究结果表明,干旱胁迫势必通过影响光合速率、蒸腾速率、气孔导度等光合结构而引起细胞的抗氧化系统紊乱,并最终降低小麦产量 [23]。如何破解干旱危害影响,提高小麦自身的干旱耐性已成为作物学科研究热点。研究表明,干旱会加速小麦叶片衰老抑制小麦产量品质形成,干旱胁迫减弱了光合产物供应能力 [24]。蛋白质和淀粉分别占小麦籽粒重的9%~26%和65%~74%左右,在很大程度上决定了小麦粒重 [25]。干旱胁迫导致灌浆期缩短,粒数和粒重降低,产量严重下降,这与小麦灌浆及储存干物质向籽粒的运转都和干旱胁迫条件有一定的联系有关,同时还会降低与其有关联的酶活性,从而严重干扰了产量形成因素,导致小麦的产量严重下降 [26]。
2. 实验材料与方法
2.1. 供试材料
筛选后的小麦品种共7个,编号分别是① 542439;② 277131;③ 538726;④ 277130;⑤ 10474;⑥ 343181;⑦ 237659。
2.2. 实验地区概况
试验地土壤黄棕壤土,地面平整,土层深厚,地力中等,土壤pH = 6.5,土壤有机质含量为1.39%,速效氮为87 mg∙kg−1,速效磷为13 mg∙kg−1,速效钾为72 mg∙kg−1。试验期间常出现高温干旱天气。
2.3. 栽培措施与试验设计
采用原位土回填的大田盆栽的栽培方式(即取大田0~20 cm耕作层土壤装入试验盆,然后将试验盆埋入试验田中)。小麦种植于聚乙烯塑料盆,每个盆钵(高30 cm,直径25 cm)内装过筛土7.5 kg,盆底部嵌入地面以下20 cm。为保证植株营养需求,每盆施用全N 1.2 g,P2O5 0.36 g和K2O 0.9 g,分别相当于大田每公顷施纯N 220 kg,P2O5 90 kg,K2O 165 kg。其中氮肥分两次施入,基追比为5:5,追肥于拔节期施入。土壤经水沉实后播种,每盆播种16粒,在三叶一心时,间苗至每盆8株。每份材料三个重复,分别随机种植于三个盆子内,试验盆周围大田种植相同品种小麦,栽培措施如大田。开花期选择长势一致的小麦植株进行标花。
本研究针对山羊草,野生二粒小麦和节节麦等世界各地的小麦种质资源观察生理响应,进行系统抗旱性评价;为进一步系统研究小麦的抗旱分子基机理和育种提供材料。在干旱胁迫条件下,对7个小麦品种进行抗旱鉴定。以材料分蘖进行分株种植,播种前土壤经水沉实,以保证小麦正常发芽,每三天浇一次水,保持土壤湿度。土中种植培养一个月后,停止浇水,把小麦转移至人工气候室开始进行干旱胁迫。分别于0/10/20天上午10时左右取材料,进行植株的生理指标测定。
2.4. 测定项目与方法
2.4.1. 相对含水量
称取植株材料0.2 g的鲜重(FW),及其饱和鲜重(SFW)。再称取干重(DW)。用以下公式计算相对含水量(RWC)。
[15]
土壤相对含水量:(湿重 − 干重)/干重。
2.4.2. 电导率
称取植物新鲜样品0.1 g,测定电导率S1,在水浴锅中煮沸直到植物组织完全被杀死后测定电导率S2。其相对电导率为L = S1/S2 [15]。
2.4.3. 超氧阴离子产生速率
样品提取:0.5 g小麦叶片,加5 ml酶提取液[50 mmol∙L−1 pH 7.0磷酸缓冲液(PBS),0.4% (W/V)聚乙烯吡咯烷酮(PVP)]冰浴研磨成匀浆,之后10,000 g/min冷冻离心20 min,上清液即为酶液。叶片超氧阴离子(
)产生速率参考前人的方法(Wang and Luo, 1990)。500 μl提取液加入pH 7.0 PBS和10 mmol∙L−1羟胺,于25℃水浴中保温20 min,加入17 mmol∙L−1对氨基苯磺酸和7 mmol∙L−1 α-萘胺,之后25℃水浴中保温20 min,测定530 nm处OD值 [15]。
2.4.4. 丙二醛含量
丙二醛(MDA)含量测定参考Zhang (1992)等的方法。加入4 ml三氯乙酸和硫代巴比妥酸混合液,1 ml酶液,沸水浴20 min,4000 g/min离心15 min,上清液测定532 nm和600 nm处的OD值 [15]。
2.4.5. 脯氨酸含量的测定
采用酸性茚三酮显色法测定 [15]。
2.4.6. 抗氧化物酶活性
过氧化氢酶(CAT)活性
CAT酶活性(mgH2O2/gFW∙min) = (A − B) × VT × 1.7/FW × VT × t [15]
过氧化物酶(POD)活性
POD活性(ΔA470/min∙gFW) = ΔA470 × V/Va/W = ΔA470 × 5/0.02/0.5 = ΔA470 × 500 [15]
2.4.7. 综和抗旱系数、抗旱隶属函数值的计算
综和抗旱系数(RI) =
[16]
式中:PI = Xi/Cki:Xi为干旱胁迫条件下相对含水量的值,CKi为正常灌水条件下相对含水量的值
隶属函数值
式中:X为各品种的相对含水量的值,Xmax和Xmin分别为所有品种相对含水量的最大值和最小值。最后累加每个品种各指标的抗旱隶属值,并求其平均值。平均值越大,表示抗旱性越强。
抗旱分级标准:
综和抗旱系数:强抗RI ≥ 1.00;中抗0.99 ≥ RI ≥ 0.90;干旱敏感型RI ≤ 0.89抗旱隶属函数值:强抗X(u) ≥ 0. 60;中抗0.499 ≥ X(u) ≥ 0.40;干旱敏感型X(u) ≤ 0.499。
2.5. 统计分析
运用Microsoft2010进行数据处理和作图,通过DPS数据处理系统进行数据分析。
3. 结果与分析
3.1. 干旱胁迫下不同小麦品种叶片相对含水量变化
由表1可知在小麦灌溉10天后,田间取样测得各品种小麦的叶片含水量之间无显著性差异。D1组和D0组测得的各品种叶片相对含水量均有不同程度的下降,并达到显著水平。且在D1处理水平条件下,下降的幅度依次为③ 538726 < ⑥ 343181 < ⑦ 237659 < ② 277131 < ① 542439 < ④ 277130 < ⑤ 10474;在D0处理水平条件下,下降的幅度依次为③ 538726 < ⑥ 343181 < ⑦ 237659 < ① 542439 < ④ 277130 < ⑤ 10474 < ② 277131。这说明小麦品种,③ 538726受干旱胁迫的影响最小,其次是⑥ 343181和⑦ 237659这两个品种对干旱的敏感度相对较低。而② 277131和① 542439的短期内抗旱能力高,但长期处于干旱环境下生长则会受到抑制。因而综合考虑,③ 538726、⑥ 343181和⑦ 237659这三个品种综合抗旱性较好,可作为小麦抗旱育种的优质材料,④ 277130、⑤ 10474这两个个品种的耐旱性较差,抗旱育种时不宜考虑。

Table 1. Relative water content of different wheat varieties
表1. 不同小麦品种叶片相对含水量
注:同行中标注不同小写字母的数据代表处理间差异在5%水平显著。下同。
3.2. 干旱胁迫下不同品种小麦叶片相对电导率变化
由图1可以看出,小麦叶片在受到干旱胁迫时相对电导率升高。干旱条件下各个品种的叶片RWC降低,导致叶片相对电导率的升高。抗性强的作物品种在干旱环境下叶片相对含水量降低缓慢的,相对电导率上升平缓,植物受伤害程度较轻。由图1可知,编号为③ 538726、⑥ 343181和⑦ 237659的品种在干旱条件下相对电导率升高慢且程度平缓,表明其耐旱性强;品种编号① 542439;④ 277130;⑤10474由于RWC降低幅度极大,相对电导率上升的也很快,表明了其对干旱反应最敏感,耐旱性最弱。
 注:图中同一品种上标的不同小写字母代表处理间差异在5%水平显著。下同。
注:图中同一品种上标的不同小写字母代表处理间差异在5%水平显著。下同。
Figure 1. Changes of relative conductivity of different wheat cultivars under drought stress
图1. 干旱胁迫下不同品种小麦叶片相对电导率的变化
3.3. 干旱胁迫下不同品种小麦叶片超氧阴离子产生速率、丙二醛含量变化
由图2和图3可知,小麦在干旱胁迫下叶片超氧阴离子产生速率和丙二醛含量均显著提高。通常植物在干旱胁迫下体内活性氧积累会超过正常水平,抗氧化酶会受ROS (活性氧)的增加而被诱导合成,用以抵御清除活性氧和防止膜脂过氧化,从而增强植物的自我保护能力 [18] [19]。丙二醛(MDA)是脂质过氧化的主要产物之一,其浓度反映了膜脂过氧化程度,在本研究中,干旱情况下,小麦叶片的超氧阴离子产生速率直线上升,MDA含量总体呈现上升趋势。但从图2和图3可看出,编号为② 277131、③ 538726和⑥ 343181的品种却综合呈现出缓慢上升的过程,上升幅度也较小,这表明了其对外界干旱胁迫相对不敏感,在干旱条件表现出较好的耐旱性。同时,这几个品种有较高的保护酶活性。在胁迫前期和中期,主要是以增强保护酶活性来有效地清除活性氧,抑制膜脂过氧化,而在胁迫后期,在各种抗氧化酶活性降低的条件下,则靠增加渗透调节能力来适应干旱。相比之下品种⑦ 237659的超氧阴离子产生速率和丙二醛含量在受旱前期上升较② 277131、③ 538726和⑥ 343181相对缓慢,但在干旱胁迫后期超氧阴离子的产生速率和丙二醛含量突然升高,说明品种⑦ 237659耐短期干旱,不能长期生长在干旱地区。
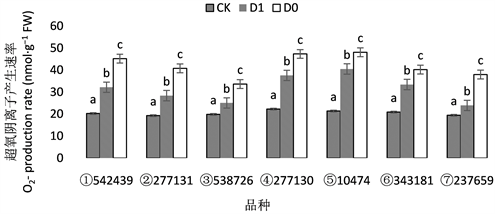
Figure 2. Effect of drought stress on the rate of superoxide anion production in different wheat cultivars
图2. 干旱胁迫对不同品种小麦叶片超氧阴离子产生速率的影响
3.4. 干旱胁迫下不同品种小麦叶片脯氨酸含量变化
植物在受到逆境胁迫时,体内会迅速积累脯氨酸这类渗透调节物质,以及时改变细胞渗透式,防止细胞过度失水,对植物体造成不可恢复的伤害 [20]。脯氨酸通过渗透调节,可以保护植物体中的重要蛋白质和酶类,避免其变性失活,使各种生理生化反应能够正常进行,缓解逆境(干旱)对植物的伤害。从图4中可以得出品种③ 538726各处理间的脯氨酸含量变化最不显著;品种② 277131在分蘖后灌水的脯氨酸含量相对于D0处理之间有上升但没有达到显著水平;灌水量对品种⑦ 237659的影响微弱,W1处理组与对照组之间脯氨酸含量的差异没有达到显著水平。

Figure 3. Effect of drought stress on malondialdehyde content in different wheat varieties
图3. 干旱胁迫对不同品种小麦叶片丙二醛含量的影响
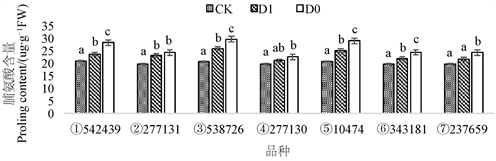
Figure 4. Changes of proline content in wheat leaves of different cultivars under drought stress
图4. 干旱胁迫下不同品种小麦叶片脯氨酸含量的变化
3.5. 干旱胁迫下不同品种小麦叶片抗氧化物酶活性变化
植物在受到干旱胁迫时,体内活性氧清除机制被破坏,活性氧产生和清除的动态平衡被打破,导致活性氧在体内过度积累;另一方面逆境影响了植株体内多种氧化还原酶的活性,致使活性氧的积累,植物体受到伤害。过氧化氢酶(CAT)、过氧化物酶(POD)等抗氧化物酶作为活性氧清除酶类,其作用是清除植物体内过多的活性氧,避免其过度积累 [21] [22] [27]。在受到干旱胁迫时,活性氧的不断积累,会破坏植物体内的抗氧化系统,并进一步破坏抗氧化物酶的活性。由此得出结论在同样的逆境条件下,抗氧化物酶活性高,则抗旱能力相对较强。由图5、图6可以看出品种② 277131、③ 538726、⑥ 343181和⑦237659的CAT活性和POD活性都相对较高,且活性降低较小,其中品种③ 538726的耐旱性状最好,D1处理和D0处理之间CAT和POD的活性改变较小,没有达到显著水平。
3.6. 不同小麦品种抗旱指标
为了评价这7个小麦品种的抗旱能力,我们通过计算各品种的综合抗旱系数与抗旱隶属函数值来观察的品种小麦的耐旱性。由表2可知品种③ 538726的综合抗旱能力最强,品种⑦ 237659与⑥ 343181的耐旱性略次之。品种④ 277130的耐旱能力最弱,不宜在干旱地区种植。
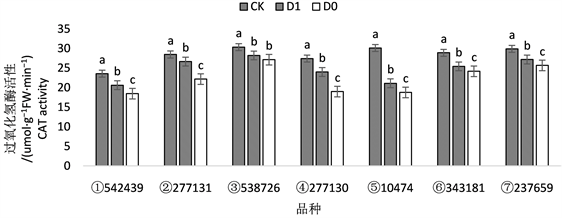
Figure 5. Changes of CAT activity in different wheat cultivars under drought stress
图5. 干旱胁迫下不同品种小麦叶片CAT活性的变化
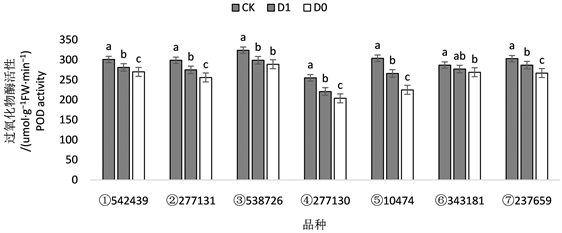
Figure 6. Changes of POD activity in different wheat cultivars under drought stress
图6. 干旱胁迫下不同品种小麦叶片POD活性的变化

Table 2. Drought resistance indicators of different wheat varieties
表2. 不同小麦品种抗旱指标
4. 讨论
本研究结果表明,逆境条件下,植物通过代谢变化即形成逆境蛋白、增加渗透调节物质等来提高细胞对逆境的抵抗能力,其中可脯氨酸等是植物体内重要的渗透调节剂 [25] ,可使植物在逆境条件下维持正常的渗透压,通过清除活性氧以及激发抗氧化酶活性,来增强植物的抗性。逆境胁迫会导致植物根系对水分和养分的吸收量降低,导致丙二醛含量和超氧阴离子在植物体内积累,加剧了逆境对物植物的伤害 [28]。本实验中,干旱胁迫下,各品种小麦叶片的丙二醛含量大幅度增加,是细胞膜脂过氧化作用加强的结果,且干旱导致细胞内POD、SOD等抗氧化酶的活性降低,从而加剧干旱胁迫导致小麦产生的氧化胁迫。
5. 结论
通过对叶片相对含水量、电导率、丙二醛(MDA)含量、脯氨酸含量、以及过氧化氢酶(CAT)和过氧化物酶(POD)等的数据分析,我们得出以下结论:
叶片相对含水量在干旱胁迫下,随着供植株生长的土壤相对含水量不断下降,叶片相对含水量也都呈下降趋势。干旱胁迫下,编号③ 538726和⑥ 343181品种在干旱条件下RWC降低幅度较小,相对电导率升高慢,表明其耐旱性强;品种编号④ 277130和⑤ 10474由于RWC降低幅度极大,相对电导率上升的也很快,表明了其对干旱反应最敏感,耐旱性最弱。在干旱条件下,能长期保持较高含水量的品种的耐旱性较好。编号为② 277131和④ 277130的品种在胁迫前期含水量较高,但胁迫后期含水量骤降,波动性大;而编号为③ 538726的品种含水量保持相对平缓,表示其对外界的干旱胁迫并不敏感。
干旱胁迫下,超氧阴离子的产生速率迅速升高,但是③ 538726和⑦ 237659的产生速率最慢,编号为④ 277130和⑤ 10474的产生速率最高,最不耐干旱。
干旱情况下,MDA含量总体呈现上升趋势,但是编号③ 538726、⑥ 343181和⑦ 237659品种的MDA含量增加量较少,这表明了其应对外界环境的干旱胁迫能力较好。
干旱胁迫下,脯氨酸含量呈整体呈现上升趋势,其中编号为③ 538726和⑤ 10474的品种,脯氨酸的增量较其他品种多,有利于其应对干旱的胁迫,② 277131、④ 277130的脯氨酸含量增量较少,不利于其抗旱生长。
在干旱条件下生长时,在CAT活性方面,试验的7个品种中,编号为③ 538726和⑤ 10474的品种CAT活性变化较为平缓,且每次样品的活性均较高;而编号为① 542439和④ 277130的品种CAT活性波动最大,最终CAT活性又降至最低,其耐旱性状最差。
干旱胁迫下POD活性升高,细胞清除自由基能力增强,在底物浓度对酶活性影响的下,逆境时抗旱性弱的植株品种产生的自由基多,而同一逆境下自由基的生成量差异也可以理解成是抗旱性不同所致。根据实验中数据的波动状态,并不是始终上升或始终下降趋势,即抗氧化酶活性波动较小、曲线相对平缓的品种抗旱性较好。根据编号为③ 538726和⑥ 343181的品种三次取样测得的POD活性变化图,在试验的7个品种中,它们的变化最为平缓。图6表现的是编号为④ 277130 ⑤ 10474和品种的POD活性变化,在7个试验品种中,其波动最大。
结果表明:编号为③ 538726的品种抗旱系数与抗旱指数在7个品种中排最高,且总体变化趋势相对平缓,在胁迫后期仍能保持较高的含水量和抗氧化酶活性,耐旱性好;编号为② 277131的品种在胁迫前期综合性状较好,在短期内抗旱性较好;编号为④ 277130的品种总体来看,耐旱性较差。
基金项目
国家重点研发计划项目(2017YFD0301304)。
NOTES
*通讯作者。