摘要:
目的:分析角膜曲率对Haigis,SRK-II,Hoffer-Q,Hollday-1及SRK-T 5种人工晶状体屈光度计算公式在高度近视伴后巩膜葡萄肿合并白内障患者中的影响,从而为眼科临床工作提供理论依据。方法:选取我院行白内障手术的高度近视并后巩膜葡萄肿的患者59例(72眼),术前分别用IOL Master测量眼轴长度,角膜曲率,前房深度等参数,然后选择眼轴长度为26.0 mm ≤ AL ≤ 30.0 mm的患者,按照角膜曲率分为A组(K ≤ 43.0 D),B组(43.0 D < K ≤ 45.0 D),C组(K > 45.0 D)。分别对每组患者采用IOL Master500系统带的Haigis,SRK-II,Hoffer-Q,Hollday-1,SRK-T 5种人工晶状体屈光度计算公式预测术后屈光,术后3个月联合显然验光及电脑验光的实际屈光值,与各公式预测的实际平均屈光误差(MNE)及平均绝对屈光误差(MAE)进行比较。从而评价各种人工晶状体计算公式在高度近视伴后巩膜葡萄肿患者的优劣。结果:Haigis,SRK-II,Hoffer-Q,Hollday-1,SRK-T公式在A组计算的MNE各个公式之间比较无显著差异(F = 0.242, P = 0.913);B组公式之间比较有显著差异(F = 1.040, P = 0.393);C组间比较出现了差异(F = 2.561, P = 0.047),SRK-II与其余各组比较均有意义(P < 0.05)。在MAE的比较中,A组中各公式之间比较无明显差异(F = 0.128, P = 0.971);B组各组之间的比较有明显意义(F = 3.407, P = 0.013);C组组间比较出现了差异(F = 4.762, P < 0.05);SRK-II与其余各组比较均有意义(P < 0.05);Haigis与其余各组之间均出现了差异(P < 0.05)。结论:在高度近视伴后巩膜葡萄肿的患眼中,当K ≤ 43.0 D及K > 45.0 D时,Haigis最准确,SRK-T,Hoffer-Q次之,SRK-II准确性最差;43.0 D < K ≤ 45.0 D,SRK-T更准确,其次是Haigis,Hollday-1,Hoffer-Q,SRK-II。
Abstract:
AIM: To analyze the effect of Haigis, SRK-II, Hoffer-Q , Hollday-1, SRK-T formulas for calculating the intraocular lens (IOL) power for eyes of high myopia with posterior staphyloma, and make guidance for the practical application of clinical work. METHODS: Prospective clinical study. Seventy-two eyes of fifty-nine cases of high myopia with posterior staphyloma were treated with cataract surgery in our hospital. IOL Master was used to measure axial length (AL), cornea curvature (K), anterior chamber depth (ACD) and other parameters before operation, and the patients with 26.0 mm ≤ AL ≤ 30.0 mm were selected, which were then divided into 3 groups: group A (K ≤ 43.0 D), group B (43.0 D < K ≤ 45.0 D), group C (K > 45.0 D). They all underwent regular phacoemulsification and posterior chamber IOL implantation. The actual postoperative refraction was measured with the methods of phoropter and subjective optometry 3 mo after surgery. Then we took MNE (mean numerical error) and MAE (mean absolute error) as comparison parameters to compare the differences of the predicted and actual postoperative refraction of the five formulas in each group. RESULTS: MNE: There was no significant difference in group A (F = 0.242, P = 0.913) and B (F = 1.040, P = 0.393); There was a difference between group C (F = 2.561, P = 0.047), and the compari-son between SRK-II and other groups was significant (P < 0.05). MAE: There was no significant dif-ference among the formulas in group A (F = 0.128, P = 0.971), but group B had obvious significance (F = 3.407, P = 0.013); and comparing the differences between group C (F = 4.762, P < 0.05), SRK-II and Haigis, all showed difference and the data were statistically significant (P < 0.05). CONCLUSION: When the cornea curvature was too large or too small (K ≤ 43.0 or K > 45.0 D), Haigis was the most accurate, then the SRK-T and Hoffer-Q, SRK-II the last. But when cornea curvature was normal (43.0 D < K ≤ 45.0 D), the order was SRK-T, Haigis, Hollday-1, Hoffer-Q, SRK-II.
1. 引言
高度近视由于眼球纵向上进行性拉长,巩膜变薄,在眼内压的作用下极易发生后巩膜萄肿(posterior staphyloma, PS)。此类患者合并白内障后行白内障超声乳化抽吸联合人工晶状体植入术是矫正视力的一种有效的治疗方法。但是由于眼球解剖结构变化以及后巩膜葡萄肿位置的不确定性导致影响人工晶状体度数的两大因素:生物参数测量和人工晶体度数的计算公式选取,一直是临床上比较棘手的问题。本文通过回顾性研究,使用IOL Master光学法进行术前生物参数的测量,比较分析生物参数中的角膜曲率对Haigis,SRK-II,Hoffer-Q,Hollday-1,SRK-T 5种人工晶状体屈光度计算公式的准确性研究进行分析。
2. 对象和方法
2.1. 临床对象
选取2016年6月~2017年5月青岛大学附属医院眼科住院行白内障手术的高度近视并后巩膜葡萄肿的患者59例(72眼),其中男性38例(45眼),女性21例(27眼);年龄在50~88岁,平均(65.7 ± 9.6)岁。本项目经青大附院伦理委员会伦理通过(批准编号:ChiCTR1800015251)。
2.2. 纳入及排除标准
1) IOL Master测量的眼轴长度26.0 mm ≤ AL ≤ 30.0 mm,眼部B超示存在后巩膜葡萄肿;2) 术前患者注视好,晶状体混浊程度(C1-3N1-3P1-4),不伴有角膜以及影响结果的其他眼疾,或手术史、外伤史;3)术中人工晶状体均固定于囊袋内,光学面居中;4) 术中及术后未出现严重并发症;5) 术后最佳矫正视力≥ 0.2;随访 ≥ 3 mon。
2.3. 术前检查及术中操作
术前均进行眼科常规检查:裂隙灯,眼压,验光,眼底,B超及黄斑部OCT检查。由同一技师使用IOL Master测量患者的角膜曲率(K),眼轴长度(AL),前房深度(ACD);测量过程中保证信噪比(SNR) ≥ 2.0,取测量5次的平均值。
手术均有同一位资深教授操作,手术方式均为PHACO + IOL植入术。术前表面麻醉,左眼鼻上方或右眼颞上方做透明角膜缘3.0 mm的微切口,前房注入玻璃酸钠后连续撕囊,直径约5 mm,晶状体核乳化后吸净皮质后均放入囊袋同一种Rayner折叠后房型人工晶状体,冲洗前房,水密切口,术毕。术后给予局部眼药水抗炎治疗4 w。
2.4. 术后检查
术后3 mon对术后患者分别行裂隙灯,眼压,眼底,B超及黄斑部OCT检查,并由同一检查者对患者进行电脑验光及显然验光,获得患者术后实际屈光度数(屈光度SE = 球镜 + 1/2柱镜)。根据IOL Master中Haigis,SRK-II,Hoffer-Q,Hollday-1,SRK-T几种公式预测的屈光度数进行差值比较,计算平均屈光误差(mean numerical error, MNE),和平均绝对屈光误差(mean absolute error, MAE)。
2.5. 分组方法
对患者角膜曲率(K)分成以下组:K ≤ 43.0 D,43.0 D < K ≤ 45.0 D和K > 45.0 D三组,分别为A组,B组,C组。
2.6. 统计学方法
采用SPSS19.0软件分析,对数据进行正态分析,数据不完全符合正态分布及方差齐性;对符合正态分布的数据采用
描述,采用方差分析,有差异的再对组间两两比较采取SNK检验;对不符合正态分布的数据采用秩和检验,所有检验水准为P < 0.05。
3. 结果
3.1. 各组患者基本资料的比较
详见表1。
3.2. 各组平均屈光误差(Mean Numerical Error, MNE)比较
按K分为A,B,C三组,其中A组中Haigis,SRK-II,Hoffer-Q,Hollday-1,SRK-T平均误差值分别为:(−0.328 ± 0.751) D,(−0.717 ± 0.864) D,(−0.175 ± 0.912) D,(−0.194 ± 0.760) D,(−0.275 ± 0.680) D,均为负值表现,并且比较无明显统计学意义(F = 0.242, P = 0.913),其中Hoffer-Q,Hollday-1的值最小。B组中各公式的值为:(0.340 ± 0.419) D,(0.767 ± 1.130) D,(0.567 ± 0.766) D,(0.548 ± 0.681) D,(0.165 ± 0.519) D,Haigis和SRK-T误差值最小,各组之间的比较无明显意义(F = 1.040, P = 0.393)。C组中对应的误差值为(−0.381 ± 1.119) D,(−1.213 ± 1.571) D,(−0.856 ± 1.262) D,(0.503 ± 1.465) D,( −0.350 ± 1.260) D,组间比较出现了差异(F = 2.561, P = 0.047),SRK-II与其余各组比较均有意义(P < 0.05);Haigis和SRK-T出现负值表现且最为接近,差异无意义;Hollday-1出现了正值表现。在三组比较中,SRK-II的误差值均最大。详见表2。

Table 1. Basic preoperative data of patients
表1. 患者术前基本资料

Table 2. Comparison results of MNE between groups with different formulas
表2. 不同公式间MNE的组间比较结果

Table 3. Comparison results of MAE between groups with different formulas
表3. 不同公式间MAE的组间比较结果
3.3. 各组平均绝对屈光误差(Mean Absolute Error, MAE)比较
A组中Haigis,SRK-II,Hoffer-Q,Hollday-1,SRK-T平均误差值分别为:(0.595 ± 0.535) D,(0.072 ± 0.864) D,(0.588 ± 0.603) D,(0.175 ± 0.912) D,(0.642 ± 0.635) D,比较无统计学意义(F = 0.128, P = 0.971),其中SRK-II的值最小,其次为Hollday-1和Haigis。B组中各公式的值为(0.446 ± 0.293) D,(0.893 ± 0.671) D,(0.817 ± 0.465) D,(0.745 ± 0.438) D,(0.414 ± 0.339) D,各组之间的比较有明显意义(F = 3.407, P = 0.013)。Haigis和SRK-T差值较小。C组中对应的误差值为(0.750 ± 0.895) D,(1.054 ± 1.148) D,(1.070 ± 1.071) D,(1.105 ± 1.050) D,(1.010 ± 0.788) D,组间比较出现了差异(F = 4.762, P < 0.05),SRK-II与其余各组比较均有意义(P < 0.05);Haigis与其余各组之间均出现了差异(P < 0.05)。详见表3。
3.4. 不同组别中屈光值在±0.5 D和±1.0 D之间的比例
A组Haigis,SRK-II,Hoffer-Q,Hollday-1,SRK-T 5种公式的屈光值在±0.5 D之间的百分比分别为:68.3%,42.0%,48.3%,38.7%,41.7%;B组的百分比依次为52.2%,26.1%,40.4%,31.8%,50.2%;C组则是59.6%,13.2%,30.4%,43.5%,52.2%。
对应的5种公式屈光值在±1.0 D之间的百分比:A组依次为:91.7%,58.3%,83.3%,91.7%,83.3%;B组依次为:82.6%,52.2%,65.2%,71.1%,80.6%;C组为84.1%,34.2%,60.2%,69.6%,78.3%。详见图1,图2。
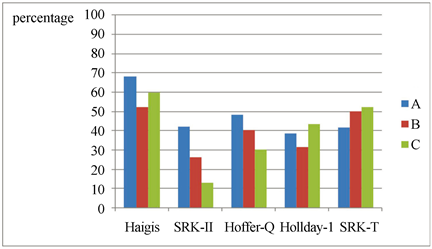
Figure 1. Proportion of MNE calculated by different formulas in ±0.5 D
图1. 不同公式计算的MNE在±0.5 D所占的比例

Figure 2. Proportion of MNE calculated by different formulas in ±1.0 D
图2. 不同公式计算的MNE在±1.0 D所占的比例
3.5. 各种公式之间与术后实际SE的一致性比较(按角膜曲率比较)
图3看出,在5中公式中可以看出除了SRK-II公式,其余4种公式的波动幅度较平和,又有Haigis 更接近术后实际波动情况。
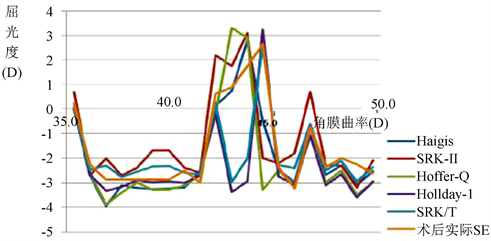
Figure 3. Comparison of consistency between diopter of various formulas and actual SE
图3. 各种公式屈光度与实际SE之间的一致性比较
4. 讨论
随着白内障手术技术的提高和人工晶状体的多样化产生,白内障手术已有传统的复明手术转变为屈光手术,成为矫正视力的一种有效方法。选取合适的度数的IOL,提高术后视觉质量是手术的最终目的,而影响IOL度数选择的因素主要是眼球的生物测量及IOL度数的计算公式。
(一) 眼球的解剖特性及生物测量
高度近视由于眼轴变长,极易发生后巩膜萄肿(posterior staphyloma, PS),PS发生率与近视度数呈正相关。PS根据所在位置可以分为后极部型(最常见)、黄斑型、视乳头周围型、视乳头鼻侧和视乳头下方型5种类型。由于这种解剖结构的变化,使得眼球不仅表现出眼轴长度增加,还附带角膜曲率(corneal curvature, K)增加,散光增大;前房深度(anterior chamber depth, ACD)对于低度近视者变深,>−10 D时由于晶状体前移此时的ACD变浅。这些参数的变化都会影响术后屈光。而0.1 mm眼轴长度误差将会带来0.27 D的屈光误差 [1] [2] ,0.1 mm的角膜曲率半径误差会导致0.57 D的误差,影响均非常显著,这是临床的不能接受的。
在研究中,为增加术前生物测量精确性,我们选择IOL Master光学法。其测量原理是采用类似于OCT技术,利用780 nm激光干涉原理,多次测量进行高强度信号放大。其原理基于角膜曲率计,即测量反射光影像之间的距离,采用的是六点描记,在2.3 mm范围角膜内进行测量。通过计算对角线的长度和模拟椭圆形进行K1和K2的屈光力计算和轴位的计算 [3] ,精确值可达0.01 mm [4] 。加之一次测量可获取AL,ACD,WTW等多个参数,还具有非接触性、坐位测量,不需摘掉眼镜(使得注视更好)等特点,既提高了检查准确率,检查效率以及患者的舒适度又减少了感染几率。但是,由于不同程度的PS的存在,视网膜变薄,各个象限的视网膜厚度不均,使得IOL Master测量时RPE层的定义线有失准确,会对眼轴长度的测量造成一定的误差。据杨青华,郑虔等 [5] [6] 研究表面,在高度近视眼球的术后视力的影响主要是生物参数中的AL及K,所以我们在选择分组中根据K进行讨论研究,来讨论术后MNE及MAE。
(二) 人工晶体屈光度的计算公式及误差分析
目前IOL的计算公式已有回归公式演变到第四代,而在高度近视的长眼轴研究中,主要设计第二代的SRK-II (经验回归公式)和三、四代的SRK-T,Hollday 1,Hoffer-Q,Haigis (理论公式),以及最新的公式Holladay-2,Barrett Universal II,Olsen。最新的公式需要术前参数较多,对预测术后屈光相对可靠,不过正是这样,也同时限制了它们优势,尤其是Holladay-2 (需要AL、K值、晶状体厚度、WTW、ACD、术前屈光状态、患者年龄)和Olsen (需要AL、K值、晶状体厚度、ACD、术前屈光状态、IOL常数)。所以本次研究中主要是分析SRK-II,SRK-T,Hollday 1,Hoffer-Q,Haigis5公式。目前对于正常眼轴的IOL计算公式的选取已成熟,但是对于高度近视伴PS的患者这样的眼球的选择仍存在异议。1990年,Sanders [7] 等报道称,SRK-T公式是预测高度近视的最好公式,但是在他的研究中所选取的欧洲人中高度近视较国人发病率小 [8] ,导致AL > 28.4 mm的病例较少,样本量不足。后来,Asaad A [9] 等研究,在选取的87例患者127只患眼的高度近视长眼轴(AL > 26.0 mm)的研究中,使用SRK-T,Hoffer-Q, Holladay-2和Haigis预测的术后发现,Haigis最好,其次是Holladay-2。Petermeier和Szurman [10] 报道,在平均眼轴为32.35 mm (29.22~36.51 mm)的长眼轴研究中,使用SRK-T,Haigis,和Holladay-1,其中绝对误差值Haigis最小,分别是+0.84 D (SRK-T),+0.67 D (Haigis)和+1.18 D (Holladay-1),而平均误差值则是SRK-T (−0.55 ± 1.79 D),Haigis (+0.04 ± 1.56 D),Holladay-1 (−0.1 ± 2.07 D),仅有Haigis出现了远视状态。Chong Chen [11] 在选取的148只患眼的研究中发现使用Haigis,Hoffer-Q,Holladay-1和SRK-T4种公式时,当眼轴在26.0~33.0 mm时,Haigis和SRK-T均较好,预测的MAE较小,且两者无明显差异,但与其他二者之间存在差异;当眼轴 > 33.0 mm时,Haigis与其他三者均有差异,并且随着眼轴的增加,预测的MAE增大,准确性降低。郑虔等 [6] 人报道,在轴性高度近视眼患者中,SRK-T及优化Haigs公式预测性一致,并且SRK-T随眼轴的增加误差变大,即较短AL (26.0~28.0 mm)比较长AL (30.0~34.0 mm)的误差小,两种公式在不同K的分组中准确性无差异。
以上所有公式的研究均是根据眼轴长度作为出发点,本研究中,我们采用角膜曲率作为研究对象,探讨其对术后视力的影响,从而选择合适的公式减少因角膜曲率带来的术后影响。文章中比较了一个经常作为评估IOL计算公式准确性的指标MAE,但是鉴于它不能反应出结果的方向(近视或远视),所以联合应用MNE。结果中显示:A组和B组的所有公式之间无统计学差异(P < 0.05),在A组中,所有公式术后均出现近视状态,SRK-II (0.072 D)的绝对值最小;B组中的数据显示术后均有远视表现,SRK-T (0.414 D)绝对值最小,其次是Haigis (0.446 D);C组中公式之间差异有意义(F = 4.762, P < 0.05) Haigis预测的术后绝对屈光最小,与其余各组均出现差异,有统计学意义(P < 0.001),其余的组绝对值误差均在1.0 D以上。在选择IOL时使用Haigis时为避免术后出现远视,选择IOL时尽量选稍大度数,并且Haigis [12] [13] 提出在选择正、负度数人工IOL时应用不同的A常数,而不能只使用正度数时的常数,这是导致术后出现远视的一大原因。
根据经验,为保证高度近视患者术后视觉质量,我们术后一般为患者预留一定的近视度数(−3.0 D~−1.0 D)。术后植入的IOL的有效位置(ELP)是术后屈光的主要来源 [14] 。上述几种公式使用的参数及常数是用来预测ELP的,每种公式都有一个A常数。二代的SRK-II计算公式P = A1 − 2.5L − 0.9K (P为正视眼时人工晶状体度数,A1为人工晶状体常数(根据AL进行调整的),L为眼轴长度,K为角膜曲率),是根据模型眼计算出来的,缺乏ACD参数。随后出现的Hollday-1,是利用虹膜表面到植入的IOL表面的距离,将角膜表面到虹膜表面的距离作为穹隆高度;Hoffer-Q则是利用ACD常数,即角膜表面到植入的IOL表面的距离;SRK-T则是人工IOL固定的A常数;Haigis则引入a0,a1,a2三个常数,a0类于其他公式的常数,a1,为ACD常数,a2为AL常数 [15] [16] ,预测ELP = a0 + (a1 × ACD) + (a2 × AL),值得注意的是,公式中未设计到K值的影响,这对于眼球变形导致的角膜K值变化的影响不大,所以在K值变化的病例中我们优选选择Haigis。但是,我们的研究样本量较小,缺乏证明力度。另外,高度近视伴后巩膜葡萄肿的患者眼底基本都会伴随着视网膜脉络膜的萎缩,视网膜劈裂,视网膜下出血等并发症,术前检查和术后视力都会受到一定的影响:术前视力差,检查时导致注视准确性差。其次,IOL Master在测量过程中,只能测量角膜两点间的平均角膜曲率,不能反应整个角膜的曲率和形态信息;最后对于还有一些高龄患者,理解力相对较差,不能很好的配合,都会影响结果。
5. 结论
综上所述,高度近视伴后巩膜葡萄肿患者在现有样本的研究下,当K值较小时,各公式之间均可以,但随着K值增大,优先选择Haigis,其次是SRK-T,Hoffer-Q。尤其是长眼轴、大曲率的情况,Haigis更实用。
基金项目
2016年青岛大学附属医院青年基金优秀项目(QDFY201612)。
NOTES
*通讯作者。