1. 引言
铜元素在微量元素中占据重要地位,长期食用含铜量较高的食物会伤害人体的健康。人口服硫酸铜致死量约为10 g。大量调查研究显示,Cu的毒性受其形态影响,游离的Cu2+拥有更强的毒性,对生物体的破坏更大。在实验室,常用的Cu2+检测方法有原子吸收光谱法、电感耦合等离子发射光谱法、分光光度法等 [1] [2] [3] [4] ,这些检测方法不适宜应用于食药环案件现场的快速检测。因此,研究一种能适用于食药环案件现场快速检测食品或水中Cu2+的方法是很有必要的。
纳米金颗粒(AuNPs)在可见光区具有很高的稳定性以及良好的生物相容性,任何表面结构的改变、聚集,或解职折射率的改变可能都会改变其分散性,最终导致颜色变化,成为最常用的光学传感材料。本论文主要以AuNPs为基础与木瓜蛋白酶合成功能化纳米金,寻找反应的最佳条件,建立木瓜蛋白酶-AuNPs快速检测Cu2+方法,该方法操作简便,灵敏度高,能应用于食药环案件现场快速检测食品或水中Cu2+。
2. 材料与方法
2.1. 仪器设备
UV/VIS Lambda 25紫外–可见分光光度计,美国PerkinElmer公司;
JEOL-2100透射电镜,日本电子公司;
85-2型恒温磁力搅拌器,上海司乐仪器有限公司;
超声波清洗器,上海金棋实业公司;
十万分之一电子天平,德国赛多利斯公司。
2.2. 试剂及溶液配制
铜标准溶液(G62024-90) 1 mg∙mL−1 (10% HCl);木瓜蛋白酶(含量不少于98.5%阿拉丁试剂公司);氯金酸(分析纯,上海试剂一厂),柠檬酸三钠(分析纯,南京化学试剂厂)。
称取木瓜蛋白酶0.0220 g用100 mL容量瓶定溶配置成0.22 mg∙mL−1的木瓜蛋白酶溶液。
氯金酸称得0.9280克于棕色容量瓶中配成100 mL溶液,置内避光存放。
柠檬酸三钠配成质量分数为1%的溶液。
精确移取1.00 mL铜标准溶液于100 mL容量瓶中,加二次蒸馏水稀释至刻度,配成0.0100 mg∙mL−1母液。
3. 实验内容
3.1. 纳米金的合成和表征
纳米金制备 [5] [6] [7] [8] :移取2.00 mL 1%的氯金酸至装有100 mL水和磁石的烧杯中,将烧杯置于磁力加热搅拌器上加热至沸腾,开动磁力搅拌器搅拌的同时迅速加入4 mL 1%柠檬酸三钠水溶液,开始有些变黑,经过一段时间,变蓝,再加热出现红色。煮沸两到三分钟后,出现透明的酒红色,继续加热搅拌至5分钟,移去热源同时停止搅拌。冷却至室温,避光保存即得胶体金溶液。
用紫外可见光谱仪在400~700 nm波长范围表征纳米金溶液,并考察其稳定性。
用透射电子显微镜测定表征上述溶液中纳米金颗粒度。
3.2. 功能化纳米金的合成和表征
精确移取4 mL的柠檬酸钠溶液分别加入到含有1,2,4 mL的木瓜蛋白酶溶液的试管中并且充分振荡;移取2 mL 1%的氯金酸至装有100 mL水和磁石的250 mL的烧杯内,将烧杯置于磁力搅拌器上加热至沸腾,迅速加入柠檬酸钠和木瓜蛋白酶混合溶液。半分钟后溶液开始由无色透明变黑,变紫接着变蓝,煮沸2~3分钟后出现透明酒红色,继续加热搅拌数分钟至5分钟移去热源,同时停止搅拌,冷却至室温后转移到棕色试剂瓶中避光保存,即胶体金溶液,用紫外可见分光光光度计检测,选择最佳配比;用透射电子显微镜表征功能化纳米金的颗粒度。
3.3. 水中铜离子的测定
3.3.1. 吸收光谱法检测铜离子 [9]
Cu2+标准曲线的制备:在1 mL木瓜蛋白酶-AuNPs溶液,分别加入1 mL 1.0、2.5、5.0、7.5、8.0 μg∙mL−1的硝酸铜溶液,充分混合后,用紫外分光光度计测量其吸光度,建立标准曲线。
3.3.2. 应用
取可疑铜污染水质的检材1 mL,加入1 mL木瓜蛋白酶-AuNPs溶液,充分混合后,用紫外分光光度计测量其吸光度,并计算水中铜离子的浓度。
4. 结果与讨论
4.1. 纳米金的合成与表征
按照2.1制备纳米金溶液,得到酒红色溶液,并考察了氯酸金与柠檬酸三钠的配比,见图1。图中样品1.1是氯金酸与柠檬酸三钠的比值为1:1时合成的1%的AuNPs溶液,样品1.2是氯金酸与柠檬酸三钠的比值为1:2时合成的1%的AuNPs溶液。实验结果表明,合成AuNPs溶液氯金酸与柠檬酸三钠的最佳比例为1:2,此时特征峰为520.07 nm。
在最佳比例条件下合成纳米金溶液的颗粒度在透射电镜下检测,其结果见图2。
由图2可以看出制备的纳米金颗粒大小在10~15 nm之间,分离度较好。
将合成的纳米金溶液在棕色瓶中放置6个月后,测定其可见区的吸收光谱,并与之前的吸收光谱比较,考察了该纳米金溶液的稳定性。
由图3可以知道所合成的纳米金溶液在半年前后的最大吸收峰的波长不变,只是吸光度略微减小,因此,纳米金溶液在避光保存的条件下稳定性较好,可以长期保存。
4.2. 功能化纳米金的制备与表征
采用木瓜蛋白酶为功能化试剂,制备功能化纳米金。通过调整氯金酸和木瓜蛋白酶的加入比值,选

Figure 1. Chlorauric acid and citric acid three sodium and ratio spectra
图1. 氯金酸和柠檬酸三钠比例不同时的光谱图

Figure 2. Determination of nanoscale gold transmission electron microscopy
图2. 纳米金透射电子显微镜测定表征
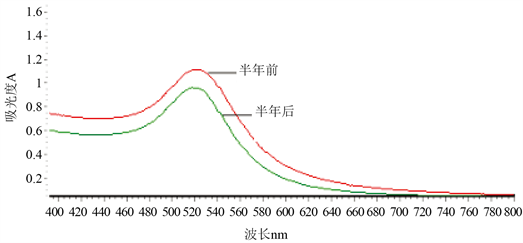
Figure 3. Stability comparison of nanoscale gold solution before and after half a year
图3. 纳米金溶液半年前后稳定性比较
择其最佳配比,用紫外可见吸收光谱表征实验结果,见图4。
由图4可以看出氯酸金与木瓜蛋白酶的比例不同,其最大吸收峰和吸光度都会发生变化,具体数据见表1。
实验结果表明,氯金酸与木瓜蛋白酶比例为1:2合成的木瓜蛋白酶-AuNPs溶液吸光度最高,为最佳比例。
透射电镜表征上述制备的功能化纳米金,结果见图5。
1:2合成的AuNPs-木瓜蛋白酶的颗粒基本呈圆形,粒度在10~20之间,尺寸分别较均匀。
4.3. 功能化纳米金测定Cu2+
4.3.1. 功能化纳米金测定铜离子的标准曲线
为了考察木瓜蛋白酶-AuNPs快速检测Cu2+离子的适用性,在上述优化条件下,在木瓜蛋白酶-AuNPs溶液中加入不同浓度Cu2+离子反应两分钟,结果发现无Cu2+离子存在时,溶液保持红色不变,随Cu2+离子浓度增加,溶液逐渐由红色变为蓝紫色。且在521 nm处的吸光度逐渐降低。体系对不同浓度Cu2+离子的响应表明,木瓜蛋白酶-AuNPs溶液在521 nm处的吸光度减去和不同浓度Cu2+离子反应后的溶液在521 nm处的吸光度即为 A521(y)与Cu2+离子浓度(x, μg∙mL−1)成良好的线性关系,标准曲线见图6。
实验结果得到,其线性方程为:y = 150.48x − 0.0514,R2 = 0.9978,线性范围0.5~25 μg∙mL−1。
4.3.2. 功能化纳米金木瓜蛋白酶测定铜离子的精确度和检出限
在同样条件下,取三份1 mL 5.0 μg∙mL−1铜溶液分别加入1 mL木瓜蛋白酶-AuNPs溶液,按照本方法进行测定,计算得出,其相对标准偏差(RSD, n = 3)为2.36%,如图7所示。

Table 1. Characteristic peaks and absorbance of different proportions of chloric acid and papain
表1. 氯酸金与木瓜蛋白酶不同比例的特征峰和吸光度

Figure 4. Spectrogram of different proportions of chloro auric acid and papain
图4. 氯金酸和木瓜蛋白酶比例不同时的光谱图

Figure 5. Functionalized nanoparticles of nanoscale papain
图5. 功能化纳米金木瓜蛋白酶的颗粒

Figure 6. Standard curve for determination of copper ion concentration by functionalized nano gold papain
图6. 功能化纳米金木瓜蛋白酶测定铜离子浓度的标准曲线
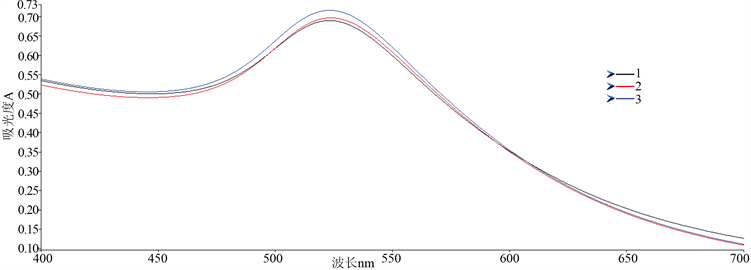
Figure 7. Spectrographic determination of the accuracy of papain AuNPs solution
图7. 木瓜蛋白酶-AuNPs溶液精确度测定光谱图
取不同浓度的铜标准溶液分别加入1 mL木瓜蛋白酶-AuNPs溶液中。经过紫外分光光度计测定,木瓜蛋白酶-AuNPs检测Cu(Ⅱ)的检出限(3 S/N)为0.3 μg∙mL−1。
4.4. 方法应用
取可疑铜污染水质的检材1 mL,加入1 mL木瓜蛋白酶-AuNPs溶液中。经紫外分光光度计测定,测得其在521 nm处的吸光度为0.7931 A,木瓜蛋白酶-AuNPs溶液在521 nm处的吸光度减去其在521 nm处的吸光度,并将其代入其线性方程为:y = 150.48x − 0.0514,R2 = 0.9978,测得其铜离子浓度为4.4 μg∙mL−1。
5. 结论
基于Cu2+离子能够引起含巯基(-SH)的木瓜蛋白酶-AuNPs溶液相互形成Cu-S键,诱导纳米金发生团聚导致溶液颜色发生变化,实现了水中Cu2+的比色检测,其检出限为0.3 μg∙mL−1;同时该方法具有简单的、成本低、效益高和快速比色法检测Cu2+离子等优点。因此,在水环境中Cu2+的检测方面具有很好的应用前景。
基金项目
江苏警官学院重点项目,项目编号:201610329004Z;江苏警官学院《物证分析新技术》创新团队2015SJYTZ02;江苏省“十三五”一级学科省重点建设学科资助项目;江苏省高校优势学科建设工程资助项目(PAPD)。