1. 引言
灵芝[Ganoderma lucidum(Leyss ex Fr)Karst]又称为赤芝、红芝,俗称瑞草、灵芝草;日本人称之为万年茸,其英文名称为Reishi mushroom。根据卯晓兰主编的《中国大型真菌》描述,灵芝属菌物界、真菌门、担子菌亚门、层菌纲、非褶菌目、灵芝科。灵芝的生活史是由成熟的担孢子离开母体开始,当遇到适宜的温、湿度、营养及空气等条件时,孢子萌发成菌丝体。当灵芝菌丝体达到生理成熟后,遇到适宜的条件,菌丝开始分化,在菌丝体表面开始出现纽结,发育成灵芝子实体原基,最后成为子实体。灵芝的开发经历了简单利用灵芝子实体到以子实体发醇菌丝体为原料提取多糖等活性成分 [1] 、发展灵芝孢子破壁技术提取孢子内涵物的过程。灵芝为担子菌纲多孔菌科灵芝属真菌。
灵芝主要药效成分为灵芝多糖(Ganoderma lucidium Polysaccharide),具有多种药理学活性功能及保健养生效果 [2] [3] [4] ,目前,对灵芝进行了有效成分、药理和临床等方面的研究,就药理作用而言,灵芝具有多种药理活性成分,其灵芝中包含了多肽、多糖、三萜类、16种氨基酸(其中含有七种人体必需氨基酸)、蛋白质、甾类、甘露醇、香豆精苷、生物碱、有机酸(主含延胡索酸)等10类药理活性成分,以及微量元素Ge、P、Fe、Ca、Mn、Zn等 [5] [6] [7] 。而且各药理活性成分在发挥保健及药理作用时各成分之间还体现有协同效应。已从它的子实体、菌丝体和孢子中分离出数十类。灵芝的菌丝体,是其营养体,它是由菌丝体的气生菌丝及分泌物共同组成的一种营养结构。菌丝呈细管状,管壁即细胞壁由葡聚糖、糖蛋白、蛋白质及几丁质微丝等成分组成。子实体灵芝的子实体,是其繁殖体,常因其粘附大量的孢子粉,而使盖面因灰褐色粉末覆盖而失去了光泽 [8] [9] [10] 。灵芝在成熟时可产生数百分子孢子,这些孢子飘散在子实体周围似一阵烟雾一样围绕着灵芝子实体,因此称为孢子粉。灵芝孢子是灵芝的种子,浓缩了灵芝的精华,具有灵芝全部遗传活性物质,药理活性成分更具多样性。在电镜下孢子大小,只有8~12*6~7 μm [11] 。由于灵芝孢子细胞壁由具有抗压、耐酸和不易酶解的几丁质、树脂和纤维素等成分组成,孢内药理活性成分难以外释,增加了人体对各有效成分的吸收利用难度 [12] [13] [14] ,因此采用热水浸提法对灵芝多糖的提取工艺条件进行研究,为灵芝多糖的开发利用提供理论资料和基础技术,它的深入研究和开发将成为中药现代化的一个典范。
2. 实验材料与设备
2.1. 实验材料
赤灵芝粉(林源珍宝参茸销售有限公司)、平盖灵芝粉(白山市名源特产有限公司)。
不同产地的不同种灵芝由于其生长环境、栽培条件的不同,会导致多糖含量的差异。
2.1.1. 主要试剂
主要试剂如表1。
2.1.2. 主要仪器
主要仪器如表2。
2.2. 实验方法
2.2.1. 灵芝多糖提取的工艺流程
灵芝多糖的提取:原料烘干至恒重→索氏提取→热水浸提并调节pH值→离心分离(常温3000 r/min,20 min),得上清液→Sevage法脱蛋白→乙醇沉淀→过滤,得沉淀物→干燥得灵芝多糖。
2.2.2. 灵芝多糖提取的操作要点
1) 原料的处理
将灵芝粉用滤纸分批包好,放进索氏提取装置中进行脱脂肪。
注:灵芝要尽量粉碎,不要留大块,以便提取完全。

Table 1. List of experimental drugs
表1. 实验药品清单

Table 2. List of experimental instruments
表2. 实验仪器清单
2) 多糖的浸提
灵芝多糖的浸提法有水浸提、碱法水解、酶解等,在此次实验中,我们通过对热水浸提法的研究选出最佳的浸提方法,在实验中用浸提率的高低为标准来衡量浸提各因素对浸提效果的影响。
在提取时要避免温度浮动,并通过不断搅拌使局部温度不会过度偏高。浓缩水提液时应尽量缩短时间,减少料液受热时间,以减少多糖分解的机会。
3) 蛋白质的去除
灵芝中的蛋白质、胶质、粗纤维及脂肪等成分不利于糖类物质析出。分离之前,必须去除蛋白质。Sevage法脱蛋白:Sevage法是利用蛋白质遇到有机溶剂会变性而不溶于水的特点分离去除蛋白的。
将上述澄清溶液中,加入用氯仿和正丁醇按4:1比例所配制成的Sevage试剂,使溶液产生絮状凝聚物在摇床上45℃下振摇30至40 min,离心1 min,然后将两相分开。再向水相中加入其体积1/3的氯仿–正丁醇,重复操作,直至无乳白色变性蛋白质析出,无凝聚物生成。
注:灵芝多糖在实际提取和应用上,对其产品和色泽无特别要求时,尽量不要去脱色。因为我们在提取多糖的同时也应注重其他有效成分的提取。
4) 醇沉
将乙醇慢慢注入脱蛋白和冷却后的浓缩液中,此时灵芝多糖呈现絮状凝胶物沉淀析出,而大部分的蛋白质和其他成分保留在溶液中,并边加边搅至完全混合均匀,静止过夜。然后过滤,得沉淀物。
2.2.3. 灵芝多糖提取条件研究
采用热水浸提法对灵芝多糖的提取工艺条件进行优化根据前人研究结果 [3] ,以多糖得率为评价指标,考察浸提比、pH值、浸提温度、乙醇浓度、浸提时间等5个因素对对灵芝多糖得率的影响,得出最佳提取条件。
1) 采用单因素试验和L18 (35)正交实验设计得出热水浸提最佳条件;
2) Sevage法脱蛋白得多糖样品。
2.3. 灵芝多糖含量测定
测定灵芝多糖含量采用3.5-二硝基水杨酸(DNS)法。取提出的灵芝多糖5 mg,加7.5 mL蒸馏水及5 mL 6 mol/L HCl溶液于50 mL的锥形瓶中,置沸水浴中加热水解30 min。待水解液冷却,定容至50 mL作为总糖测试液。另取5 mg多糖配置单糖供试液。其他操作与制作标准曲线相同。
2.3.1. 配制标准葡萄糖溶液
取一定量的葡萄糖放入烘箱中,105℃干燥至恒质量,冷却后,精确称取50 mg,定容至500 mL,即为0.1 mg/mL的标准液。
2.3.2. 配制显色剂DNS溶液
将6.3 g 3.5-二硝基水杨酸(DNS)溶于262 mL 2 mol/L NaOH溶液中,将此溶液与500 mL含有182.0 g酒石酸钾钠的热水(不超过50℃)混合,向该溶液中再加入5.0 g重蒸酚和5.0 g亚硫酸钠,充分搅拌使之溶解,待溶液冷却后,以蒸馏水稀释到1000 mL储存于棕色瓶中(在冰箱中放置1周后方可使用)。
注:3.5-二硝基水杨酸和NaOH加入的时间要很接近,或者先加入NaOH,否则将产生难容的沉淀,导致溶液配置失败。
2.3.3. 制作葡萄糖标准曲线
取6支20 mL具塞刻度试管,编好号后,按表3分别加入0.1 mg/mL葡萄糖标准溶液、蒸馏水和DNS试剂,配成不同葡萄糖含量的反应液。

Table 3. Glucose standard curve reagent table
表3. 葡萄糖标准曲线试剂表
将各管摇匀,在沸水浴中准确加热5 min,取出,冷却至室温,用蒸馏水定容至20 mL,加塞后颠倒混匀,在分光光度计上进行比色。调波长540 nm,用0号管调零,测出1~5号管的吸光度。以吸光度为纵坐标,葡萄糖含量(mg)为横坐标,绘制葡萄糖标准曲线。
2.4. 灵芝多糖提取的单因素分析方法
2.4.1. 材料预处理
分别称取灵芝粉2 g,放入编号的三角瓶中,加蒸馏水,使其组织软化,备用。
2.4.2. 不同浸提比提取灵芝多糖方法
取5个三角瓶,按表4的浸提比加蒸馏水(以干品重量计) pH 7下置于90℃恒温水浴锅中浸提2 h,3000 r/min离心20 min,弃沉淀留上清液,加入约1/3原体积的Sevage试剂,置于气浴恒温振荡器中45℃振荡30 min,取上清,再加4倍于热水浓缩后体积的95%乙醇,醇析24 h,过滤得到粗多糖。
2.4.3. 不同pH值提取灵芝多糖方法
取5个三角瓶,以1:30浸提比加蒸馏水(以干品重量计),按表4调pH值,置于90℃恒温水浴锅中浸提2 h,离心、脱蛋白、浓缩、醇析、过滤,得到粗多糖。
2.4.4. 不同浸提温度提取灵芝多糖方法
取5个三角瓶,以1:30的浸提比加蒸馏水(以干品重量计),pH 7下置于不同温度下(见表4)恒温水浴浸提2 h,离心、脱蛋白、浓缩、醇析、过滤,得到粗多糖。
2.4.5. 不同浸提时间提取灵芝多糖方法
取5个三角瓶,按1:30的浸提比(以干品重量计)、pH 7下置下90℃恒温水浴锅中浸提不同时间(见表4),离心、脱蛋白、浓缩、醇析、过滤,得到粗多糖。
2.4.6. 不同乙醇浓度提取灵芝多糖方法
取5个三角瓶,按1:30的浸提比加蒸馏水(以干品重量计),pH 7下置于90℃恒温水浴锅中浸提2 h,离心、脱蛋白、浓缩,再加4倍于浓缩后体积的不同浓度乙醇(见表4)醇析24 h,再过滤,得到粗多糖。
2.5. 正交试验方法
本实验通过对各单因素影响灵芝多糖提取效果的分析,确定正交试验的因素和水平(表5)。采用热水浸提法提取多糖,对实验结果进行极差分析,确定灵芝最佳的提取工艺。实验数据用Microsoft Excel 2007进行统计分析。

Table 4. The single factor extraction conditions of Ganoderma lucidum polysaccharides
表4. 灵芝多糖的单因素提取条件

Table 5. Extraction of Polysaccharides from Ganoderma lucidum
表5. 提取灵芝多糖因素水平
3. 结果与分析
3.1. 影响灵芝多糖提取的单因素分析
3.1.1. 计算多糖的含量及得率
将粗多糖沉淀物置于60℃干燥至恒重。按以下公式计算
式3-1
式中C1为葡萄糖含量(mg);C2为总糖含量(mg) (图1)。
式3-2
3.1.2. 不同浸提比对灵芝多糖提取的影响
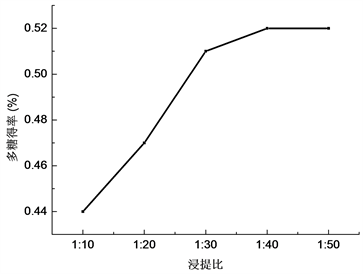
用不同的浸提比进行提取效果比较,结果见表6和图2。从图2看出随着浸提比的增加多糖得率提高,最后曲线出现一个高峰,即在1:40,这是由于当浸提比小于1:40时增加水分更有利于多糖的浸出,达到一定值之后无影响。从实验结果考虑,选取1:20,1:30,1:40三个浸提比作为正交试验浸提比的三个水平。
3.1.3. 不同pH值对灵芝多糖提取的影响
调节不同的pH值,提取灵芝多糖。从图3和表7看出,在pH 7.0时多糖得率最高,达0.41%,pH < 7.0多糖得率随着pH值升高呈上升趋势,在pH > 7.5以后,多糖得率则随pH值升高呈下降趋势。这是由于灵芝多糖大多是碱性多糖根据相似相溶原理碱性环境有利于多糖浸出,多糖提取率较高,但当碱性过强时浸提液呈粘性不利于过滤导致多糖得率降低。对比它们的多糖含量进行分析,在pH 7.0时多糖含量最高,在pH > 7.0以后,多糖含量均较高,故选取pH 6.5、7.0、7.5三值作为正交试验pH值的因素水平。
 注:图表中(1)为赤灵芝,(2)为平盖灵芝。图像分析以赤灵芝多糖例。以下同是。
注:图表中(1)为赤灵芝,(2)为平盖灵芝。图像分析以赤灵芝多糖例。以下同是。
Figure 2. The polysaccharide content of different extraction ratio
图2. 不同浸提比的多糖含量

Figure 3. Polysaccharide content of different pH values
图3. 不同pH值的多糖含量

Table 6. Effect of different extraction ratio of polysaccharide content
表6. 不同浸提比对多糖含量的影响

Table 7. Effect of different pH on the content of polysaccharide
表7. 不同pH对多糖含量的影响
3.1.4. 不同浸提温度对灵芝多糖提取的影响
温度的高低直接影响多糖提取率。以不同的温度提取灵芝多糖。由实验结果(见图4、表8)得知,浸提温度为80℃、90℃多糖量均较高,分别达0.41%、0.42%,但100℃提取率明显下降,出现此现象的原因可能是高温对多糖的结构与活性有一定的影响,100℃时多糖容易分解产生单糖而溶解在浓乙醇中进而影响多糖的提取率,从多糖含量看,90℃时所得多糖含量也较高,因此取70℃、80℃、90℃为正交试验浸提温度的三个水平。
3.1.5. 不同浸提时间对灵芝多糖提取的影响
以不同的浸提时间提取灵芝多糖,结果见图5和表9。从曲线走势看到,浸提2 h时,多糖得率高达0.62%,以后增加较为平缓,多糖提取率几乎保持不变。可能由于加热时间过长,促进多糖的溶解使得提取率增大,但是加热时间过长提取率无明显变化,因此提取时间选择由此确定1.5 h,2 h,2.5 h作为正交试验浸提时间因素的三个水平。
3.1.6. 不同乙醇浓度对灵芝多糖提取的影响
用乙醇沉淀法提取多糖时,乙醇的浓度对多糖的含量影响最大。图6、表10结果显示,低浓度的醇析效果不佳,多糖得率低,多糖含量也低,当乙醇浓度达95%时,醇析效果最好,多糖含量最高,100%乙醇时多糖含量也较高,但从经济、实验成本角度考虑,不宜选用100%乙醇,乙醇浓度为85%和90%时的多糖得率和含量都明显高于80%的提取效果。选取85%、90%、95%三个数据作为正交试验乙醇浓度因素的三个水平。
3.2. 灵芝多糖提取工艺的优化
为了提高在多因素条件下灵芝多糖的提取率,我们在单因素试验的基础上进行多因素正交试验,以优化提取工艺。结合3.2的试验结果和分析,我们采用五因素三水平L18(35)正交法进行正交试验。采用热水浸提法,提取灵芝多糖,结果见表11。
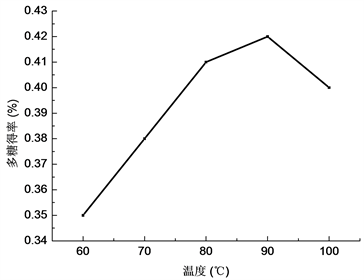
Figure 4. The content of polysaccharide in different extraction temperatures
图4. 不同浸提温度的多糖含量
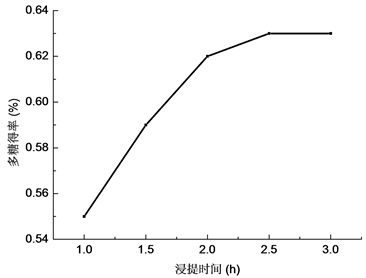
Figure 5. Polysaccharide content of different extraction times
图5. 不同浸提时间的多糖含量

Figure 6. The content of polysaccharides in different ethanol concentrations
图6. 不同乙醇浓度的多糖含量

Table 8. Influence of different extraction temperatures on polysaccharide content
表8. 不同浸提温度对多糖含量的影响

Table 9. Effect of different extraction time on polysaccharide content
表9. 不同浸提时间对多糖含量的影响

Table 10. The effect of different ethanol concentration on the content of polysaccharide
表10. 不同乙醇浓度对多糖含量的影响


Table 11. L18 (35) orthogonal test scheme and test results
表11. L18(35)正交试验方案及试验结果
注:l,2,3分别表示各因素水平;
,
,
为各因素各水平多糖含量的总和。
由正交试验结果可知,极差R愈大的因素对指标的影响愈显著,即影响灵芝多糖提取率因素大小依次是D (乙醇浓度)、C (浸提温度)、E (浸提比)、A (pH值)、B (浸取时间),其中乙醇浓度和浸提温度是主要因素,浸提时间对多糖提取的影响最小。正交试验结果显示,18组实验中,第16组灵芝多糖得率最高为0.775%,提取条件是A3B1C3D2E3,即pH 7.5,浸取时间1.5 h,浸取温度90℃,乙醇浓度90%,浸提比1:40。
4. 结论
本实验采用热水浸提法对灵芝多糖进行提取,对影响多糖得率的各种因素分析,得出最佳工艺条件为:pH 7.5,浸取温度90℃,乙醇浓度90%,浸提比1:40,浸提时间为1.5 h。最优条件下多糖提取量为0.775%。
由各因素分析表中看出,不管哪个因素影响,结果表明赤灵芝粉中多糖含量多于平盖灵芝粉中的多糖,不同产地的不同种灵芝由于其生长环境、栽培条件的不同,会导致多糖含量的差异,对于灵芝多糖的提取有待进一步的研究。
NOTES
*通讯作者。