1. 引言
猪流行性腹泻是由猪流行性腹泻病毒(Porcine Epidemic Diarrhea Virus, PEDV)引发的急性肠道传染病,1978年从比利时发病猪病料中分离病毒获得成功,毒株命名为CV777 [1] 。2010年7月,我国发现新的强毒力的PEDV毒株,并爆发一轮全国性的PED疫情 [2] [3] ,美国于2013年发现PEDV强毒株 [4] ,随后爆发了猪流行性腹泻全美大流行。
CV777毒株的全基因组序列于2001年公布 [5] ,PEDV为单链正义RNA病毒,其基因组全长约28 Kb,编码4种主要结构蛋白:纤突蛋白S、小膜蛋白E、膜蛋白M和核衣壳蛋白N。目前,GenBank已收录PEDV基因组序列431个,研究发现PEDV的变异比较快 [6] ,且临床粪便样品成分复杂,有时会影响常规单重RT-PCR检测结果的准确性,而猪群发病时能否快速、准确地检测PEDV是决定防控效果的关键因素之一。
本研究基于N和S基因,建立了检测PEDV的双重RT-PCR检测方法,有望弥补单重RT-PCR准确性欠缺的不足。
2. 材料和方法
2.1. 材料
2.1.1. 病毒材料
猪流行性腹泻病毒毒株SH-2012-5由孙涛教授实验室保存;猪的几种常见病毒病活疫苗(TGEV, PRRSV, PRV, PCV2, SEEBV, SFV)为中牧公司产品;临床哺乳仔猪粪便样本收集自上海及周边省份发病猪场。
2.1.2. 试剂
RNA抽提试剂TRIZOL LS、无RNase的DNase I为Invitrogen公司产品;反转录试剂盒为Takara公司产品;PCR扩增试剂盒ES Taq PCR mix为全式金公司产品;Gel Extraction Kit为OMEGA公司产品;Generuler 1Kb DNA Ladder为Fermentas公司产品;引物由上海生工公司合成。
2.2. 方法
2.2.1. 病毒RNA提取及cDNA制备
保存毒株及病毒样品以PBS适当稀释后,4˚C,12,000 rpm离心5 min。取上清250 μL与750 μL TRIZOL LS Reagent混合,室温放置5 min。加入200 μL三氯甲烷,剧烈振荡15 s,室温放置5 min。4˚C,12,000 rpm离心15 min。取上层无色水相500 μL与500 μL异丙醇混合,室温放置5分钟。4˚C,12,000 rpm离心8 min。弃去上清,用1 mL 75%乙醇洗涤沉淀,4˚C,7500 rpm离心5 min。弃上清,晾干3分钟,用55˚C预热的RNase free ddH2O 20 μL溶解RNA沉淀,并用无RNase的DNase I处理。
取8 μL RNA溶液(<5 μg)与1 μL随机引物、1 μL dNTPs混匀,65˚C保温5分钟后,在冰上迅速冷却数分钟。加入4 μL 5 × Prime Script II Buffer、0.5 μL RNase inhibitor、1 μL Prime Script II RTase、4.5 μL RNase free ddH2O,混匀。经30˚C 10 min、42˚C 60 min、70˚C 15 min孵育,得cDNA,−80˚C保存备用。
2.2.2. N、S基因单重RT-PCR
根据GenBank已收录的PEDV基因组序列,利用Multi-alignment软件分析,分别在N基因和S基因的保守区域设计引物,其中引物对P1:5’-ATGGCTTCTGTCAGTTTTC-3’和P2:5’- CGAAGTGGCTCTGGATTTGTT-3’ 用于N基因的RT-PCR扩增,引物对P3:5’- ATGAAGTCTTTAACCTAC-3’和P4:5’-GCAACACGGGACCAATCATT-3’用于S基因的RT-PCR扩增。优化引物设计和反应条件后,N、S基因的单重RT-PCR扩增体系均为20 μL:1 μL cDNA模板、1 μL上游引物、1 μL下游引物、10 μL ES Taq Master Mix、7 μL ddH2O;扩增程序为:95˚C 3 min;95˚C 10 s、58˚C 30 s、72˚C 45 s,30个循环;72˚C 10 min。
2.2.3. N、S基因双重RT-PCR
N/S基因双重RT-PCR的反应体系为20 μL:1 μL cDNA模板、1 μL各个引物、10 μL ES Taq Master Mix、5 μL ddH2O;优化后扩增循环为:95˚C 3 min;95˚C 10 s、58˚C 30 s、72˚C 60 s,30个循环;72˚C 10 min。
2.2.4. 特异性试验
采购几种常见猪病毒病活疫苗,病毒RNA同上抽提并进行反转录,病毒DNA按常规方法抽提。首先测试N、S基因单重RT-PCR的特异性,在单重RT-PCR表现良好特异性的基础上,再测试N/S基因双重RT-PCR的特异性。
2.2.5. 灵敏性试验
以实验室已建立的TaqMan探针荧光定量RT-qPCR定量检测毒株SH-2012-5样品,调整其cDNA浓度为1.0 × 109/μL,用灭菌ddH2O作连续10倍梯度稀释,用于单重和双重RT-PCR的灵敏度测试。
2.2.6. 双重RT-PCR检测临床样品
利用建立的双重RT-PCR检测临床发病仔猪的粪便样品。
3. 结果
3.1. N、S基因单重RT-PCR的特异性
由图1可见,针对N基因的引物对只在PEDV中扩增出800 bp左右的片段,扩增产物与预期的809 bp大小一致,进一步的测序分析确认该扩增产物为PEDV的N基因,而TGEV、PRRSV、PRV、PCV2、SEEBV和SFV的扩增结果均为阴性。针对S基因的引物对只在PEDV中扩增出550 bp左右的产物,扩增产物与预期的559 bp大小一致(图2),测序分析确认该扩增产物为PEDV的S基因,而TGEV、PRRSV、PRV、PCV2、SEEBV和SFV的扩增结果也均为阴性,上述结果表明两对引物的特异性良好。
3.2. N、S基因单重RT-PCR的灵敏性
N基因单重RT-PCR可检测1 × 104拷贝的毒株SH-2012-5的cDNA (图3)。S基因单重RT-PCR则可检测1 × 105拷贝的病毒cDNA (图4)。
 M: DNA Marker; 1~7:PEDV, TGV, PRRSV, PRV, PCV2, SEEBV and SFV, respectively
M: DNA Marker; 1~7:PEDV, TGV, PRRSV, PRV, PCV2, SEEBV and SFV, respectively
Figure 1. Specificity test of single-plex RT-PCR for N gene amplification
图1. N基因单重RT-PCR特异性试验
 M: DNA Marker; 1~7:PEDV, TGV, PRRSV, PRV, PCV2, SEEBV and SFV, respectively
M: DNA Marker; 1~7:PEDV, TGV, PRRSV, PRV, PCV2, SEEBV and SFV, respectively
Figure 2. Specificity test of single-plex RT-PCR for S gene amplification
图2. S基因单重RT-PCR特异性试验
 M:DNA Marker;1~9:109、108、107、106、105、104、103、102、101拷贝数的PEDV cDNA
M:DNA Marker;1~9:109、108、107、106、105、104、103、102、101拷贝数的PEDV cDNA
Figure 3. Sensitivity test of single-plex RT-PCR for N gene amplification
图3. N基因单重RT-PCR灵敏性试验
3.3. N、S基因双重RT-PCR的特异性
由图5可见,只有PEDV的扩增产物为两条带,且大小与单重RT-PCR的扩增产物大小一致,而TGEV、PRRSV、PRV、PCV2、SEEBV和SFV的扩增结果均为阴性。
3.4. N、S基因双重RT-PCR的灵敏性
图6显示两条特异性条带,大小分别与单重RT-PCR一致,可检测105拷贝的毒株SH-2012-5的cDNA。
3.5. 双重RT-PCR检测临床样品
利用所建立的双重RT-PCR检测10个临床样本,其中,9个样本可扩增两个特异性条带,但有1个
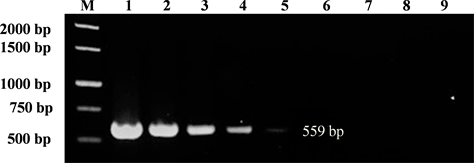 M:DNA Marker;1~9:109、108、107、106、105、104、103、102、101拷贝数的PEDV cDNA
M:DNA Marker;1~9:109、108、107、106、105、104、103、102、101拷贝数的PEDV cDNA
Figure 4. Sensitivity test of single-plex RT-PCR for S gene amplification
图4. S基因单重RT-PCR灵敏性试验
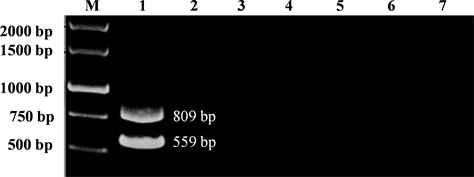 M: DNA Marker; 1~7:PEDV, TGV, PRRSV, PRV, PCV2, SEEBV and SFV, respectively
M: DNA Marker; 1~7:PEDV, TGV, PRRSV, PRV, PCV2, SEEBV and SFV, respectively
Figure 5. Specificity test of duplex RT-PCR for N/S genes amplification
图5. N/S基因双重RT-PCR特异性试验
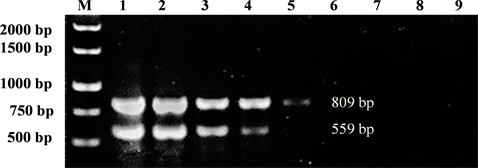 M:DNA Marker;1~9:109、108、107、106、105、104、103、102、101拷贝数的PEDV cDNA
M:DNA Marker;1~9:109、108、107、106、105、104、103、102、101拷贝数的PEDV cDNA
Figure 6. Sensitivity test of duplex RT-PCR for N/S genes amplification
图6. N/S基因双重RT-PCR灵敏性试验
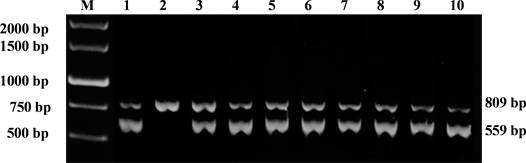 M: DNA Marker; 1~10: Clinical fecal samples
M: DNA Marker; 1~10: Clinical fecal samples
Figure 7. Clinical fecal samples detected with duplex RT-PCR
图7. 双重RT-PCR检测临床粪便样品
样品只扩增出一个条带(图7),该扩增产物测序结果证明其为PEDV的N基因。
4. 讨论
仔猪感染PEDV后,发病很急,很多仔猪因剧烈腹泻而在感染后2~3天死亡 [2] ,因此,及时、准确地确诊病原是防控该病的关键因素之一。但PEDV的变异比较快 [6] ,且临床粪便样品成分复杂,应用常规单重RT-PCR检测有时候会出现假阴性的现象,为此,本研究经引物和反应条件优化,在确认N、S基因单重RT-PCR的特异性和灵敏性基础上,建立了基于N和S基因的双重RT-PCR检测方法。从图7的临床样品检测结果也可看出,其中的2号样品仅扩增出一个条带,如果仅使用针对S基因的单重RT-PCR进行检测就会因扩增结果阴性而导致疾病误判。
资助项目
上海市科委攻关项目(课题编号:15391901600)。