1. 引言
MCPA-Na,化学名2-甲基-4-氯苯氧乙酸钠,是一种苯氧乙酸类选择性内吸传导激素型有机氯除草剂,广泛用于小麦田、玉米田、水稻田、城市草坪、麻类作物。MCPA-Na除草剂本身是中等毒性,但能在作物植株和果实上残留,虽然会在农作物及环境中缓慢消解,但仍然会引起土壤、水体和大气的污染,也会在人和动物体的脂肪中积累,因此它们的残留问题也是长期的 [1] [2] [3] [4] [5] 。研究表明MCPA-Na除草剂能够引起大鼠胃肠道、肺部和肾脏功能发生异常,引起小鼠癌症和白血病,长期接触可导致雌鼠妊娠后代发育不良,肌肉骨骼发育受阻 [6] - [11] 。
长期施用除草剂或使用不当都会引起的植物的抗药性、耐药性等问题的出现 [12] [13] ,导致除草剂施用的效果也逐渐下降,若继续加大剂量使用会造成恶性循环,加大了其进入各种生物体的可能。近年来利用微生物进行生物修复的方法越来越得到了广泛的应用 [14] [15] [16] ,微生物在繁殖和代谢的过程中,可以将土壤内残留的污染物进行分解并转化为新的无害或低害化合物,降低土壤的污染程度。因此,筛选MCPA-Na降解菌并运用其进行生物修复 [17] [18] 显得尤为重要。
本研究从长期受到污染的MCPA-Na生产车间进行土壤取样,分离出4株MCPA-Na降解菌,利用紫外分光光度法 [12] 进行了菌株生长和降解特性的研究,筛选降解效果较好的菌株,以期为MCPA-Na降解菌株的筛选和微生物在土壤修复中的应用提供理论依据。
2. 材料与方法
2.1. 样品采集及培养基的配制
土样于2016年5月取自MCPA-Na生产车间,取样时先将表层土刮去2~3 cm,每份取土样10.0 g左右,去除小石子、杂草等杂质,并将土样碾碎,注明采样地点及日期,4℃保存备用。
牛肉膏蛋白胨培养基:牛肉膏3.0 g,蛋白胨10.0 g,NaCl 5.0 g,葡萄糖10.0 g,蒸馏水1.0 L,pH 7.5。固体培养基加入2.0%琼脂,115℃高压蒸汽灭菌20 min。药品采用56% MCPA-Na可湿性粉剂。
2.2. 方法
2.2.1. 降解菌株的富集
将采集的土壤标本用土壤筛过筛后,取2.0 g加入50 mL MCPA-Na含量为0.025%的牛肉膏蛋白胨培养基中,37℃,150 r/min震荡培养3 d;然后取出1 mL加入50 mL牛肉膏蛋白胨培养基中,并提高MCPA-Na含量到0.05%,继续37℃,170 r/min振荡培养3 d。依此连续驯化12 d,至MCPA-Na终浓度为0.1%。
2.2.2. 降解菌的分离与纯化
取富集后的菌液进行浓度稀释10−1、10−2、10−3、10−4、10−5,均匀涂布在含MCPA-Na的牛肉膏蛋白胨固体培养基上,37℃恒温培养3 d,挑取单菌落划线,反复分离纯化。
2.2.3. 降解菌株的鉴定
对菌株KE-01、KE-02、KE-03、KE-04进行菌落形态观察、革兰氏染色 [19] 、芽孢染色 [19] 、电镜拍照 [20] 。对照《伯杰氏细菌鉴定手册》,对菌株进行生理生化实验。
分子鉴定:提取细菌KE-01~KE-04总DNA,将通用引物
16F:(5'–AGAGTTTGATCCTGGCTCAG–3')
1492R:(3'–TACGGCTACCTTGTTAGGACTT–5')
作为上下游引物扩增16S rDNA片段,由上海生工生物工程公司完成序列测定。将测序结果上传至NCBI进行Blast分析,利用MEGA5.0构建系统进化树。
2.2.4. 降解菌株的筛选
采用紫外分光光度法 [14] 测定菌株降解率。首先,建立MCPA-Na标准曲线,配制浓度为0、10、20、40、60、80 mg/L的MCPA-Na标准溶液,扫描190~400 nm波长范围的特征吸收值 [21] [22] ,在特征吸收波长下测定不同浓度标准溶液的吸光度(Abs),以MCPA-Na标准溶液浓度为横坐标,吸光度(Abs)为纵坐标,并绘制标准曲线。其次是对降解率的测定,取活化菌液(OD600 ≈ 0.8)接入100 mL MCPA-Na含量为0.1%的牛肉膏蛋白胨培养液中,37℃,150 r/min摇床震荡培养。于0、4、8、12、16、20、24、28、32、36、40、44、48 h分别取样,12,000 r/min离心5 min。取上清液,稀释10倍,测定其吸光度值。根据标准曲线方程计算培养基中MCPA-Na的浓度,通过对降解率进行比较来选取高效降解菌株。降解率的计算方法:
其中C0为MCPA-Na的初始浓度,C1为培养后MCPA-Na的浓度。
取活化菌液(OD600 ≈ 0.8)接入牛肉膏蛋白胨培养液,设3个重复,37℃、150 r/min摇床振荡培养。分别于培养0、4、8、12、16、20、24、28、32、36、40、44、48 h分别取样,稀释10倍后在600 nm处测定菌株的吸光度,表示菌体生物量。结合菌株降解曲线可以确定菌株降解效率与生长的关系。
2.2.5. 最优实验操作条件
将活化菌液(OD600 ≈ 0.8)按2.0%接入50 mL的液体培养基(MCPA-Na含量为0.1%)中,分别加入麦芽糖、葡萄糖、蔗糖、可溶性淀粉、乳糖作为碳源,实验浓度为3.5%~5.0%;加入蛋白胨、胰蛋白胨、酵母浸粉、尿素、KNO3作为氮源,实验浓度为0.5%~3.0%;分别加入NaCl、K2HPO4、CaCl2.2H2O、MgSO4∙7H2O、FeSO4∙7H2O、MnSO4∙H2O、FeCl3∙6H2O为培养基提供无机盐;调节pH为5~12,分别在25℃~45℃,在60~180 r/min转速下,每个处理设3个重复,测定MCPA-Na降解率。
再运用响应面法对实验操作条件优化,根据单因素实验,选取影响降解效果较大的因素作为自变量,降解率作为响应值,根据Box-Benhnken的中心组合实验设计原理进行响应面分析实验设计。应用Design Expert 8.0软件进行实验设计和结果分析,建立响应面,最后对分析结果进行验证实验。
3. 结果与讨论
3.1. MCPA-Na降解菌株的分离纯化及鉴定
经过连续富集与逐级驯化培养,从土壤样品中分离得到了6株细菌菌株,再通过复筛得到对0.1% MCPA-Na具有降解能力的4株菌株,分别标记为KE-01、KE-02、KE-03、KE-04,均能在MCPA-Na含量为0.1%的培养基中生长。
4株菌株的形态特征描述如表1所示,图1~4分别为菌落形态图、革兰氏染色、芽孢染色及电镜扫描的结果(从左到右依次为KE-01、KE-02、KE-03、KE-04)。从图2~4可以看出分离筛选的降解MCPA-Na的菌株均为杆菌。
通过形态观察和生理生化实验(见表2),可以初步确定菌株属于杆菌属,为了进一步对菌株进行鉴定,利用细菌的的16S rDNA的通用引物进行PCR扩增,得到的扩增产物如图5所示。测序成功后将菌株DNA序列与Genbank细菌基因库中序列进行比对,发现4株菌株KE-01 (Genbank登录号KY274847)、KE-02 (Genbank登录号KY274848)、KE-03 (Genbank登录号KY303833)、KE-04 (Genbank登录号KY274849)与多株芽孢杆菌属(Bacillus sp.)的相似程度较高,达到100%。根据16SrDNA序列,结合其生理生化性质可确定4株菌株均为芽孢杆菌属(Bacillus sp.)。利用MEGA5.0构建系统进化树结果见图6。

Table 1. Morphological characteristics of strain
表1. 菌株形态特征

Figure 2. Grem dyeing of the strains
图2. 革兰氏染色(1600×)

Figure 3. Spore staining of strains
图3. 菌株芽孢染色(1600×)

Figure 5. 16S rDNA amplified PCR products
图5. 16S rDNA PCR扩增产物

Table 2. Physiological and biochemical identification of strains
表2. 菌株生理生化鉴定
“+”表示阳性,“−”表示阴性。
3.2. 降解菌株的筛选
通过配制不同浓度的MCPA-Na标准溶液,利用紫外分光光度计 [14] 在特征吸收波长283 nm测定吸光度值,进行3次测量,求得平均值,以MCPA-Na标准溶液为横坐标,吸光度值为纵坐标,绘制标准曲线(如图7),得拟合方程为y = 0.0035x + 0.0022 (R2 = 0.9881)。
将菌株接入到牛肉膏蛋白胨液体培养基中培养48 h,通过对培养前后菌液吸光值与标准曲线的比对得到MCPA-Na浓度,计算4株菌株降解率,如表3所示。对比得到降解能力最强的菌株为KE-04,48 h降解率达到51.54%。MCPA-Na本身呈紫红色,加入培养基后培养基呈现橘红色,经过48 h的培养后,4瓶培养基中橘红色颜色变浅或消失。
通过对菌株KE-04生长曲线的测定,可以确定KE-04降解效率与生长的关系(见图8)。菌株KE-04较快进入对数期,其中在0 h~24 h生长较快,24 h后OD值趋于平缓,说明菌株生长受到限制。而在0 h~40 h,MCPA-Na的降解速率随底物浓度增大而加快,培养40 h后MCPA-Na的降解率为58.54%,40 h后,MCPA-Na降解变化不大,基本趋稳定,这一现象说明菌液浓度不再增加。
3.3. 最优操作条件
相同条件下,KE-04在以4.0%蔗糖为碳源、2.0%酵母浸粉为氮源、加入NaCl提供无机盐的pH为8.0的培养基中,在40℃下180 r/min震荡培养48小时测定到最大降解率,可达到63.84%。再运用响应面法进行进一步优化:
1) Box-Behnken实验
通过Plackett-Burman实验和最陡爬坡实验确定出了影响降解率的主要因素:碳源(4.0%、4.5%、5%)、氮源(1.0%、1.5%、2.0%、)、无机盐(0.04%、0.05%、0.06%)和pH (7.0、7.5、8.0),进行四因素三水平的响应面分析实验,29个实验点给出的实验结果如表4。
通过Design Expert 8.0软件对表4中Box-Behnken设计及实验结果进行回归分析,得到分析结果如表5所示。可以得出此模型F = 115.36,P < 0.0001,表明该回归模型的结果是显著的;失拟项P = 0.9098 > 0.05,说明该模型的失拟项是不显著的,因此该模型选择是正确。此外,对其进行可信度分析见表6,回归系数R2 = 0.9914,调整回归系数
= 0.9828,预测回归系数
= 0.9693,说明该模型可以解释99.14%实验操作,表明拟合度比较好。根据回归分析得到该模型的二次回归方程:
响应面实验3D图与等高线图如图9~14所示,由图可以看出模型的开口向下,实验结果存在最大值。并根据等高线图可判断,最大值落在我们的实验范围以内。
通过以上一系列分析可知,本实验的最优实验操作条件为:蔗糖(碳源)浓度为4.74%,酵母浸粉(氮源)浓度为2.34%,NaCl (无机盐)浓度为0.41%,初始pH为7.8,降解率预测值为69.64%。
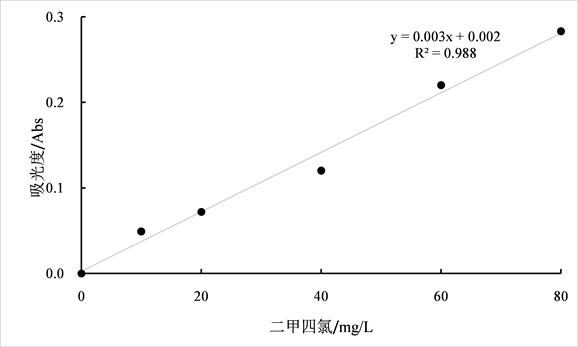
Figure 7. Standard curve of MCPA-Na
图7. MCPA-Na的标准曲线图

Figure 8. Relationship between growth and degradation rate of KE-04 strain
图8. KE-04菌株生长与降解率的关系

Table 3. Comparison of degradation rate in 48 h
表3. 菌株48 h降解率的比较

Table 4. Design and results of Box-Behnken optimization experiments
表4. Box-Behnken设计及结果

Table 5. ANOVA analysis for regression equation
表5. 回归方程的方差分析
表6. 可信度分析

Figure 9. Response surface and contour plots of the effect of carbon source and nitrogen source on degradation rate
图9. 碳源、氮源对降解率影响的3D图和等高线图

Figure 10. Response surface and contour plots of the effect of carbon source and inorganic salt on degradation rate
图10. 碳源、无机盐对降解率影响的3D图和等高线图

Figure 11. Response surface and contour plots of the effect of carbon source and pH on degradation rate
图11. 碳源、pH 对降解率影响的3D图和等高线图

Figure 12. Response surface and contour plots of the effect of nitrogen source and inorganic salt on degradation rate
图12. 氮源、无机盐对降解率影响的3D图和等高线图
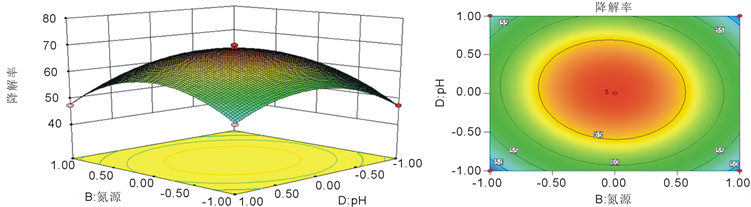
Figure 13. Response surface and contour plots of the effect of nitrogen source and pH on degradation rate
图13. 氮源、pH对降解率影响的3D图和等高线图

Figure 14. Response surface and contour plots of the effect of inorganic salt and pH on degradation rate
图14. 无机盐、pH对降解率影响的3D和等高线图
由以上操作确定的条件:蔗糖5.0%、酵母浸粉2.0%、NaCl 0.41%,初始pH 7.8,其他条件不变,重新配置培养基,设置3次重复实验,测得降解率分别为69.32%、69.74%、69.61%,平均值为69.56%,比优化前的61.26%提高了13.55%,说明此次优化获得的条件对降解率的提高是有效的。
4. 结论
1) 从土壤中筛选得到4株MCPA-Na降解菌株,经16S rDNA序列分析鉴定均为芽孢杆菌属(Bacillus sp.)。其中菌株KE-04能力较强,37℃条件下对含量0.1% MCPA-Na的降解效率可达61.26%。
2) 利用响应面法进行最优操作条件优化,最终菌株KE-04在MCPA-Na含量为0.1%的以5.0%蔗糖为碳源,2.0%的酵母浸粉为氮源,无机盐0.41%,pH为7.8的培养基中培养时降解效果最佳,可达到69.56%。
3) 之前有报道 [12] 称从湖南郴州地区长期受到MCPA-Na污染的烟田土壤中分离到1株肠杆菌属(Enterobacter sp.)细菌SE08,对MCPA-Na溶液的降解效率可达45.21%。本研究中分离得到的菌株KE-04对MCPA-Na的降解能力在实验室条件下降解效果更佳,具有潜在的应用前景。
基金项目
国家青年科学基金项目(No.31200400);山东省青年基金项目(No.ZR2013EEQ009)。