1. 引言
熊果酸(ursolic acid, UA)又名乌索酸、乌苏酸,是一种三萜类化合物,广泛存在于多种天然植物中。熊果酸具有抗炎、护肝、降血脂、抗突变、抗氧化等多种生物学活性 [1] [2] [3] ,并且作为天然的抗氧剂被广泛应用于食品、药品和保健品中。因此,从天然植物中快速、高效地提取高纯度的熊果酸具有重要意义。目前,从天然植物中获得熊果酸的方法主要采用常规的溶剂萃取和柱层析技术 [4] [5] ,这些方法存在有机溶剂消耗量很大,操作繁琐,分离效率低等问题。分子印迹技术(molecular imprinting technique, MIT)是近年来发展的一项制备具有高度选择性和亲和能力的聚合物的新型技术,在环境、食品、医药等领域得到广泛应用 [6] [7] [8] 。近来,分子印迹聚合物(molecularly imprinted polymers, MIPs)因具有特异识别性、广泛实用性和构效预定性等优点,作为一种固相萃取吸附剂也越来越多地用于复杂样品的分离纯化,实现了对目标分子及其结构类似物的选择性富集和分离。因此,本研究采用表面印迹聚合技术,以熊果酸为模板分子合成MIPs并对其特性进行研究,以期建立一种简便、快速、高效地分离纯化天然植物中熊果酸的方法。
2. 仪器与试剂
熊果酸(UA)、齐墩果酸(OA)由上海同田生物技术股份有限公司提供;、甲基丙烯酸(MAA)、乙二醇二甲基丙烯酸酯(EDMA)、偶氮二异丁腈(AIBN)均购于国药集团化学试剂有限公司;3-氨丙基三乙氧基硅烷(APTES)。MAA和EDMA使用前均经过纯化处理。甲苯、乙酸、甲醇和氯仿均为分析纯试剂。
2300Ⅱ高效液相色谱仪(大连伊利特分析仪器有限公司);SHA-C型水浴恒温振荡器(江苏省金坛市医疗仪器厂);UV-2450PC 型紫外可见分光光度计(日本岛津设备公司);KQ-250DB 型数控超声波清洗器(昆山市超声仪器有限公司)。
3. 方法
3.1. 硅胶的活化及改性
称取6 g硅胶分散于50 mL 50%的硝酸溶液中,常温静置24 h,然后用蒸馏水冲洗至中性,抽滤,60℃下干燥24 h,置于干燥器中保存备用。
取活化硅胶5 g和50 mL甲苯置于圆底烧瓶中,缓慢加入硅烷偶联剂APTES 2 mL和三乙胺1 mL,90℃下磁力搅拌回流24 h。反应后用甲醇多次洗涤,60℃下真空干燥24 h。
3.2. 熊果酸表面分子印迹聚合物的合成
称取0.1 mmol熊果酸置于6 mL甲醇中,超声溶解,加入0.4 mmol功能单体MAA和0.4 g改性硅胶,25℃恒温振荡6 h进行预组装。再加入交联剂EDMA 1.6 mmol和引发剂AIBN 20 mg,超声25 min后,通N2 30 min,密封后50℃反应48 h。反应后,减压抽滤,用甲醇/冰醋酸溶液(体积比为9:1)洗涤3次,以除去模板分子熊果酸,用丙酮冲洗,再用蒸馏水洗至中性,真空干燥即得熊果酸表面分子印迹聚合物。
非印迹聚合物(non-imprinted polymers, NIPs)的制备,除不加入模板分子熊果酸外,其它步骤同上。
3.3. 色谱条件
实验中含量测定采用HPLC,色谱柱:Hypersil BDS C 18 (4.6 mm × 200 mm, 5 μm);流动相:乙腈-甲醇−0.5%醋酸铵溶液(67:12:21);检测波长:210 nm;柱温:25℃;流速:1.0 mL·min−1。
3.4. 聚合物的静态吸附实验
精密称定MIPs 20.0 mg放入锥形瓶中,加入不同浓度的熊果酸甲醇溶液,充分混合后于25℃恒温空气振荡器内振荡12 h。高速离心沉淀,吸取上清液,用HPLC测定平衡质量浓度,NIPs按同样操作进行。平衡吸附量(Q)按公式(1)计算 [9] 。
(1)
式中:
为吸附前熊果酸的质量浓度(mg∙mL−1);
为吸附后t时间溶液中熊果酸的平衡质量浓度(mg∙mL−1);V为熊果酸溶液体积(mL);m为MIPs或NIPs的质量(g)。
3.5. 聚合物的动态吸附试验
精密称定20.0 mg MIPs和NIPs各8份于锥形瓶中,加入一定浓度的熊果酸溶液,25℃恒温空气振荡器内振荡,分别于10、30、50、70、90、110、130、150、170 min取样,离心,测定上清液中游离熊果酸的含量。
3.6. 聚合物的吸附选择性实验
分别精密称定20.0 mg MIPs和NIPs于锥形瓶中,分别加入一定量的熊果酸溶液和齐墩果酸溶液,25℃恒温空气振荡器内振荡12 h,离心,取上清液,测定游离含量。
4. 结果
4.1. 分子印迹聚合物的制备
利用硝酸活化处理硅胶颗粒,以使硅胶颗粒表面含有羟基基团。硅烷偶联剂APTES可化学键合于硅胶微粒表面,将氨基基团接枝在硅胶表面。加入的模板分子UA和功能单体MAA通过羧基与硅胶表面的氨基相互作用,在硅胶表面发生聚合反应,使聚合物层包覆在硅胶表面,洗脱模板分子后,形成表面分子印迹聚合物。
合适的模板分子-功能单体摩尔比有利于聚合物具有更好的特异识别能力和吸附特性;模板分子和功能单体在交联剂的作用下聚合形成刚性的聚合物,在选择模板分子-功能单体摩尔比时,既要使聚合物具有一定的刚性以保持良好的空间构型,又要具有一定的柔韧性以便易于接近其识别位点,从而具有良好的识别性能。当MAA用量较少时,只有少量的UA能与MAA形成稳定配合物,且部分UA仍处于游离状态,这样分子印迹中形成的与UA结构相匹配的立体孔穴的密度较低,识别位点少,结合容量低;随MAA用量的增加,UA与MAA之间形成稳定配合物的量增多,与UA结构相匹配的立体孔穴就多,吸附量变大。随着MAA与UA摩尔比的增加,MIPs的吸附量逐渐增加,当达到4:1时,吸附量达到最大;但当MAA用量过多时,聚合物的吸附性能反而下降。因此,MAA与UA的最佳摩尔比为4:1。交联剂使模板分子和功能单体聚合形成高度交联、刚性的聚合物,实验中交联剂与模板分子摩尔比为16:1时所制得的聚合物对UA的结合特性最佳。
4.2. 聚合物静态吸附实验
聚合物的静态吸附实验结果如图1所示。随着UA溶液初始质量浓度从0.1 mg∙mL−1升高到1.4 mg∙mL−1,MIPs对UA的吸附量先呈明显的增加趋势,当溶液浓度增加至1.0 mg∙mL−1后,聚合物对UA的吸附处于平衡状态。在实验浓度范围内,MIPs和NIPs对UA的最大吸附量分别27.15 mg∙mL−1和9.17 mg∙mL−1。在整个吸附过程中,随UA浓度的增大,MIPs的吸附量明显高于NIPs的吸附量。这说明MIPs对模板分子UA有明显的富集吸附的作用,具有较好的印迹效果,硅胶表面形成了能与UA分子相匹配且具有特异识别位点的三维孔穴结构,而NIPs没有形成特异性结合位点,对模板分子没有选择性,因而吸附能力差。
4.3. 聚合物动态吸附实验
为研究MIPs达到吸附平衡所需的时间和吸附速率,在不同的时间内测定了MIPs和NIPs对UA的吸附量,吸附动力学曲线见图2。MIPs对UA的吸附量在短时间内有很大的增加,随着时间的延长,吸附量增加变缓,110 min后吸附量变化趋于平缓,基本达到吸附平衡;且在任何时间段MIPs对UA的吸附量均明显高于NIPs。这说明能够与模板分子UA相互匹配且带有识别位点的三维空穴大都存在于聚合物的表面,从而可以快速地吸附目标化合物。
4.4. 聚合物吸附选择性实验
为考察MIPs对模板分子UA的特异性识别能力,实验选用模板分子UA及与其结构类似的齐墩果酸OA为底物,采用平衡吸附法测定MIPs和NIPs对底物的结合量,并通过静态吸附分配系数KD和分离因子α来表征 [10] 。
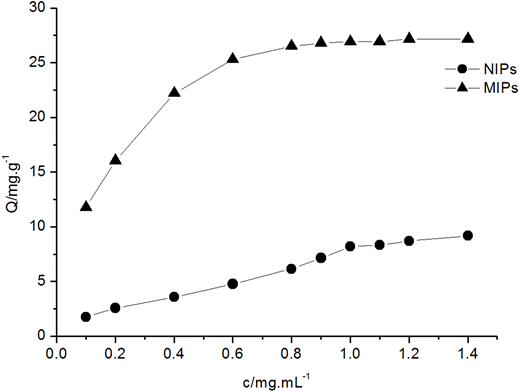
Figure 1. Adsorption isotherms of MIPs and NIPs
图1. 聚合物的吸附等温线
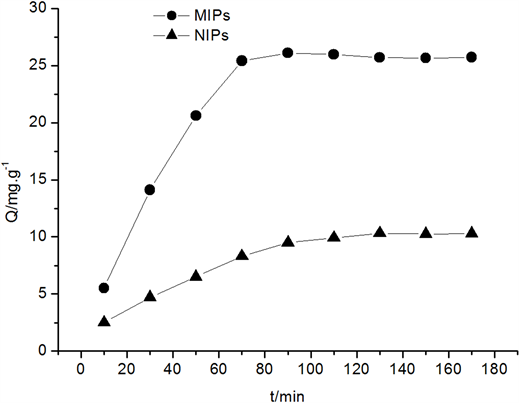
Figure 2. Adsorption dynamic curves of MIPs and NIPs
图2. 聚合物的动态吸附曲线

Table 1. The recognizing ability of MIPs and NIPs
表1. MIPs和NIPs分子识别性能
静态吸附分配系数KD定义为
式中,Cp表示底物在聚合物中的浓度,Cs表示底物在溶液中的浓度。KD越大说明MIPs对底物的吸附能力越强。
分离因子α的定义为
式中,i和j分别表示模板分子和底物,i = j时,α = 1。α越大表明MIPs对模板分子的选择专一性越好。若α < 1,则表明MIPs对底物没有选择性;若α > 1则表明,MIPs对底物有一定的选择性。
由表1可见,模板分子UA在MIPs中的KD明显大于OA的KD,说明MIPs对模板分子UA的吸附能力更强。MIPs中UA的KD明显大于NIPs中UA的KD,表明MIPs对UA分子产生了明显的印迹效应。α的数值表明MIP对模板分子UA有一定的选择性,对OA没有选择性。
5. 结论
本实验采用表面分子印迹技术,制备了熊果酸分子印迹聚合物,并考察了MIP对模板分子UA的特异性吸附作用,结果表明MIP对模板分子能产生良好的选择性和吸附作用,用于选择性分离、富集天然产物中的熊果酸是可行的。
基金项目
国家级大学生创新创业训练计划(201610439138),泰山医学院学生科研计划课题(201601006)。