1. 引言
由新型布尼亚病毒感染引起的严重发热伴血小板减少综合征(fever with thrombocytopenia syndrome, SFTS)于2007年在中国首次被发现,现已成为世界性的问题,死亡率高达6.3%~30% [1]。SFTS最常见的临床表现是发热、呕吐、腹泻、血小板减少和白细胞减少。然而,严重病例极易合并其他感染造成神经系统表现以及弥散性血管内凝血功能障碍,最终走向多器官功能衰竭 [2]。近年来,我省此病的发病例数逐年增多 [3],为此,我院对2020年收治的1例ECMO联合CRRT救治的由新型布尼亚病毒感染所致发热伴血小板减少综合征合并多重感染的重症患者的临床资料进行回顾性研究,报道如下。
2. 临床资料
2.1. 一般资料
患者男,73岁,因“发热伴头晕5天,加重并意识不清1天”于2020年8月27日收住于青岛大学附属医院神经内科,既往体健。5天前无明显诱因发热,体温最高38.5℃,伴有头晕、乏力、肌痛,2天前当地医院就诊,予以“左氧氟沙星抗感染”等治疗,1天前再次出现发热40℃,意识不清,伴有呼吸困难、腹痛、呕吐咖啡色胃内容物,以“头晕、发热原因待诊”收入神经内科。2020年8月27号查体:T:38.3℃,P:85次/分,R:20次/分,BP:135/84 mmHg。昏睡状态,双瞳孔等大等圆,对光反射灵敏,心肺腹(−),四肢肌力、肌张力正常,颈软,无抵抗,双侧巴氏征未引出。实验室检查:血常规:WBC 1.27 × 109/L,L 0.26 × 109/L,N 0.98 × 109/L (77.1%),PLT 42 × 109/L,Hb 157 g/L;PCT 0.32 ng/mL;CRP 14.29 mg/L;血凝常规:APTT 54.0 sec,FIB 1.99 g/L,D-二聚体测定7410.00 ng/ml,肝功:白蛋白31.01 g/L,AST 200.48 U/L,ALT 97.78 U/L,肿瘤标志物、抗核抗体、抗双链DNA抗体(−)肌钙蛋白、BNP(−),胸部CT:左侧腋窝淋巴结肿大,头腹部CT(−)。
2.2. 诊断与治疗
该患者于2020年8月27日入院神经内科诊断为:① 发热原因待诊;② 头晕原因待诊;③ 血小板减少;④ 凝血功能异常;⑤ 肝损害。入院后,神经内科予以米诺环素抗感染、保肝、抑酸等治疗。后意识障碍加重,由昏睡状态转为浅昏迷,血小板由42 × 109/L持续下降到27 × 109/L,合并休克、呼吸衰竭。经多学科会诊,当天转入ICU继续治疗。
2020年8月28号入ICU后,追问有虫咬病史,发热5天,伴有头晕、肌痛、乏力、腹痛,查体:T 36.6℃,P 127次/分,R 23次/分,BP 104/55 mmHg,SPO2 85%。浅昏迷,咯血痰,双肺闻及少许湿啰音,心脏腹部(−),脑膜刺激征(−)。实验室检查:血常规:WBC 2.14 × 109/L,PLT 23 × 109/L,Hb 139 g/L;PCT 0.49 ng/mL;CRP 13 mg/l;血凝常规:APTT 61.6 s,FIB 1.35 g/L,D-D二聚体5320 ng/ml;肝功:白蛋白20.58 g/L,AST 598 U/L,ALT 114.73 U/L;血气分析(高流量氧疗FIO2 100%):PH 7.37,PO2 64 mmHg,PCO2 36.2 mmHg,
20.9 mmol/L,Lac 3.4 mmol/L;心肌酶:hsTnI 1.497 ng/mL,BNP 130.50 pg/ml;胸片:双肺渗出(图1)。实验室检查提示白细胞、血小板降低、肝酶升高、D-二聚体升高,炎症指标PCT、CRP轻度升高,病程进展迅速,出现神经、呼吸、心脏、消化、血液、肝脏等多脏器受累情况,左氧氟沙星治疗无效。
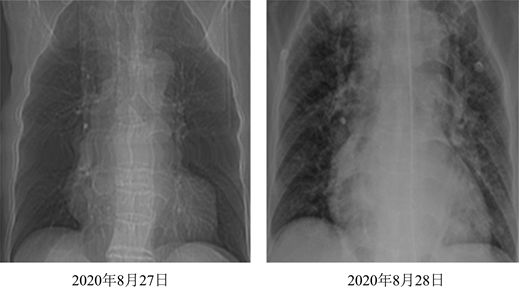
Figure 1. Changes of chest radiographs before and after admission to ICU
图1. 入ICU前后胸片变化
根据患者症状、体征以及实验室检查,考虑诊断如下:感染性疾病:① 病毒性感染:蚊虫等叮咬可传播各种病毒,如发热伴血小板减少征,出血热肾病综合征、登革热等,确诊有赖于抗体及核酸相关诊断。② 立克次体感染:可通过蜱叮咬传播。主要症状为发热全身不适、乏力、头痛、肌肉酸痛,以及恶心、呕吐、厌食、腹泻等。可伴有心、肝、肾等多脏器功能损害。③ 其他感染:细菌、真菌、结核、布鲁氏菌等,病史及相关检查不支持;非感染性疾病:血液系统肿瘤、结缔组织病、中毒等。初步考虑为发热伴血小板减少综合征,并给予利巴韦林、米诺环素、哌拉西林/他唑巴坦抗感染治疗;针对其呼吸衰竭进行气管插管机械通气,肺保护性通气,氧合指数170;通过血流动力学监测指导液体复苏对其休克状态进行纠正;考虑患者消化道出血问题,给予禁饮食、抑酸、生长抑素、并纠正凝血功能,同时进行保肝、镇静镇痛、营养支持等;继续完善相关检测:感染:NGS二代测序,痰、尿、血培养,真菌G试验,发热伴血小板减少抗体,非感染:骨髓穿刺活检、复查免疫相关检查。2020年8月31日,查体:神经系统:深昏迷,瞳孔等大,对光反射存在,病理征(−);呼吸系统:机械通气:P-A/C,PC 30 cm H2O,PEEP 18 cm H2O,FiO2 100%,监测VT 240 ml,SPO2 80%,痰液呈II度血性,双肺呼吸音粗,满布湿啰音;血气分析(纯氧):PH 7.23,PO2 56 mmHg,PCO2 59 mmHg,Lac 9.6 mmol/L;胸片双肺大量渗出表现,肺部超声:B线,双侧少量胸腔积液;循环系统:P:126次/分,BP:89/57 mmHg (NE 0.6 μg/kg∙min,肾上腺素0.4 μg/kg∙min),TNI 12 ng/ml,BNP 2387 Pg/ml,超声:EF 55% SV 50 ml,CVP 12 cmH2O,SVO2 48%;消化系统:胃肠减压血性液体,暗红色血性便;AST 1219 U/L;Hb 91 g/L;肾脏:无尿;血常规:WBC 4.46 × 109/L,L 1.58 × 109/L,PLT 160 × 109/L;血凝:APTT 71s,FIB 1.35 g/L;真菌G170 pg/ml;痰培养:白假丝酵母菌;NGS二代测序:白色念珠菌(序列数1193),发热伴血小板减少白蛉病毒(序列数38),肺炎链球菌;血培养:阴性,出血热、布鲁氏菌、流感、不典型菌、结核等(−);免疫指标(−),骨髓常规:不考虑血液病;sofa评分:16分,APACHE II评分46分,病人病情持续恶化,预计死亡率98%。
经会诊后诊断为发热伴血小板减少,对其病情进行评估,2020年8月30号病人病情最重,31号虽然病情在恶化,但实验室指标已有好转倾向(如图2),提示该患者可能已经产生了抗体或者逐渐已经进入恢复期,经过支持治疗病人将好转的可能。根据指南,该患者已符合呼吸窘迫综合征的标准,考虑行体外膜肺氧合进行治疗,遂对其病情进行评估,最终选择行V-V ECMO。后根据病人基本情况以及病原学证据调整治疗方案:因患者消化道出血,故没有抗凝;并根据NGS病毒感染结果加用利巴韦林,病人的肠道功能和全身情况比较差,出现再次感染将大大降低好转的几率,因此预防性给予泰能抗感染,以及血培养结果予以目标性抗感染治疗,2020年9月2日血培养结果中的屎肠球菌加用了万古霉素,对于痰培养的白假丝酵母菌感染,应用了卡泊芬净,同时下调了呼吸机参数,机械通气采用超保护肺通气PC模式:PC 10 cmH2O,PEEP 8 cmH2O,FIO2 40%,VT 200M;考虑其休克状态:增加氧供:DO2 = [PaO2 × 0.003 + (Hbg/dL × SaO2 × 1.3)] × CO,HB输血,SaO2 (ECMO),CO (心肺交互作用);同时通过低温和镇静降低氧耗,CRRT及其他等脏器功能支持。2020年9月8日,停用ECMO气流,氧合指数为400,顺利撤离ECMO,肺部影像学如图3所示。
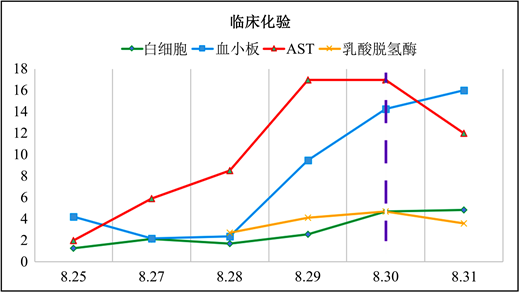
Figure 2. Trends in patient’s clinical testing
图2. 患者临床化验趋势
2020年9月9日,复查痰、血二代基因测序未发现新型布尼亚病毒遂停用利巴韦林。2020年9月10日患者意识转清,肌力2~3级,痰培养阴性,真菌G实验阴性,遂停用科赛斯。患者撤机后,血小板持续性下降,故重新评估寻找原因,进行骨髓穿刺,结果提示仍为巨核细胞增生不良导致的骨髓抑制现象,因此输注补充血小板及生血小板药物(特比澳);胆红素升高(直接胆红素为主),凝血功能逐渐趋于正常,白蛋白上升,考虑为原发病引起的肝损伤的表现,肝内胆汁淤积,给予利胆和血浆置换的对症处理;对于消化道出血仍采取禁饮食、抑酸、生长抑素、输注血小板的治疗方案;泰能抗感染:停用2天后出现发热,PCT升高4~33,故继续应用;同时采取早期康复治疗。2020年9月12日血培养阴性,停用万古霉素。2020年9月15日,消化道出血控制,恢复肠内营养。2020年9月16日,复查CT,较前好转,痰培养阴性,停用泰能。2020年9月18日,患者胆红素下降停用血浆置换治疗。2020年9月21日,血小板上升。9月22日,氧合指数350,SBT通过,脱机拔管。拔管两天后,2020年9月23发热38度,少量黄白痰,PCT 2.28→1.45 ng/ml,CRP 42→50 mg/L,WBC 7.8→4.8 × 109,真菌G 175 pg/ml,纤维支气管镜:未见明显异常,痰培养CRAB,白假丝酵母菌,复查CT较前进展,考虑鲍氏不动杆菌定植,遂加用氟康唑。9月25日,发热38.5℃,少量白痰,PCT 1.23 ng/ml,CRP 33 mg/L,WBC 14 × 109,泰能联合舒巴坦。9月29日,发热38.5℃,少量白痰PCT 0.54 ng/ml,CRP 27 mg/L,WBC 7.48 × 109,复查CT较前持续进展,氧合指数降至168,气管插管机械通气,纤维支气管镜:气道水肿,留取肺泡灌洗液NGS测序。10月2日,痰液测序结果:鲍氏不动杆菌(4784) HSV (46735),加用更昔洛韦,停用氟康唑。10月3日,尿量恢复290 ml/d。10月5日,无发热,氧合指数312,脱机拔管。10月6日,复查CT好转。10月7日,尿量870 ml/d,转入当地医院治疗。10月8日,再次高热至39度,抽搐,昏迷,气管插管后转回我院ICU,CRP 150 mg/L,PCT 11.3 ng/ml,脑脊液及颅脑CT阴性,不排除股静脉导管相关感染,更换股导管,继续阿昔洛韦、泰能、替加环素抗感染。10月10日,意识转清,脱机拔管。10月15日,连续3天无发热反复培养阴性,停用泰能、替加环素。10月21日,停用阿昔洛韦(21天)。10月23日,肾功能完全恢复,出院。

Figure 3. Pulmonary imaging changes after treatment
图3. 治疗后病人肺部影像学变化
3. 讨论
SFTS是由发热伴血小板减少病毒(severe fever with thrombocytopenia syndrome virus, SFTSV)感染所致的一种新发传染病,SFTS于2009年在中国首次报道,并迅速蔓延至中部、东部和东北部地区的其他省份 [1]。2012年,日本22例 [4] 和韩国23例 [5] 也报道了SFTS病例。中国SFTSV感染的总死亡率约为7.3% (2391例,174例死亡),在各种研究中从6.3%到30.0%不等 [3] [6]。SFTSV是一种RNA病毒,属于白蛉病毒属,可通过蜱虫叮咬传播,也可以通过接触SFTS患者的体液传播。SFTS多在春季和夏季发病,自然感染多见于牛、犬、羊等脊椎动物和长角血蜱等节肢动物 [7]。该病的发病年龄集中于40~80岁,在老年患者中病情易加重,病死率高 [8]。该病临床表现无明显特异性,常为急性起病,有发热伴恶心、呕吐、腹痛、腹泻等症状,可伴有呼吸系统、胃肠道症状和神经症状,严重者可发展至多器官功能衰竭。该病因早期的临床症状与斑疹伤寒、肾综合征出血热等疾病相似,极易被误诊。该患者转入ICU后追问有虫咬病史,考虑其为主要感染方式。
SFTS典型的感染过程有四个不同的时期:潜伏期、发热期、多器官衰竭和康复期。蜱虫叮咬后的潜伏期通常为5~14天 [9],潜伏时间可能受到多种因素的影响,包括病毒载量和感染途径,从接触或暴露于感染患者的血液或血性分泌物发病的平均时间约为10天 [10];发热期与流感症状类似,如突发高热(体温38℃~41℃),持续5~11天,头痛、乏力、肌痛以及食欲不振、恶心、呕吐和腹泻等胃肠道症状,同时伴有血小板、白细胞减少和淋巴结肿大。此期可检测到高载量的病毒,是临床诊断的重要标志 [11];多器官衰竭期的特征表现为死亡病例中器官衰竭的进行性恶化或康复患者的自限性恢复过程。多器官衰竭进展迅速,常首先在肝脏和心脏,而后进展到肺脏和肾脏。此期在大多数情况下发生在发病后约5天,持续7~14天。病情发展至此阶段,血清的病毒载量在幸存者中逐渐下降,但在死亡患者中仍然很高。该阶段重要的生物标志物(包括天冬氨酸氨基转移酶、肌酸激酶、乳酸脱氢酶和肌酸激酶同工酶)的浓度在死亡病例中明显高于康复病例 [12]。此期临床症状包括出凝血和神经系统症状、弥散性血管内凝血、多器官衰竭和持续性血小板减少,皆为死亡的主要危险因素。有病理研究表明,高病死率背后的机制即是与细胞炎症因子风暴相关的病毒感染相关性噬血细胞综合征,由弥散性血管内凝血导致的凝血功能障碍,以及多器官衰竭 [13]。因此,SFTS此阶段对于患者的病情进展至关重要,在此期幸存的患者可从逐渐恢复。
分析该患者各项检查指标可见,2020年8月30号病人病情最重,31号虽然病情在恶化,但实验室指标已有好转倾向,提示该患者可能已经产生了抗体或者逐渐已经进入恢复期,经过支持治疗病人将有好转的可能。根据指南,该患者已符合呼吸窘迫综合征的标准,考虑行体外膜肺氧合(ECMO)进行治疗。遂对其进行评估,该患者同时有呼吸系统的衰竭以及严重的循环系统的衰竭,且对于脓毒症休克的病人来说,血管活性药物使用的指数已达到行V-A ECMO的标准,行V-V或V-A均可,但考虑到:呼吸机会产生应力应变的作用,可能是导致病人出现心功能问题如心排量下降的原因,适当的减低呼吸机参数后,尽管氧合在下降,病人血压和每搏量有明显改善,通过行V-V ECMO降低呼吸机的参数来改善病人的循环是可行的。后续经过一系列出凝血方案的调整,抗感染治疗,以及呼吸辅助治疗,该患者顺利脱机,最终恢复出院。疫情期间,ECMO作为一种体外生命支持手段于大众已不再陌生,而ECMO用于治疗重症发热伴血小板减少所致器官衰竭的病例鲜有报道。本例报道中患者因重症SFTSV感染已出现脓毒症休克以及多器官功能衰竭,通过及时评估,行ECMO为患者的后续治疗提供了强有力的支持。
据国内外报道,近年来该病已成为威胁公众健康的重大风险 [14] [15]。该病毒可能通过蜱载体和脊椎动物宿主的基因突变、重组和同源重组进行快速进化。目前尚无针对SFTSV的特异性治疗药物,避免蜱虫叮咬是预防其感染和传播的重要措施,同时我们要依赖于SFTSV的早期快速检测技术来对疾病进行预防和控制,做到有效预防、及时发现、及时治疗,降低重症患者的病死率。而对于合并器官功能衰竭的SFTS患者,在严格的评估下,ECMO作为有效的支持治疗手段可为患者后续的抗感染治疗争取时间。
NOTES
*通讯作者Email: xingjy@qduhospital.cn