1. 引言
随着现代工业的迅猛发展,重金属离子对水体的污染越来越严重。被重金属污染的水体存在持久危害性,且随着污染物的迁移转化,重金属容易在人体中积累,并导致蛋白质代谢中断,对人类以及水中生物的生存构成严重的威胁 [1] [2]。因此,寻找经济有效去除废水中重金属离子的方法十分重要。目前,对于水中重金属离子的去除有以下方法:化学沉淀法 [2] [3],离子交换法 [4],吸附法 [5] [6],膜过滤法 [7],电化学处理技术 [8],混凝和絮凝法 [9] [10] 等。其中吸附法操作简单且经济高效,是一种应用普遍的处理技术。
累托石因其特殊的层状硅酸盐结构 [11],具有较大的表面积和高的阳离子交换容量,在去除重金属离子方面具有潜在的应用前景 [12] [13]。国内外专家对累托石的吸附已做了大量研究工作。李东等 [14] 研究了累托石对于Ni2+的吸附,通过实验探讨了不同因素吸附效果的影响,且环境中pH有较大影响,并表明累托石可以作为良好的吸附材料。Wang等 [15] 在累托石表面制备碳层,再与三磷酸三钠反应后,再研究改性后的累托石对Pb(II)、Cu(II)等金属离子的吸附,发现在低痕量Pb(II)浓度下去除率能达到90%,且对Pb(II)的吸附效果优于其他重金属离子。
本文采用累托石做吸附剂,以Pb(II)为处理对象,通过单因素条件试验探究累托石对水中Pb(II)的吸附效果,以期为累托石去除水中重金属离子提供依据。
2. 材料及方法
2.1. 试剂及仪器
本试验所采用的累托石购于湖北名流累托石科技股份有限公司,化学组成及性质参见文献 [13] 其化学组成如表1所示:

Table 1. The chemical compositions of rectorite
表1. 累托石的化学组成
含铅模拟废水由硝酸铅配制而成。
仪器:紫外可见分光光度计(UV290型,上海舜宇恒平科学仪器有限公司);恒温振荡器(SHZ-C,上海跃进医疗器械厂);高速离心机(TDL-5-A,上海安亭科学仪器厂);超声波清洗机(SB-3200DT,宁波新芝生物科技股份有限公司);电子天平(FA2004N,上海菁海仪器有限公司)。
2.2. 吸附实验
将0.5 g的累托石放入装有100 mL模拟废水(100 mg·L−1)的平底烧瓶(250 mL)中。在25℃条件下恒温振荡,振荡速度为180 r·min−1,定时取样,用0.45 μm的滤膜过滤后,测定铅离子浓度。
2.3. 标准曲线的绘制
二甲酚橙分光光度法测铅
1) 二甲酚橙溶液(0.2 g·L−1):称取0.1 g二甲酚橙四钠盐加入100 mL容量瓶中(1 g·L−1),取10 mL稀释至50 mL。
2) 铅标准储备液(1 g·L−1):称取1.599 g硝酸铅溶液溶于(1 + 9)硝酸溶液中,再稀释至1000 mL。
3) HAc-NaAc溶液(pH = 6):54.6 g醋酸钠加1 mol·L−1醋酸溶液20 mL溶解,加水至500 mL。
测定:分别加入0、0.5、1、1.5、2、3 mL硝酸铅溶液于10 mL比色管中,再加入1 mL HAc-NaAc缓冲溶液,0.5 mL二甲酚橙溶液,稀释至刻度,在575 nm波长处测定。所得标准曲线如图1。

Figure 1. The standard curve line of Pb(II)
图1. 铅离子标准曲线

Figure 2. Effect of adsorption time on rectorite adsorption Pb(II)
图2. 吸附时间对累托石吸附Pb(II)的影响
3. 结果与分析
3.1. 吸附时间对Pb(II)去除率的影响
以累托石为吸附剂,对硝酸铅溶液进行静态吸附实验。室温条件下,当初始浓度50 mg·L−1时,选取累托石用量3 g·L−1,考察溶液的吸附过程。累托石吸附Pb(II)的时间的关系如图2所示。
从图2可以看出,室温下累托石对Pb(II)有较好的吸附能力。在反应的前10 min Pb(II)被累托石迅速吸附,继续延长吸附时间,去除率增幅不大。吸附时间为40 min,去除率为29.4%。
3.2. 铅离子浓度对Pb(II)去除率的影响
铅离子初始浓度对吸附有较大影响。铅离子初始浓度分别为25、50、100、150、200 mg·L−1,累托石用量3 g·L−1,吸附时间40 min,室温条件下,考察铅离子浓度对累托石吸附效果的影响。结果如图3所示。
由图3曲线可以看出,累托石对Pb(II)的吸附量随Pb(II)初始浓度的增大而增加,但去除率随着浓度增加先上升,较高浓度之后趋于稳定。这主要是因为初始浓度增加时,铅离子物质的量增大,吸附量也在增大。但是累托石吸附位点是一定的,只能吸附定量的铅离子,因此当浓度较高时,Pb(II)去除率无法有效提高。因此选取了100 mg·L−1作为最佳浓度,此时去除率达到42.6%。
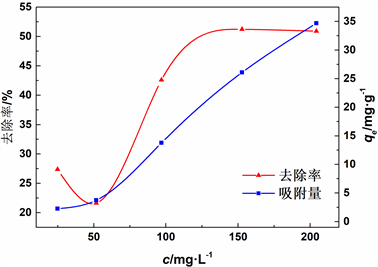
Figure 3. Effect of lead ion concentration on rectorite adsorption Pb(II)
图3. 铅离子浓度对累托石吸附Pb(II)的影响

Figure 4. Effect of the rectorite amount on the adsorption of Pb(II)
图4. 累托石用量对吸附Pb(II)的影响
3.3. 累托石投加量对Pb(II)去除率的影响
吸附剂的投加量是影响污染物去除率的重要因素。铅离子初始浓度为100 mg·L−1时,分别选取吸附剂用量 2~7 g·L−1,吸附时间为40 min,室温下,考察吸附剂用量对铅离子去除率的影响。结果如图4所示。
由图4可以看出,随着累托石投加量的增加,提供的有效吸附活性位点的总量也在增大,因而会有更多的可交换的表面吸附位与Pb(II)形成络合物 [16],相应地提高了溶液中Pb(II)的去除率。在较低的投加量条件下,各种表面官能团完全暴露,表面官能团达到饱和速度快,吸附容量高。从图4也可以看出,随着投加量的增加,累托石对Pb(II)的吸附容量逐渐降低。这是由于吸附剂投加量过大,会造成颗粒之间相互碰撞的机率增大,从而使颗粒更容易聚集。综合考虑去除率及吸附量,选取累托石用量为5.0 g·L−1,此时去除率达62.12%。
3.4. 温度对吸附效果的影响
当硝酸铅溶液初始浓度为100 mg·L−1时,吸附剂用量5 g·L−1,吸附时间为40 min时分别考察了15℃、25℃、35℃、45℃、55℃、65℃温度下,累托石对铅离子的吸附效果,结果如图5所示。
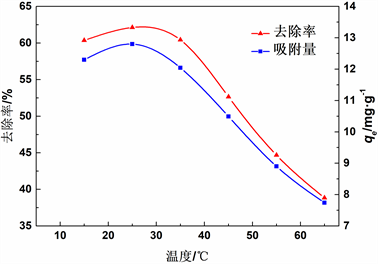
Figure 5. Effect of temperature on rectorite adsorption of Pb(II)
图5. 温度对累托石吸附Pb(II)的影响
图5表明随着反应体系温度的增加,吸附剂的吸附量呈现减小的趋势。这说明累托石对于Pb(II)的吸附是一个放热过程,较低温度有利于累托石对于Pb(II)的吸附。温度过高会使吸附剂的吸附能力降低。累托石吸附金属离子之后螯合形成的配位化合物不稳定,温度升高会使配合物再次脱离,导致吸附量降低 [17]。由图可看出在15℃~30℃范围内累托石对Pb(II)的去除率变化不大,因此反应温度定设为常温。
3.5. 吸附等温线
配制100 mL初始浓度分别为100,150,200,300,400和500 mg·L−1的硝酸铅溶液,分别加入0.5 g累托石,在不改变溶液初始pH条件下测定298 K时累托石对Pb(II)的等温吸附曲线,所得实验数据用Langmuir,Freundlich和Temkin模型进行拟合,得到Langmuir,Freundlich和Temkin等温吸附方程的相关参数如表2所示,拟合结果如图6所示。

Table 2. Adsorption isotherm parameters of Langmuir, Freundlich and Temkin models
表2. Langmuir,Freundlich和Temkin模型的吸附等温线参数
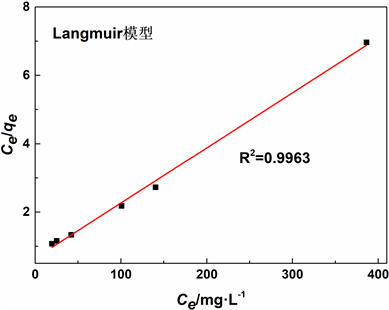
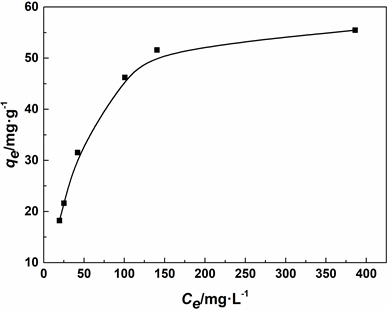
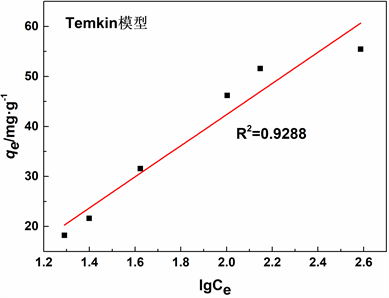

Figure 6. Adsorption isotherm model fitting of Pb(II) by rectorite
图6. 累托石对Pb(II)的吸附等温线模型拟合
如表2和图6所示,随着溶液Pb(II)浓度的增加,累托石对Pb(II)的吸附容量增加。在初始阶段,累托石对Pb(II)的吸附量增加较快,表明此时吸附剂表面吸附位点数量较多,有利于REC吸附Pb(II)。而随着浓度的增加受到吸附位点的限制,吸附量缓慢增长。
累托石吸附Pb(II)的Langmuir模型的R2 (0.9963)高于Freundlich模型R2 (0.8728),以及Temkin模型R2 (0.9288),表明Langmuir吸附等温线模型能更好的描述累托石对Pb(II)的吸附机理,说明累托石对Pb(II)的吸附主要为单分子层吸附。
用Langmuir吸附等温线模型拟合累托石吸附MB在298 K温度条件下的最大吸附量qm为62.03 mg·g−1。
3.6. 吸附动力学
为了研究传质和化学反应等吸附过程的控制机理,采用了3种动力学模型(即准一级动力学模型、准二级动力学模型、内扩散动力学模型)对三个不同浓度下的实验数据进行拟合。
配制初始浓度分别为50 mg·L−1,100 mg·L−1和200 mg·L−1的硝酸铅溶液,向其中分别加入5 g·L−1累托石,恒温振荡,每隔一定时间取5 mL上清液过滤后测定吸光度。根据吸光度算出t时刻吸附量和平衡时刻吸附量,进行动力学方程拟合。拟合得到准一级动力学、准二级动力学和粒子内扩散动力学方程的相关参数见表3,拟合曲线如图7所示。

Table 3. Adsorption kinetic model fitting parameters
表3. 吸附动力学模型拟合参数
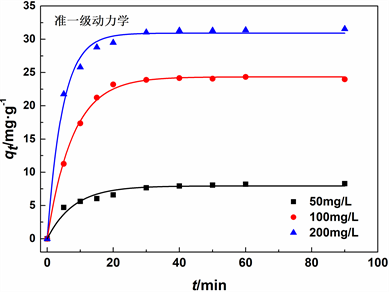
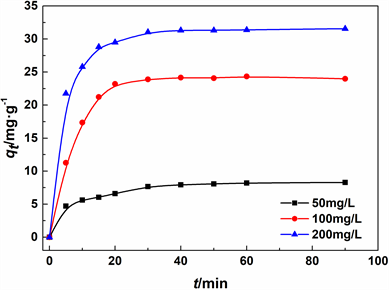
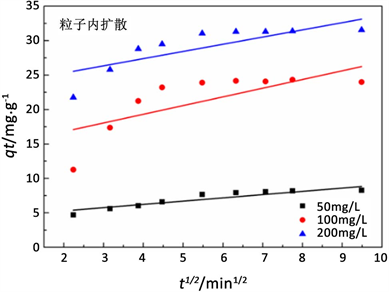

Figure 7. Adsorption kinetic model fitting
图7. 吸附动力学模型拟合
吸附时间对吸附过程有一定的影响。在开始30 min内,累托石对Pb(II)的吸附容量增长迅速,吸附速度随着吸附时间的增加明显变缓,该反应在30 min之后渐渐趋于稳定。累托石的吸附过程可分为增加和平衡2个部分,刚开始发生吸附时,累托石的表面存在大量的吸附位点,溶液中重金属的浓度较高,吸附量相对比较大。随着吸附时间的延长,吸附位点逐渐减少导致吸附速率变慢,随后达到吸附平衡。到了平衡的阶段,吸附位点的减少导致吸附过程变得缓慢,吸附能力逐渐达到饱和。
根据拟合计算出的单位吸附量qe,准一级动力学模型下对Pb(II)分别为7.93、24.34、30.91 mg·g−1;准二级动力学模型下对Pb(II)分别为8.65、25.06、32.15 mg·g−1;对比来看,试验qe,exp的值(8.57, 24.33, 31.56 mg·g−1)与来自准二级动力学模型的计算的qe,cal值一致,准二级吸附动力学模型能够更好的描述REC对Pb(II)的吸附过程和行为。此外,准二级动力学模型的R2较准一级动力学模型的R2更接近1,在整个研究范围内,对于不同的初始浓度,准二级动力学模型与累托石吸附Pb(II)的动力学行为非常吻合。因此,累托石对Pb(II)的去除过程是化学吸附为主导,该吸附过程与累托石表面的活性位点和吸附质之间的离子交换、表面沉淀有关。
4. 结论
1) 累托石可有效去除水中的Pb(II),对于硝酸铅溶液,最佳的吸附条件为:Pb(II)浓度为100 mg·L−1,累托石投加量5 g·L−1,反应温度25℃,吸附反应时间40 min达到平衡,去除率为62.12%。
2) 吸附等温线模型拟合表明累托石吸附Pb(II)符合Langmuir吸附等温线模型,累托石对Pb(II)的吸附主要为单分子层吸附。
3) 吸附动力学模型拟合表明累托石吸附Pb(II)更符合准二级动力学模型,表明累托石对Pb(II)的去除过程是化学吸附为主导。