1. 引言
聚合硫酸铁(Polymeric Ferric Sulfate, PFS)是一种新型、优质、高效的铁盐类无机高分子絮凝剂,具备混凝性能优良,矾花密实,沉降速度很快等特点。PFS比表面积大、吸附性强,能有效地去除水体中的悬浮物、有机质和部分重金属离子、放射性物质及致癌物等,具备良好的脱色、除臭等功能。同时由于生产成本低、相较铝盐系无机絮凝剂净化过程投加量少、适用pH范围广、杂质少、COD去除率高、残留物浓度低、矾花大且沉降速度快、脱色效果好等特点,所以近年来发展很快,正在逐步取代碱式硫酸铝等无机絮凝剂 [1]。因此PFS被广泛应用于生活饮用水、工业用水、各种工业废水、城市生活污水、污泥脱水等的净化处理 [2]。相比传统的铝系絮凝剂而言,PFS在反应过程中无离子水相转移和残留积累,即使是液体产品,也有着使用更方便、价格更便宜、用量更省的特点 [3]。与此同时,PFS在制备过程中能与多种金属离子以及非金属离子结合,具有良好的改性前景。
我国国内对优化直接氧化法制备PFS的制备条件的探究使用的分析方法一般为单因素试验分析法和正交实验法。目前国内学者普遍对PFS的改性进行了大量的研究。主要分为无机改性与有机或生物改性和复合式改性 [4]。韩晓燕等 [5] 在制备PFS时引入
,并采用碱化法制备出新型无机高分子絮凝剂聚合磷硫酸铁(PPFS)。并通过正交实验法探究其优化制备条件和水处理效果。Wei Chen [6] 提出物理化学法改性,其中以钛离子为例,讨论了物理化学法改性的优缺点。
聚合硫酸铁除了运用于地表污水常规指标处理之外,近年来专家学者也开始将其运用于水中重金属的处理探究,崔金利等 [7] 通过使用PFS处理含砷地下水,探究了聚合硫酸铁处理重金属的机理等。
近年来,响应面分析法被广泛运用于多变量生物、化学试验的试验条件优化上。因其良好的应用前景在各界受到大力关注。H2O2直接氧化法是目前制备PFS的主流方法之一,具有工艺简单、生产设备简易、生产周期短、单次投入低、产品质量良好等特点,相较于其他制备方法有着明显的优势。因此具备良好的工业前景。目前尚未有关运用响应面分析法探究优化PFS制备条件的相关报道。
因此本文通过响应面分析软件对直接氧化法制备PFS的三大因素的单因素探究试验的试验结果设计试验;对设计试验数据作进一步统计分析并建立模型,以期得到直接氧化法制备PFS的优化条件。本文可以为未来的相关研究提供参考。
2. 材料与方法
2.1. 试验材料
2.1.2. 试验原料
七水合硫酸亚铁晶体。
2.1.2. 试验试剂材料与仪器
工业级过氧化氢溶液、硫酸、盐酸、磷酸、氯化汞、氯化亚锡、二苯胺磺酸钠、酚酞、高锰酸钾、氢氧化钠、硫酸亚铁铵、钼酸铵、硫酸银、邻菲罗啉、硫酸汞、氟化钾、重铬酸钾;分析纯;洗涤剂。
多头磁力搅拌器(HJ-6型金坛市中大仪器厂),数显不锈钢干燥箱(DGX-9053B-2上海浦东荣丰科学仪器有限公司),分析天平(ME104E梅特勒–托利多仪器(上海)有限公司)
2.2. PFS盐基度对模拟废水COD及浊度去除率的影响
配制COD为500 mg/L、0.1 g/L的高岭土悬浊液模拟废水。分别取1 L模拟废水置于六联搅拌器的6个大烧杯中,根据《水处理剂聚合硫酸铁》(GB/T 14591-2016),选取盐基度范围为[8%, 16%],然后按不同梯度加入500 mg盐基度的聚合硫酸铁,开动搅拌器以250 r/min的转速搅拌1 min,再以30 r/min的转速搅拌10 min,静置30 min,然后取液面下6 cm处的水样测定其COD和SS。
2.3. 单因素试验方法及测定原理
2.3.1. 试验方法
通过改变n(H2SO4):n(FeSO4)、n(H2O2):n(FeSO4)和熟化温度T,以盐基度[采用《水处理剂聚合硫酸铁》(GB/T 14591-2016)]中盐基度的测定方法]作为主要表征参数,全铁含量以及还原性物质含量为质量保证参数,探究出双氧水氧化硫酸亚铁的优化工艺条件。
2.3.2. 全铁含量的测定原理
根据《水处理剂 聚合硫酸铁》(GB/T 14591-2016) [8],选用重铬酸钾法进行全铁含量的测定,原理:在酸性溶液中,用氯化亚锡将三价铁还原为二价铁,过量的氯化亚锡用氯化汞去除,最后用重铬酸钾标准滴定液进行滴定。
反应方程式为:
(1)
(2)
(3)
2.3.3还原性物质(以Fe2+计)含量的测定原理
在酸性溶液中用高锰酸钾标准滴定溶液滴定。
反应方程式为:
(4)
2.3.4. 盐基度的测定原理
在试样中加入定量盐酸溶液,再加氟化钾掩蔽铁,以酚酞为指示剂或以pH计指示终点,用氢氧化钠标准滴定溶液滴定、至溶液变为淡红色或pH为8.3即为终点。
2.4. 响应面分析法设计并输出最佳试验条件
将以上试验所得的三因素最佳试验区间的高值和低值分别输入Box-Behnken Design响应面分析法模型中,输出设计优化试验数值。根据响应面分析法设计试验并进行试验。随后将所得试验数据输入相应模型,软件输出最佳制备条件,随后验证 [8]。
2.5. 硫酸絮凝剂混凝效果比较
将本文最终条件制得的PFS与市面上在售商品一同对模拟废水进行处理,并对比处理效果。
3. 结果与讨论
3.1. 聚铁盐基度对模拟废水COD及SS去除率的影响结果
由表1和图1试验试验数据可知,盐基度在《水处理剂聚合硫酸铁》(GB/T 14591-2016)一等品要求区间内,对废水中的COD及SS的去除率影响为:随着盐基度上升,去除率呈先增大后减小的趋势。当盐基度为12%时,去除率最高,处理效果最好,因此以下试验将在其他主要因素达标的情况下使产品盐基度趋向于12%。

Table 1. Effect of salt base degree on COD and SS removal rate of simulated wastewater
表1. 盐基度对模拟废水COD及SS去除率的影响

Figure 1. Effect of salt base degree on COD and SS removal rate of simulated wastewater
图1. 盐基度对模拟废水COD以及SS去除率的影响
3.2. 单因素试验结果
从表2和图2中可看出随着硫酸投加量的增大,全铁含量逐渐降低,同时还原性物质含量快速下降,在n (硫酸亚铁):n (硫酸)达到1:0.25时,还原性物质的质量分数为0.0002%。降低至国家一等品标准,盐基度呈现下降的趋势。为确保在样品合格的同时,硫酸用量达到最优化条件,暂时界定n(FeSO4):n(H2SO4)、区间应取为[1:0.2, 1:0.3],同时取硫酸与硫酸亚铁投加比为1:0.25进行双氧水与硫酸亚铁投入比区间试验。

Table 2. Sulfuric acid and ferrous sulfate injection ratio interval test results
表2. 硫酸与硫酸亚铁投加比区间试验结果

Figure 2. Sulfuric acid and ferrous sulfate cast ratio interval test
图2. 硫酸与硫酸亚铁投加比区间试验

Table 3. Test results of the ratio of ferrous sulfate to hydrogen peroxide input ratio
表3. 硫酸亚铁与双氧水投入比区间试验结果
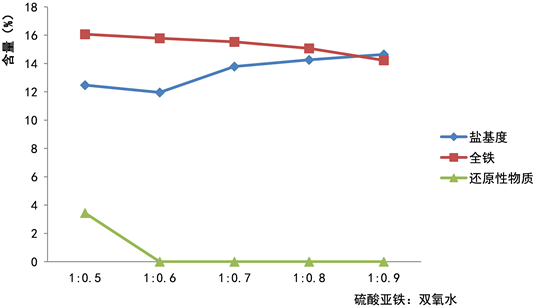
Figure 3. Experiment of the input ratio between hydrogen peroxide and ferrous sulfate
图3. 双氧水与硫酸亚铁投入比区间试验
图3和表3中所有样品的全铁含量及盐基度都能达到《水处理剂聚合硫酸铁》(GB/T 14591-2016)一等品要求。样品1还原性物质含量不合格,其他样品符合国家标准一等品标准。双氧水投加量增大时,样品全铁含量逐渐下降;排除样品1中还原性物质含量的干扰之后,盐基度随双氧水投加量的增大而增大;当硫酸亚铁与双氧水投加比为1:0.6时,还原性物质含量已趋近于零。为确保在样品合格的同时,双氧水用量达到最优化条件,暂时界定n(FeSO4):n(H2O2)区间应取为[1:0.5, 1:0.7],则取七水合硫酸亚铁与双氧水投加比为1:0.6进行熟化温度区间试验。

Table 4. Curing temperature range test results
表4. 熟化温度区间试验结果

Figure 4. Curing temperature range test
图4. 熟化温度区间试验
根据图4和表4,可以直观看出,熟化温度区间中试验所有样品全铁含量和还原性物质含量达到国家标准一等品标准。样品4的盐基度含量高于国家一等品标准,其余样品盐基度满足国家标准一等品标准。随着温度的升高,全铁含量逐渐变大,还原性物质含量也随之增大,盐基度则呈先升高后降低的趋势。造成以上变化的原因是随着温度逐渐升高,反应过程结束后溶液体积会有些许变化,全铁含量以及还原性物质含量随体积而改变。盐基度的变化则是由于直接氧化法制备PFS最后的聚合反应是吸热反应,适当保持温度将有利于其聚合反应的正向进行从而使得盐基度达标。但当温度高于65℃之后盐基度呈下降趋势。其原因在于过高的温度会破坏已经完成聚合反应的阳聚离子与羟基架桥形成的多核络离子之间的结构,造成产物分解,使样品聚合度下降,盐基度降低。由此,样品熟化温度(T)的区间为[55, 65]℃。
综合以上三个单因素试验,样品中全铁含量的大小取决于硫酸亚铁的投入量的多少以及样品溶液体积的大小,硫酸亚铁投加量越大,样品中的全铁含量越高;样品溶液体积越大,样品全铁含量越低。试样中的还原性物质含量受双氧水加入量以及溶液体积的影响。随着双氧水加入量增大,还原性物质含量逐渐降低并趋近于零;双氧水加入量一致时,溶液体积越小还原性物质含量越高。盐基度则由多个复杂因素相互影响而确定。
3.3. 响应面分析法优化工艺条件结果
利用单因素试验提供的信息,根据模型的中心组合试验设计原理,选取PFS样品的盐基度为响应指标,以Y表示,选取n(H2SO4):n(FeSO4)、n(H2O2):n(FeSO4)以及样品熟化温度(T)等3个因素,并分别以A、B、C表示,分别取设计区间为[0.2:1, 0.3:1]、[0.5:1, 0.7:1]、[55, 65]℃进行响应面分析法中试验设计,并进行试验。设计参数及结果如表5。
使用Design Expert8.06中的Box-Behnken模型对试验响应值Y (盐基度)进行二次回归分析,三因子对响应值的影响可用以下回归方程表示:
式中:
Y——盐基度(响应值);
A——硫酸:硫酸亚铁;
B——双氧水:硫酸亚铁;
C——熟化温度。
根据上述回归模型进行方差分析,优化PFS制备条件响应面分析结果如表6所示。

Table 6. Response surface analysis results of PFS preparation conditions
表6. PFS制备条件响应面分析结果
对于P值,当P ≤ 0.05,则所在项目对X影响显著;若P ≤ 0.01,则所在项目项对X影响极显著;反之,当P ≥ 0.05,所在项对X影响不显著。若模型项的P ≤ 0.05,说明响应值X与A,B,C,A2……各项目的回归方程的关系是显著的,同样P ≤ 0.01说明响应值X与A,B,C,A2……各项目的回归方程的关系是极显著的。
模型项的F值为1223.51,P值 ≤ 0.0001,表明X与A,B,C,A2的回归方程的关系极显著。其中除却AB的P值为0.9359 ≥ 0.05,影响不显著之外,其余项均小于0.01,影响极显著。模型的校正决定系数R2为0.9997,表明该模型拟合效果较好有较高的可信度,能够解释99.97%的变化。由此可见,该模型设计具备合理性和可取性。
为了更好地表征该模型的拟合效果,应通过分析常态概率与标准化残差的关系,得出该模型的残差正态分布图 [9],如图5、图6可知,模型的残差正态分布基本上都在直线上,标准化残差的数据主要分布在[−1,1]区间内,全部数据均在[−1.5,1.5]区间内,这表示标准化残差服从N(0,1)正态分布。此外,如下图所示,预测值与实际值各点基本分布在直线上,大部分数据在[8,16]区间内。
综合以上分析,该模型实际拟合度高,可以应用于本文的研究。
在响应面分析法双因子交互影响等高线图中,等高线排布越密集,越陡,即说明在设定范围两个因子对响应值的影响越显著,反之,两因子对响应值得影响越不显著 [10]。
n(H2SO4):n(FeSO4)和n(H2O2):n(FeSO4)的比值对盐基度的交互影响响应面图及其等高线图如图7所示。通过图7(A)可知,在设定区间内,当n(双氧水): n(硫酸亚铁)一定时,盐基度随着n(H2SO4):n(FeSO4)的增大而降低。图7(B)中的等高线单向突出且呈左侧较陡,右侧平缓的趋势。可见当n(H2O2):n(FeSO4)一定时,n(H2SO4):n(FeSO4)的增大对盐基度影响逐渐减缓。当n(H2SO4):n(FeSO4) < 0.243时,盐基度将大于且无法达到12%。当n(H2SO4):n(FeSO4) ≥ 0.243时,可通过调节双氧水与硫酸亚铁之比,使产品盐基度为12%,最低n(H2O2):n(FeSO4)为0.5:1。

Figure 7. n(H2SO4):n(FeSO4) and n(H2O2):response surface diagram (A) and contour diagram (B) of the influence of n(FeSO4) on the salinity
图7. n(H2SO4): n(FeSO4)和n(H2O2): n(FeSO4)对盐基度的影响响应面图(A)及等高线图(B)
n(H2SO4):n(FeSO4)和熟化温度对盐基度的交互影响响应面图及其等高线图如图8所示。如图8(B),在设定区间内,温度较低时,等高线变化趋势明显较陡,此时温度和n(H2SO4):n(FeSO4)对盐基度的影响较显著。温度较高或者n(H2SO4):n(FeSO4) > 0.23时,变化逐渐减缓。当T < 59.2℃或者n(H2SO4):n(FeSO4) < 0.23时,盐基度将大于且无法达到12%。T ≥ 59.2℃且硫酸亚铁的比值≥0.53时,可沿等高线取得一系列让盐基度达到12%的点。所以最低应取n(H2SO4):n(FeSO4) > 0.23,T ≥ 59.2℃。
n(H2O2):n(FeSO4)和T对盐基度的交互影响响应面图及其等高线图如图9所示。
根据图9(A),在选定区域之内,随着n(H2O2):n(FeSO4)与熟化温度(T)的增大,盐基度逐渐降低。当n(H2O2):n(FeSO4) > 0.6时,这一趋势逐渐减缓;当T > 60℃时,盐基度减小的趋势也开始减缓并达到最低值,最后缓缓上升。根据图9(B),在选定区域之内,温度较低时,n(H2O2):n(FeSO4)与T对盐基度的影响较明显,随着两个因子增大,其本身对产品盐基度的影响降低。同时盐基度随着n(H2O2):n(FeSO4)与熟化温度(T)的增大而降低。

Figure 8. n(H2SO4):response surface diagram (A) and contour diagram (B) of the ratio of n(FeSO4) and curing temperature’s influence on the salinity
图8. n(H2SO4): n(FeSO4)之比与熟化温度对盐基度的影响响应面图(A)及等高线图(B)

Figure 9. n(H2O2):response surface diagram (A) and contour diagram (B) of the influence of n(FeSO4) and curing temperature on the salinity
图9. n(H2O2): n(FeSO4)与熟化温度对盐基度的影响响应面图(A)及等高线图(B)
3.3. PFS优化工艺条件及试验验证
3.3.1. 优化工艺条件结果
通过Design Expert8.06对该模型进行优化,得到最优化数字结果:n(H2SO4) :n(FeSO4)为0.25:1;n(H2O2):n(FeSO4)为0.60:1;熟化温度为59.88℃。预测盐基度为12.00%。
为了验证模型的可行性和优化结果的可靠性和准确性,通过实验验对该结果进行了模型的验证。采用优化设计条件制备PFS,进行3组平行试验,结果如表7所示。
优化工艺后制得的PFS全铁含量、还原性物质含量、盐基度、pH均达到《水处理剂聚合硫酸铁》(GB/T 14591-2016)一等品标准,同时三个平行测得的盐基度平均值12.01%与理论预测值12.00%相近,但差距极小。
3.3.2. 混凝试验
将本文所得最佳条件制备的PFS与市售商品PFS同时用于模拟废水处中,并对比两者处理效果。

Table 7. Optimization process results
表7. 优化工艺结果

Table 8. Coagulation test results of simulated wastewater
表8. 模拟废水混凝试验结果

Figure 10. Coagulation test results of simulated wastewater
图10. 模拟废水混凝试验结果
从表8和图10可以看出,在一定范围内,随着絮凝剂投加量的增加,废水的COD、SS的去除率都在增加,当投加量为500 mg·L−1时,各指标的去除率达到最大值,同时随着投药量的增大两种药品的处理效果逐渐趋近,可见本试验制备的PFS的处理效果与市售商品的处理效果相当。
3.4. 成本测算及比较
根据响应面分析法输出的直接氧化法制备PFS最佳条件进行计算得到制备1吨PFS的成本计算公式为:
根据目前工业药品价格行情,工业级药品单价在逐步调整,尤其是工业级硫酸下降趋势迅猛,无法实时监测其变化。本文成本测算按照拟写完成时工业级药品的单价进行成本测算。工业化化生产一吨PFS的原料单价如表9。

Table 9. PFS raw material specifications and price list
表9. 制备PFS原料规格及价格一览表
计算得出按照本文条件,目前工业生产PFS的成本价格约为309.05元/t。目前液态PFS商品市场价格约为400元/t。按照本文所得到的H2O2氧化法制备PFS的最优条件,目前工业生产PFS能够产生的利润比使用NaNO2催化氧化法制备PFS成本更高,但质量更好,更加环保。
4. 结论
本文主要通过单因素试验结合响应面分析法对H2O2直接氧化法制备PFS的制备条件中的n(H2SO4):n(FeSO4)、n(H2O2):n(FeSO4)以及熟化温度(T)进行了优化,验证之后从而得到的关于PFS的最佳制备条件。结果表明:盐基度单因素试验中,最佳n(H2SO4):n(FeSO4)比值区间为[0.2, 0.3];最佳n(H2O2):n(FeSO4)比值区间为[0.5, 0.7];最佳熟化温度T区间为[55, 65]℃。经过响应面分析法优化后的最佳制备条件为:n(H2SO4):n(FeSO4)的比值为0.25;n(H2O2):n(FeSO4)的比值为0.60;熟化温度T为60.25℃。且经验证,产品符合《水处理剂聚合硫酸铁》(GB/T 14591-2016)一等品标准。
李芙蓉 [11] 运用单因素试验逐步探究直接氧化法制备PFS的制备条件最终结果为:每氧化10 g七水合硫酸亚铁,需要消耗0.8 mL H2SO4与3.0 mL H2O2。通过换算,相比本文每氧化10 g七水合硫酸亚铁,消耗0.49 mL H2SO4与2.2 mL H2O2。H2SO4消耗量同比下降38.91%,H2O2消耗量同比下降26.67%。赵志雄 [12] 实验得出的最佳条件是:FeSO4,H2SO4和H2O2摩尔比为1:0.26:0.6,,温度控制在常温,反应 2.5 h。本文响应面分析法输出的最优条件为:FeSO4,H2SO4和H2O2摩尔比为1:0.25:0.6,反应温度为常温,熟化温度为59.88℃。本文H2SO4消耗量同比下降3.85%。
5. 建议
本文最终产品对废水处理效果与市售PFS商品,效果相仿,废水处理的最佳投药量约为500 mg/L。根据成本测算,工业化H2O2氧化生产PFS利润空间较催化氧化法要小,然而本实验只在众多影响因素中取三个为表征系数,H2O2氧化生产PFS的最佳条件还有待进一步的研究。
基金项目
1) 2019年广东省省级农业产业技术体系–水产疫病监测与综合防控共性关键技术研发创新团队,已经立项同,经费30万元。(子项目第1主持人)
2) 2019年广州市对外合作项目–大数据优化的高效菌藻废水资源化系统及低抗饲料制品示范(201907010056)。
3) 基于大数据网络分析菌藻联动除磷机制(2019年“攀登计划”广东大学科技创新培育专项资金pdjh2019a0241)。
4) 2018年广东省自然科学基金–基于交互网络分析的养殖废水处理中微藻–益生菌联动机理研究(2018A03031342)。
NOTES
*通讯作者。