1. 引言
葡萄糖是自然界分布最广的一种单糖,同时它是糖尿病判断的标准之一。目前糖尿病发病率较高,对葡萄糖检测和防治至关重要。它是活细胞的能量来源和新陈代谢的中间产物,是生物主要的供能物质。葡萄糖的测定在工业生产、生物科技、医疗领域等方面有着重要的意义。因此,建立其快速、简便、准确的分析检测方法在临床和实际应用中具有重要意义。目前常用的分析方法为葡萄糖氧化酶(GOx)法,这种酶具有专一性高、反应速率快等优点,但易受温度、湿度、pH值、有毒物质等周围环境的影响,并且成本较高、不易储存、固定程序复杂 [1] [2] ,从而限制了该类酶传感器的应用和推广。因此,新型无酶葡萄糖传感器的研究成为该领域的热点。
无酶葡萄糖传感器的电极材料主要包括纳米金属(金 [3] 、银 [4] 、铜 [5] 、镍 [6] 、铂 [7] )及其氧化物(氧化铜 [8] 、氧化镍 [9] 等)。其中,纳米Cu因价格低、不易毒化而备受关注。本文用电沉积法将纳米铜粒子修饰在碳糊电极上,成功制备了纳米铜修饰碳糊电极,并研究了葡萄糖在修饰电极上的电化学行为,实现了对葡萄糖的高效、快速、定量检测。
2. 实验部分
2.1. 仪器与试剂
电子分析天平FA2104 (上海民桥电子仪器厂)、KQ-50B型超声波清洗器(昆山市超声仪器有限公司)、电化学工作站(上海辰华仪器公司)。三电极系统:铂电极为对电极,饱和甘汞电极为参比电极,自制碳糊电极为工作电极。
硫酸、硫酸铜、氢氧化钠、葡萄糖、尿素、柠檬酸、草酸、抗坏血酸等均为国药集团生产的分析纯试剂,维他命水(农夫山泉有限公司),西柚茉莉花茶(农夫山泉有限公司)。
2.2. 修饰碳糊电极的制备
将高岭土、石墨粉与液体石蜡以质量比为3:11:6混合,放入玛瑙研钵中研磨均匀,压入碳糊电极中,将所制碳糊电极在称量纸上磨擦处理,使其表面至平整。若液体石蜡比例低,则电流残留电流过大,灵敏度较低,测定结果不太理想。若液体石蜡比例较高,则碳糊容易脱落,影响测定。
将制备好的碳糊电极放入25 mL 0.1 mol/LH2SO4溶液中,加入100 μL 0.1 mol/L硫酸铜,设定沉积电位为−1.2 V,沉积80 s后取出,用去离子水冲洗即得到由铜修饰的碳糊电极 [10] 。相同的方法制得钴镍修饰碳糊电极。
2.3. 实验方法
所有的电化学测试采用三电极系统,铂电极为对电极,饱和甘汞电极为参比电极,铜修饰的碳糊电极为工作电极,在室温下进行,在0.0~0.8 V电位范围内,用循环伏安法研究葡萄糖在不同电极上的电化学行为,交流阻抗在2.5 × 10−3 mol/L K3Fe(CN)6/K4Fe(CN)6 + 0.1 mol/L KCl溶液中进行。用计时安培法研究葡萄糖的浓度与电流的关系,并对实际样品进行检测。
3. 结果与分析
3.1. 修饰电极的表征
分别测定了裸碳糊电极和铜修饰碳糊电极在2.5 × 10−3 mol/L K3Fe(CN)6/K4Fe(CN)6 + 0.1 mol/L KCl溶液中的交流阻抗(EIS)行为。如图1所示,铜修饰碳糊电极阻抗小于裸碳糊电极的阻抗,说明纳米铜负载于碳糊电极后,减小了对带负电的[Fe(CN)6]3−/[Fe(CN) 6]4−电对的电子转移阻力,更有利于电化学反应的进行。说明铜成功修饰到碳糊电极上。

Figure 1. Electrochemical impedance spectroscopy of bare carbon paste electrode (CPE) (b) and Cu modified carbon paste electrode (a)
图1. 铜修饰碳糊电极和裸碳糊电极的交流阻抗图,a修饰铜碳糊电极的阻抗图;b裸碳糊电极的阻抗图
3.2. 葡萄糖在修饰电极上的电化学响应
分别将裸碳糊电极和铜修饰碳糊电极放入25 mL 0.1 mol/L NaOH溶液中加入25 μL 1.01 × 10−4 mol/L葡萄糖溶液进行循环伏安法扫描(图2),结果表明葡萄糖在铜修饰碳糊电极具有明显的氧化还原响应。葡萄糖在铜修饰碳糊电极上的反应机理推测如下 [11] :
(1)
(2)
(3)
(4)
首先,Cu在NaOH溶液中被电化学氧化为CuO;CuO进一步被氧化为具有强氧化力的Cu(III)形式,如CuOOH或
;最后,葡萄糖被Cu(III)催化氧化为葡萄糖酸内酯,而葡萄糖酸内酯最终水解为葡萄糖酸。

Figure 2. Cyclic voltammograms of different electrodes by sweeping potential from 0 V to 0.8 V; 1: CPE, 2: CPE/Cu
图2. 葡萄糖在碳糊电极上的CV图;1裸碳糊电极CV图;2铜修饰碳糊电极CV图
3.3. 葡萄糖在不同修饰电极上的计时安培曲线
在25 mL 0.1 mol/LNaOH溶液加入25 μL 1.01 × 10−4 mol/L葡萄糖溶液,分别用不同修饰电极研究葡萄糖的电化学行为(图3)。从图中可以看出葡萄糖在修饰钴镍碳糊电极和裸碳糊电极上均无明显的响应,说明钴镍修饰碳糊电极无催化氧化葡萄糖的性能。葡萄糖在铜修饰碳糊电极上有明显的电化学响应。
3.4. 电沉积电位的影响
在25 mL 0.1 mol/LH2SO4的沉积液中,加入100 μL 0.1 mol/L硫酸铜溶液。沉积时间60 s,改变沉积电位分别为(−1 V, −1.2 V, −1.3 V, −1.4 V, −1.5 V),研究不同沉积电位对修饰电极的电化学性质的影响。将不同沉积电位下所制得的铜修饰碳糊电极置于25 mL 0.1 mol/L氢氧化钠溶液中,加入25 μL 1.01 × 10−4 mol/L葡萄糖溶液,工作电位为0.6 V,进行计时安培扫描,得到图4。结果表明沉积电位由−1 V至−1.5 V时,响应电流逐渐增大,当沉积电位为−1.2 V时所制得的铜修饰碳糊电极对葡萄糖的电化学响应最灵敏,稳定性最好,所以最佳沉积电位为−1.2 V。

Figure 3. Amperometric response of different electrodes for successive addition of glucose to 0.1 mol/L NaOH solution at 0.6 V; (1) Co/Ni modified CPE; (2) CPE; (3) Cu modified CPE
图3. 葡萄糖在不同修饰碳糊电极上的计时安培图;1钴镍修饰碳糊电极计时安培图;2裸碳糊电极计时安培图;3铜修饰碳糊电极计时安培图

Figure 4. Amperometric response of different electrodes for successive addition of glucose to 0.1 mol/L NaOH solution at 0.6 V; (1) deposition potential: −1 V; (2) deposition potential: −1.2 V
图4. 葡萄糖在不同修饰电极上计时安培图;1沉积电位−1 V;2沉积电位−1.2 V
3.5. 电沉积时间的影响
在25 ml 0.1 mol/LH2SO4的底液中,加入1 mL 0.1 mol/L硫酸铜溶液。将电极置于上述溶液中,确定沉积电位−1.2 V。改变沉积时间分别为(20 s, 40 s, 50 s, 60 s, 80 s),将制得的铜修饰碳糊电极置于25 mL 0.1 mol/L氢氧化钠溶液中,加入25 μL 1.01 × 10−4 mol/L葡萄糖溶液,工作电位为0.6 V,进行计时安培扫描,得到图5。从图中可以看出沉积时间由20 s延长至80 s时,响应电流逐渐增大。当时间是80 s时所得到的修饰碳糊电极对葡萄糖的电化学响应最明显且最稳定,所以最佳沉积时间为80 s。
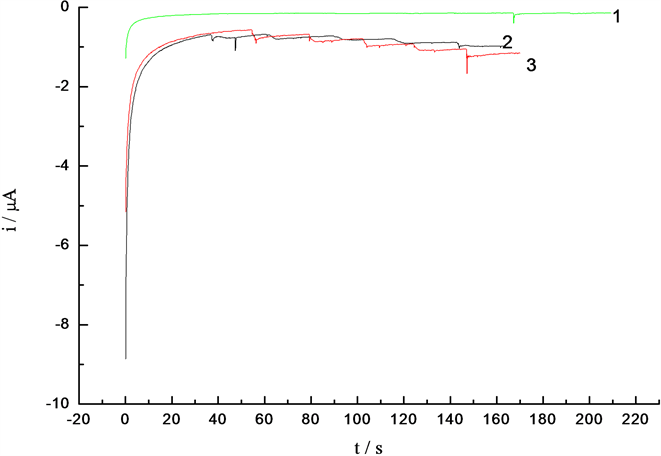
Figure 5. Amperometric response of different electrodes for successive addition of glucose to 0.1 mol/L NaOH solution at 0.6 V; (1) deposition time: 20 s; (2) deposition time: 80 s; (3) deposition time: 40 s
图5. 葡萄糖在不同沉积时间下所得的修饰电极上的计时安培图;1沉积时间 20 s;2沉积时间80 s;3沉积时间40 s
3.6. 葡萄糖定量检测
3.6.1. 工作电位的影响
在25 mL 0.1 mol/LNaOH溶液加入25 μL 1.01 × 10−4 mol/L葡萄糖溶液,在不同工作电位(0.4 V, 0.5 V, 0.6 V, 0.7 V, 0.8 V)下,研究葡萄糖在铜修饰碳糊电极上的电流响应。结果显示,当工作电位由0.4 V增至0.8 V时,电流响应逐渐增强,由于在较高工作电位下,一些在低电位下稳定的物质可能被氧化,对测定产生干扰,因此测定的工作电位确定为0.6 V。
3.6.2. 线性范围与检出限
在最佳测定条件下,向25 mL 0.1 molL NaOH溶液中依次加入25 μL 1.01 × 10−4 mol/L葡萄糖溶液20次,得到响应电流随时间的变化曲线图6所示,结果表明在浓度为1.01 × 10−7~1.20 × 10−5 mol/L范围内葡萄糖电流与浓度呈线性关系(图7),其线性方程为:I(10−7A) = 1.05 + 0.81C(10−7 mol/L),R = 0.9953,检出限为5.0 × 10−8 mol/L。
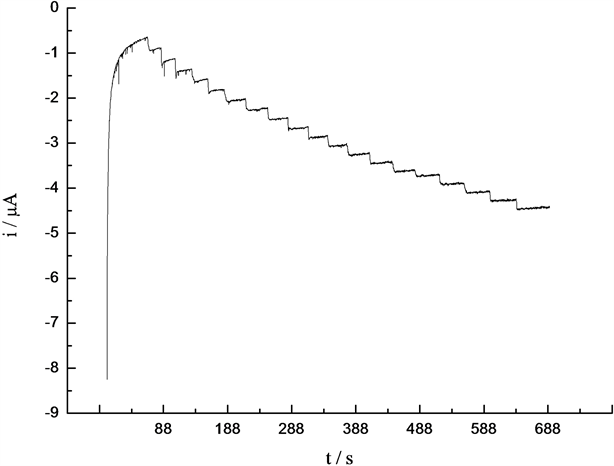
Figure 6. Chronoamperogram of Glucose at Copper Modified Carbon Paste Electrode
图6. 葡萄糖在铜修饰碳糊电极上的计时安培图

Figure 7. Linear relationship between glucose concentration and current
图7. 葡萄糖浓度与电流的线性关系曲线
3.7. 干扰实验
考察了一些干扰物对葡萄糖测定的影响。工作电位为0.6 V,在25 mL 0.1 mol/LNaOH底液中,先加入25 μL 1.01 × 10−4 mol/L葡萄糖,依次加入25 μL 0.1 mol/L尿素,柠檬,草酸,抗坏血酸,记录计时安培曲线。如图8所示,可以看出尿素对葡萄糖的响应电流略有影响,柠檬酸和草酸无明显反应,当抗坏血酸加入时电流影响大,由此可得抗坏血酸干扰最强。其它常见无机离子对测定均无干扰。
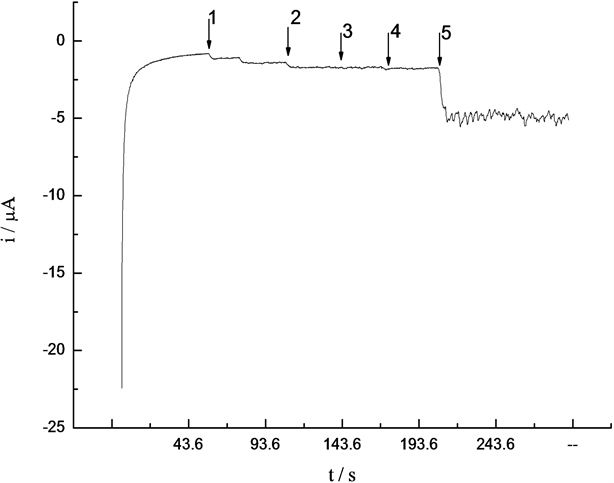
Figure 8. Amperometric response of glucose in the presence of different interferents; 1 glucose; 2 urea 3; citric acid; 4 oxalate; 5 ascorbic acid
图8. 加入干扰物时葡萄糖的计时安培图;1葡萄糖;2尿素;3柠檬酸;4草酸;5抗坏血酸
3.8. 电极的重现性、稳定性
将制备好的铜修饰碳糊电极放入25 mL 0.1 mol/L NaOH溶液中运行待背景电流稳定之后加入25 μL 1.01 × 10−4 mol/L葡萄糖标准溶液,运行250 s电流基本稳定。电极重复测定10次,电将制备好的电极在室温下放置1个月后,同样条件下对葡萄糖进行检测,其对葡萄糖的电流响应几乎不变,表明该修饰电极具有较好的稳定性和重现性。
3.9. 实际样品的测定
在上述最佳实验条件下,工作电位0.6 V,在25 mL 0.1 mol/L NaOH溶液中分别加入50 μL 2 mg/mL葡萄糖粉剂配制的溶液,25 μL西柚茉莉花茶,25 μL维他命水溶液(2 mL稀释至10 mL),记录计时安培曲线,根据响应电流及校正曲线分别计算出葡萄糖粉剂,茉莉花茶和维他命水中的葡萄糖浓度。测定结果见表1。结果与斐林试剂滴定法测定结果相近 [12] 。

Table 1. The determination of samples
表1. 样品的测定
4. 结论
实验用铜修饰碳糊电极对葡萄糖进行检测。探讨了修饰碳糊电极的条件,得到了修饰碳糊电极的最佳条件:沉积电位−1.2 V,沉积时间80 s。将修饰的碳糊电极用于葡萄糖的测定并对测定的条件进行了探讨,得到最佳工作电位0.6 V。葡萄糖在浓度为1.01 × 10−7~1.20 × 10−5 mol/L范围内电流与浓度呈线性关系,其线性方程为:I(10−7A) = 1.05 + 0.81C(10−7 mol/L),R = 0.9952,其检出限为5.0 × 10−8。用铜修饰碳糊电极测定葡萄糖不仅电极制作简单方便、容易操作,而且电极性能稳定,重现性好。