1. 引言
芦丁(Rutin)又称芸香苷,广泛存在于豆科植物槐花蕾和蓼科植物苦荞中 [1] [2] ,是自然界中常见的一种具有生物活性的黄酮成分。芦丁有抗菌,抗炎,抗氧化等多种活性,可以降低毛细血管异常通透性和脆性,临床主要用于高血压病的辅助治疗 [3] [4] 。另外,在食品工业中芦丁是很好的天然黄色素和抗氧化剂 [5] 。但芦丁的水溶性较差,限制其在体内的吸收及其他应用。目前通过芦丁-HPMC控释片、固体分散体、环糊精包合、纳米粒等技术来改善其水溶性并提高生物利用度 [6] [7] 。目前环糊精包合技术一般通过饱和水溶液法、溶液法、研磨法或超临界流体技术得到包合物 [8] [9] 。因芦丁在常用挥发性溶剂甲醇、乙醇、丙酮等中的溶解度较小,采用上述方法制备包合物的效率较低。本实验基于HP-β-CD在N,N-二甲基甲酰胺(DMF)中溶解度较大而在丙酮中溶解度较小的特点,采用反溶剂法制备环糊精包合物,并对其进行表征确定包合物的形成。另外考察了芦丁包合后水溶性及体外溶出的改善情况。
2. 仪器与材料
Waters高效液相色谱仪(美国Waters公司),SHJ-A4水浴恒温磁力搅拌器(常州华奥仪器制造有限公司),LXJ-IIB型离心机(上海安亭科学仪器厂),Philips X-射线衍射仪(XRD,荷兰Philip公司);S4800扫描电镜(SEM,日本Hitachi公司)。
RU标准品(纯度为99.9%,上海源叶生物科技有限公司);RU原粉(纯度 ≥ 98%,阿拉丁试剂);HP-β-CD (阿拉丁试剂)、二甲基甲酰胺(DMF)、丙酮(天津市天力化学试剂有限公司),分析纯;冰乙酸(天津市致远化学试剂有限公司),分析纯;甲醇、(山东禹王实业有限公司),色谱纯;水为去离子水。
3. 方法与结果
3.1. 反溶剂法制备芦丁-羟丙基-β-环糊精包合物
根据Tien An Nguyen等 [10] 的研究可知RU和HP-β-CD的最佳投料比为摩尔比1:1。将RU和HP-β-CD按比例溶解在DMF中,溶液室温下搅拌30 min,以体积比1:5将DMF溶液加入丙酮中,反应3 min,3500 r/min离心获得沉淀,并用丙酮洗涤3次,抽滤得包合物,50℃真空干燥12 h。
3.2. 芦丁含量测定
取适量RU-HP-β-CD溶于10 mL甲醇溶液中,利用高效液相色谱检测包合物中芦丁的含量 [11] 。Waters C18反相柱(250 × 4.6 mm,5 μm,中国),柱温为25℃,甲醇:0.5%冰醋酸的 = 60:40(v/v)作为流动相,流速为0.8 mL/min,进样量是5 μL,检测波长为354 nm [10] 。进样前所有样品经过0.22 μm滤膜处理。结果显示包合物中芦丁含量为26.5%。
3.3. 芦丁-羟丙基-β-环糊精表征
3.3.1. XRD
取适量芦丁、HP-β-CD、芦丁和HP-β-CD的物理混合物(以下简称物理混合物)及芦丁与HP-β-CD的包合物(以下简称包合物),使用X衍射仪对其晶型结构进行分析。检测条件为:衍射角范围4˚~50˚,扫描速率为4˚/min,电压40 kV,电流30 mA。图1中显示,芦丁有明显的晶体结构衍射峰,HP-β-CD为无定形态,两者的物理混合物中,环糊精在一定程度上减弱了芦丁的衍射峰,但在2θ = 26˚有芦丁的特征峰,而包合物中芦丁的衍射峰消失,说明芦丁已经被环糊精包合,以无定形态存在。XRD的检测结果与苏彩娟等人的研究(文章编号1673-2383(2011)01-0053-05)一致。
3.3.2. IR
分别称取适量干燥后的芦丁、HP-β-CD、物理混合物及包合物样品与KBr压片,放入红外光谱仪进行检测。薄片在400~4000 cm−1波数处检测,分辨率为4 cm−1。如图2所示,物理混合物在1208~1652 cm−1
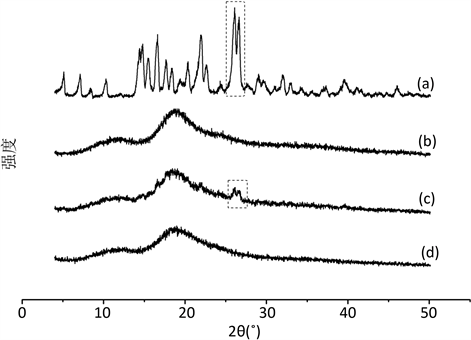
Figure 1. XRD results of Rutin (a); HP-β-CD (b); Physical mix (c); Inclusion complex (d)
图1. XRD图芦丁(a);羟丙基-β-环糊精(b);物理混合物(c);包合物(d)
之间完全显示出芦丁的特征峰,而包合物在这段区域峰的明显减少,这结果说明芦丁与HP-β-CD形成了包合物而不是简单的物理混合。红外检测结果与XRD相符。
3.3.3. SEM
为了进一步证实包合物的形成,将芦丁、HP-β-CD和包合物真空下镀金使用S4800型扫描电镜对其形貌进行观察分析。图3为三种样品的SEM图。图3a可以看出,芦丁呈规则棒状结构,HP-β-CD呈球形,由于主客分子的相互作用,包合物形态发生了明显的变化。HP-CD具有很好的水溶性特征,与其形成包合物后,芦丁的水溶性将会得到改善。
3.4. 溶解度的测定
取适量的芦丁、物理混合物和包合物置于10 mL的小瓶中,加入5 mL的蒸馏水,放入37.0 ± 0.5℃的水浴锅中,以100 r/min搅拌48 h。反应结束后从瓶中各取1 mL样品离心10 min取上清,离心速度为10,000 g。用甲醇稀释后取5 µL通过高效液相色谱进行检测。实验重复3次取平均值。图4中显示了芦丁、物理混合物和包合物在水中饱和溶解度的结果。芦丁、物理混合物和包合物的溶解度分别为0.12,

Figure 2. Infrared spectrum of rutin (a); HP-β-CD (b); physical mix (c); inclusion complex (d)
图2. 芦丁(a);羟丙基-β-环糊精(b);物理混合物(c);包合物(d)的红外图谱

Figure 3. SEM graphs of Rutin (a); HP-β-CD (b) and inclusion complex (c)
图3. 芦丁(a)、HP-β-CD (b)和包合物的SEM图谱
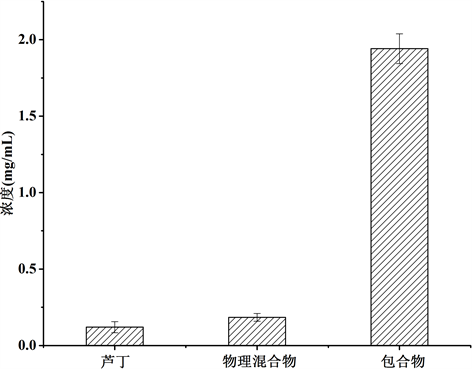
Figure 4. Equilibrium solubility of rutin, physical mix, inclusion complex in water
图4. 芦丁、物理混合物和包合物在水中的饱和溶解度

Figure 5. Dissolution profiles of rutin (a) and inclusion complex (b) in water
图5. 芦丁(a)和包合物(b)在水中的溶出速率
0.18,1.94 mg/mL。HP-β-CD对芦丁有一定的助溶作用,但包合物的溶解度明显高于芦丁原粉和物理混合物。由于HP-β-CD在水中有很好的水溶性,在芦丁与HP-β-CD形成包合物后,芦丁进入环糊精的空腔,使包合物表现出环糊精易溶于水的特性,改善了芦丁的水溶性。因此,可以通过反溶剂重结晶法获得环糊精包合物。
3.5. 体外溶出速率测定
为了研究包合物在体外释放的规律,本实验中分别取芦丁和包合物(含芦丁77.6 mg)置于200 mL水溶液中,并在37.0 ± 0.5℃和300 rpm的恒温振荡器中进行搅拌。在不同的时间间隔(0.083,0.16,0.25,0.33,0.5,1,1.5,2,4,6,8,12和24小时)中取1 mL样品进行离心,取上清利用高效液相色谱检测芦丁浓度,液相条件同3.2,计算芦丁在不同时间点的溶出速率。此实验重复3次获得平均值。
图5显示了芦丁原粉和包合物在不同时间点的溶出速率,可以看出,包合物的溶出速率远高于原粉,在水中溶出速率提高了约4倍,可释放80%左右,而由于芦丁的水溶性较差在24 h后只释放出20%。在Kouzou Miyake [12] 等人的研究中,RU-HP-β-CD的溶出速率是原药的2倍,而本实验中通过反溶剂法制备的羟丙基-β-环糊精包合物的溶出速率提高了4倍。
4. 讨论
环糊精包合物近年来在药物制备方面获得了广泛的应用。包合物与原药相比具有更好的亲水性和缓释效果,更利于人体吸收。另外包合物可以改善药物的稳定性,如对光热敏感、易分解的药物,且没有毒副作用 [13] 。在本研究中,改变传统获得包合物的方法,利用反溶剂重结晶法获得芦丁-羟丙基-β-环糊精包合物,并用XRD,SEM,红外对其进行表征,包合物表现出更多环糊精的特征形态,说明可以利用反溶剂法获得包合物。另外所得包合物很大程度上改善了芦丁的溶解度和体外溶出速率,有助于人体内更好的吸收,提高其生物利用度。
基金项目
国家重点研发计划课题(No.2017YFD060070601)。