1. 引言
马铃薯是是继玉米、水稻、小麦之后的第四大主要作物 [1] 。目前,栽培生产用的大部分是白色或黄色等薯肉的马铃薯,随着近几年来人们对彩色食品的偏爱,世界的研究热点也开始转向红色、紫色、蓝色等薯肉的彩色马铃薯,马铃薯产业也在云南省有着重要的地位 [2] 。花色苷是一种天然的抗氧化剂,具有抗氧化活性、抗衰老、防止血管硬化的功能,是一种潜在的抗癌化合物,在彩色马铃薯中含量丰富,使得彩色马铃薯不仅外形美观,而且抗氧化活性也很高 [3] 。
花色苷形合成涉及多种基因。它们可分为两大类:一类是结构基因,另一类是调节基因,即转录因子等 [4] 。研究表明,马铃薯花色苷合成调控基因编码产物为转录因子,激活或抑制靶基因的转录表达的蛋白,包括WD40、MYB、bHLH、WRKY、bZIP和MADS.BOX等,它们通过DNA序列特异性结合蛋白以及蛋白与蛋白之间的相互作用,结合到花色苷合成结构基因启动子的顺式作用元件上,特异性地激活或者抑制结构基因的表达,从而使得花色苷合成关键基因在不同组织不同阶段协同表达 [5] 。目前已经从拟南芥,玉米,矮牵牛,灯盏花,番茄等多个物种分离得到许多MYB转录因子他们大都直接或者间接转录激活花色苷多种结构基因,MYB类转录因子家族相关基因的调节活性的多样性是自然界中植物着色模式多变的主要原因 [6] 。本研究通过同源克隆技术,从彩色马铃薯中克隆新的转录因子MYB类型转录因子StMyb-like,并进行表达模式分析与RNA干涉载体构建,为研究彩色马铃薯花色苷合成途径的调控机制奠定理论基础。
2. 材料与方法
2.1. 材料与试剂
2.1.1. 植物材料
供实验材料为云南主要栽培彩色马铃薯品种“黑金刚”,种植于云南农业大学后山实验田,共采集健康的马铃薯“黑金刚”的叶片、根、茎、薯皮、薯肉和嫩芽,为实验对象,于无菌保鲜袋−80℃冰箱保存。
2.1.2. 载体与菌株
实验使用到的中间载体和终载体分别为pKANNIBAL载体(中间载体)和pART载体(最终载体)由本实验室保存,载体示意图参见刘正杰等(2013) [7] 。
PCR所用EasyTaq、EasyTaq Buffer、dNTPs、各种限制性内切酶以及T4连接酶都是TaKaRa公司产品;DNA操作试剂盒(柱式质粒DNA小量抽提试剂盒、柱式PCR产物纯化试剂盒以及柱式DNA胶回收试剂盒)都是生工公司产品。
2.2. RNA提取、cDNA合成
彩色马铃薯RNA提取参照CTAB-PVP法 [8] ,cDNA合成方法参照RT-PCR试剂盒(Promega公司)说明书。
2.3. 基因的克隆与分析
通过应用其他物种的花色苷合成相关转录因子保守区域在NCBI上Blast比对马铃薯EST数据库获得分值较高的Unigene或EST序列,经拼接获得马铃薯中花色苷合成相关转录因子MYB的部分基因序列,再重新比对马铃薯EST数据库,获得更多的Unigene或EST并进行拼接,直到获得包含完整ORF的基因序列。根据获得的包含完整ORF的基因序列,设计引物StMybF1和StMybR1 (见表1),以cDNA为模板进行扩增。
PCR体系为:cDNA模板2 ul、上游引物(10×) 1 ul、下游引物(10×) 1 μl、TaKaRa {dNTP Mixture 2 μl、Buffer (10×) 2.5 μl、TaqDNA聚合酶0.5 μl}、ddH2O补齐至总体积25 μl。
PCR反应条件:94℃预变性4 min;94℃变性30 s,退火温度57℃,72℃延伸30 S,循环30个;72℃延伸10分钟,回收PCR产物。
PCR产物连接至pMD18-T载体,转化至大肠杆菌E. coli DH5α,挑取经PCR检测的阳性单克隆送样测序。

Table 1. Primer sequences used in this study
表1. 本研究所用到的引物序列
根据目的基因StMyb-like的测序结果,应用不同软件进行初步的生物信息学分析。通过Blastn软件(http://www.ncbi.nlm.nih.gov/blast),预测目的基因可能所属于的基因家族;以NCBI-BlastORF软件进行其读码框分析;在线http://www.ncbi.nlm.nih.gov/Structure/cdd/wrpsb.cgi分析蛋白结合结构域。
2.4. StMyb-like基因RNA干涉载体构建
2.4.1. 目的基因RNA干涉片段的扩增
以彩色马铃薯“黑金刚”cDNA为模板,引物StMyb-zpF1和StMyb-zpR1 (见表1)扩增StMyb-like正向片段StMyb-zp (约600 bp);以引物StMyb-fpF1和StMyb-fpR1 (见表1)扩增StMyb-like反向片段StMyb-fp。PCR体系和反应条件参照2.3所示。正向片段StMyb-zp和反向片段StMyb-fp均通过琼脂糖凝胶试剂盒回收备用。
2.4.2. RNA干涉片段连接至中间载体pKANNIBAL
以XhoI和KpnI酶切中间载体pKANNIBAL和StMyb-zp。酶切体系:StDof-z 30 ul、XhoI 0.5 ul、KpnI 0.5 ul、10×Buffer 5 ul、ddH2O14 ul 合计50 ul,37℃恒温酶切6 h。回收酶切后的StMyb-zp片段和pKANNIBAL载体,以片段:载体 = 3:1左右配制连接体系:StMyb-zp 14 μl、pKANNIBAL 3 μl、T4-DNA连接酶1 μl、T4-DNA连接酶Buffer 2 μl,16摄氏度过夜连接(不超过12小时),将连接产物转化至大肠杆菌E. coli DH5α,挑取经酶切检测的阳性单克隆提取质粒,并将质粒命名为pKANNIBAL-Mybzp。
以BamH I和Cla I酶切pKANNIBAL-Mybzp质粒和StMyb-fp。酶切体系如上所示,回收酶切后的StMyb-fp片段和pKANNIBAL-Mybzp质粒,以片段:载体 = 3:1左右配制连接体系(如上所示),16摄氏度过夜连接,将连接产物转化至大肠杆菌E. coli DH5α,挑取经酶切检测的阳性单克隆提取质粒,并将质粒命名为pKANNIBAL-Mybzf。
2.4.3. RNA干涉最终载体的构建
以NotI单酶切pKANNIBAL-Mybzf质粒和pART载体。酶切体系:质粒载体30 ul、NotI 0.5 ul、10×Buffer 5 ul、ddH2O补平至50 ul,37℃恒温酶切6 h。回收pKANNIBAL-Mybzf质粒单酶切后较大的约4.3 kb的片段(包含启动子、RNA干涉区段以及终止子),同时回收pART载体单酶切产物。将回收的4.3 kb的片段与pART载体进行连接,将连接产物转化至大肠杆菌E. coli DH5α,挑取经酶切检测的阳性单克隆提取质粒,并将质粒命名为pART-MybRNAi。
3. 结果与分析
3.1. StMyb-like基因的RT-PCR扩增与分析
提取彩色马铃薯叶片RNA,经反转录获得cDNA模板,以StMybF1和StMybR1 (见表1)为引物进行RT-PCR扩增,获得目的基因全长序列。该基因全长798 bp,编码个265个氨基酸,分子量为30.23 kD,理论等电点为6.95。经在线预测,该序列中含有两个HTH DNA结合结构域,是两个串联的MYB类功能域,第一个功能域位于17至73个氨基酸,第二个功能域位于第74至124个氨基酸,该基因编码的蛋白质与马铃薯R2R3-MYB转录因子高度同源性,因此该基因被命名为StMyb-like,如图1。
3.2. StMyb-like基因的表达模式分析
利用半定量RT-PCR分析StMyb-like基因组织表达模式,结果显示,StMyb-like基因在花色苷含量较低的根和茎中表达量都非常低,而与之相比,在薯皮、薯肉、叶和芽等富有花色苷的组织中表达量都比较高,如图2。

Figure 1. Amplification of StMyb-like gene by RT-PCR. Lane M: DNA Maker of DL2000 (from top to bottom respectively 2000, 1000, 750, 500, 250, 100 bp); Lane 1 - 5: gene amplification products
图1. StMyb-like基因RT-PCR扩增。泳道M:DL2000的Maker (从上到下分别为2000, 1000, 750, 500, 250, 100 bp);泳道1~5:基因扩增产物
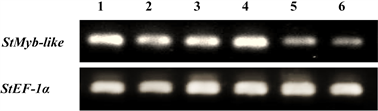
Figure 2. Expression analysis of StMyb-like in different tissues. 1: tuber skin; 2: flesh; 3: bud; 4: leaves; 5: roots; 6: stems
图2. StMyb-like基因在不同组织的表达分析。1:薯皮;2:薯肉;3:芽; 4:叶;5:根;6:茎
3.3. RNA干涉载体的构建与酶切验证
3.3.1. RNA干涉中间载体pKANNIBAL-Mybzf的构建与酶切验证
以XhoI和KpnI酶切StMyb-like基因特异的部分正向片段StMyb-zp,回收后连接至以相同酶(XhoI和KpnI)酶切的pKANNIBAL载体中,获得pKANNIBAL-Mybzp。对pKANNIBAL-Mybzp质粒DNA进行XhoI单酶切以及XhoI和KpnI双酶切验证,双酶切获得约600 bp的目的片段,如图3(a),说明构建正确。
再以BamH I和Cla I酶切StMyb-like基因特异的部分正向片段StMyb-fp,回收后连接至以相同酶酶切的pKANNIBAL-Mybzp质粒载体中,获得pKANNIBAL-Mybzf。对pKANNIBAL-Mybzf质粒DNA进行BamH I单酶切以及BamH I和Cla I双酶切验证,双酶切获得约600 bp的目的片段,如图3(b),说明RNA干涉中间载体pKANNIBAL-Mybzf构建正确。
3.3.2. RNA干涉载体pART-MybRNAi的构建与酶切验证
以NotI单酶切和pART载体,回收单酶切pKANNIBAL-Mybzf获得的约4.3 kb的大片段,如图4(a),
 (a) (b)
(a) (b)
Figure 3. Validation of RNAi intermediate vector by enzyme digestion. (a): single and double enzyme digestion of pKANNIBAL-Mybzp plasmids; (b): single and double enzyme digestion of pKANNIBAL-Mybzf plasmids. Lane 1 - 3: single enzyme digestion; lane 4 - 6: double enzyme digestion; lane M: 1 kb DL (from top to bottom are respectively 10, 8, 6, 5, 4, 3, 2, 1 kb)
图3. RNA干涉中间载体的酶切验证。(a):pKANNIBAL-Mybzp质粒的单酶切和双酶切验证;(b):pKANNIBAL-Mybzf质粒的单酶切和双酶切验证。泳道1~3:单酶切;泳道4~6:双酶切;泳道M:1 kb DL (从上到下分别为10, 8, 6, 5, 4, 3, 2, 1 kb)
 (a) (b)
(a) (b)
Figure 4. Verification of RNA interference vector by enzyme digestion. (a): single enzyme digestion of pKANNIBAL-Mybzf by NotI; (b): single enzyme digestion of RNA interference vectorpART-MybRNAi by NotI. Lane 1 - 3: single enzyme digestion by NotI. Lane M: 15 kb DL (from top to bottom are respectively 15, 10, 8, 5, 4, 2.5, 1.5, 1, 0.5, 0.2 kb)
图4. RNA干涉载体的酶切验证。(a):NotI单酶切pKANNIBAL-Mybzf质粒;(b):NotI单酶切验证RNA干涉载体pART-MybRNAi。泳道1~3:NotI单酶切产物;泳道M:15 kb DL (从上到下分别为15, 10, 8, 5, 4, 2.5, 1.5, 1, 0.5, 0.2 kb)
并连接至pART载pKANNIBAL-Mybzf质粒体,获得pART-MybRNAi。对pART-MybRNAi质粒DNA进行NotI单酶切检测,能获得约4.3 kb的目的片段,如图4(b),说明RNA干涉载体pART-MybRNAi构建正确。
4. 讨论
随着目前对彩色马铃薯花色素苷生物合成途径的认识的逐步加深,彩色马铃薯花色素苷生物合成关键酶基因和转录因子相继被克隆,马铃薯花色苷生物合成途径中相关基因和转录因子功能鉴定也逐步深入 [9] ,其中,转录因子可通过单独或协作作用与结构基因启动子中含有的能被其识别的顺式作用元件结合,促进花色苷生物合成途径中多个基因表达,从而有效启动花色素苷生物合成途径 [4] [10] 。Jung等将马铃薯花色苷调节基因an2转入普通马铃薯栽培种中,其转基因植株叶片、薯皮、薯肉都出现不同程度的紫色 [11] 。Li等从彩色马铃薯品种中克隆了一个WD40类型的转录因子StAN11,StAN11基因的过表达使转基因块茎中花色苷的含量大幅增加,最高是对照的5倍以上 [12] 。
本研究基于同源克隆的方法顺利从彩色马铃薯“黑金刚”栽培品种分离克隆得到一个Myb转录因子家族编码基因,全长798 bp,包含完整CDS的序列,其核酸序列与Gen Bank数据库中R2R3类花青素转录激活基因高度同源,被命名为StMyb-like基因。对该基因的表达模式进行半定量RT-PCT分析发现,在富花色苷的组织中基因的表达量明显高于花色苷含量缺乏的组织,说明该基因的表达与花色苷的合成存在一定的关联,但具体的机理还需要进一步研究。
基因沉默是在生物体生命进程中普遍存在的一种现象,是基因表达调控的一种重要的方式。对于转录后的基因沉默,特别是RNAi技术是分子生物学研究的常用方法,其中,利用含有内含子重复序列来沉默内源基因,是目前应用于转基因诱导基因沉默的有效方法 [13] 。本研究成功构建了含有内含子重复序列的StMyb-like基因RNA干涉载体,为下一步载体的遗传转化和基因功能的剖析提供了研究基础。
基金项目
该实验可以顺利的完成,感谢云南省应用基础研究计划项目(2014FD018)的资助。
参考文献
[1] 李昕, 王建明. 推进马铃薯主粮化的实践与思考[J]. 汉中科技, 2017(3): 11-12.
[2] 郭华春. 云南薯类作物生产现状与产业化前景分析[J]. 西南农业学报, 2004, 17(增刊): 384-387.
[3] 梁敏, 包怡红. 花色苷生物学功能的研究进展[J]. 天然产物研究与开发, 2017 (10): 1785-1790.
[4] 陈敏, 杨清. 马铃薯花色苷生物合成与调控研究进展[J]. 中国马铃薯, 2013, 27(4): 232-238.
[5] Ramsay, N.A. and Glover, B.J. (2005) MYB-bHLH-WD40 Protein Complex and the Evolution of Cellular Diversity. Trends in Plant Science, 10, 63-70. https://doi.org/10.1016/j.tplants.2004.12.011
[6] 许宏宣. 紫肉甘薯花色素苷生物合成相关转录因子克隆与功能分析[D]: [硕士学位论文]. 重庆: 西南大学生物系, 2012.
[7] 刘正杰, 张园, 王玉美, 梁伟, 华金平. 陆地棉GhDGAT1基因干涉载体构建与遗传转化[J]. 中国农业大学学报, 2013, 18(5): 1-8.
[8] Zhang, X., Zhen, J.B., Li, Z.H., Kang, D.M., Yang, Y.M., Kong, J. and Hua, J.P. (2011) Expression Profile of Early Responsive Genes under Salt Stress in Upland Cotton (Gossypium hirsutum L.). Plant Molelular Biology Report, 29, 626-637. https://doi.org/10.1007/s11105-010-0269-y
[9] 肖继坪, 李俊, 郭华春. 彩色马铃薯类黄酮-3-O-葡萄糖基转移酶基因(3GT)的生物信息学和表达分析[J]. 分子植物育种, 2015, 13(5): 1017-1026.
[10] 张新永, 郭华春, 赵昶灵. 彩色马铃薯花色苷生物合成相关基因的研究进展[J]. 中国马铃薯, 2012, 26(3): 177-180.
[11] Jung, C.S., Griffiths, H.M. and De Jong, D.M. (2009) The Potato Developer (D) Locus Encodes an R2R3 MYB Transcription Factor Thatregulates Expression of Multiple Anthocyanin Structural Genes Intuber Skin. Theoretical & Applied Genetics, 120, 45-57. https://doi.org/10.1007/s00122-009-1158-3
[12] Li, W., Wang, B., Wang, M., Chen, M., Yin, J.M., Kaleri, G.M., Zhang, R.J., Zuo, T.N., You, X. and Yang, Q. (2014) Cloning and Characterization of a Potato StAN11 Gene Involved in Anthocyanin Biosynthesis Regulation. Journal of Integrative Plant Biology, 56, 364-372. https://doi.org/10.1111/jipb.12136
[13] Smith, N.A., Singh, S.P., Wang, M.B.,Stoutjesdijk, P.A., Green, A.G. and Waterhouse, P.M. (2000) Total Silencing by Intron-Spliced Hairpin RNAs. Nature, 407, 319-320. https://doi.org/10.1038/35036500