1. 病例汇报
1.1. 临床资料
患者女,36岁,因“经期下腹痛4年余,腹痛加重半月”就诊,入院查体:骨骼发育异常,身材矮小,蹒跚步态,四肢骨骼发育异常,面部可见皮肤色素咖啡斑。实验室检查未见异常。月经史:初潮4岁。既往史:上肢骨折3次、下肢骨折2次。
1.2. X线示
骨性胸廓密度欠均匀,骨质结构紊乱,局部形态欠规整,以左侧锁骨、左肱骨近端为著;右股骨上段形态欠规整,骨质密度不均,见多发斑片状低密度影,局部骨皮质增厚,右髋关节间隙变窄:结合病史,考虑Albright综合征(见图1)。

Figure 1. X-ray showed expansive changes in bilateral iliac bone (right side) and right femur (a); Bilateral scapula (left side) and left clavicle expansion changes (b)
图1. X线显示双侧髂骨(右侧为著)及右侧股骨膨胀性改变 (a);双侧肩胛骨(左侧为著)及左侧锁骨膨胀性改变(b)
1.3. CT示
所示肋骨、椎体及骨盆诸骨骨质排列紊乱、形态失常,呈膨胀性改变,骨质密度不均,部分呈磨玻璃样改变,部分骨质膨胀性改变显著,内见团块状高、低混杂密度,局部向外突出生长,骨皮质连续性中断(见图2)。
1.4. MR示
骨盆骨质多呈膨胀性改变,其内信号不均,以右侧髂骨为著,内见团块状异常信号,T1WI呈高信号,T2WI呈高、低混杂信号,部分区域脂肪抑制后信号减低,局部区域提示扩散受限,部分骨皮质不连续(见图3)。

Figure 2. CT showed bilateral iliac and femoral expansion changes, with patchy low density shadow and ground glass density, and soft tissue density shadow in the right iliac bone
图2. CT示双侧髂骨及股骨膨胀性改变,内呈斑片状低密度影及磨玻璃密度,右侧髂骨内见软组织密度影
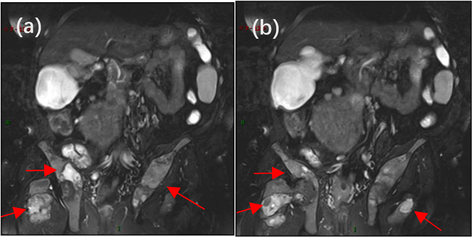
Figure 3. Magnetic resonance T2WI showed expansive changes in bilateral iliac bones and femurs, with patchy high and low mixed signals, and right iliac bones with mass soft tissue shadows.
图3. 磁共振T2WI示双侧髂骨及股骨呈膨胀性改变,内见斑片状高低混杂信号,右侧髂骨为著并见团块状软组织影
1.5. 超声
宫体(位置高,位于脐上约三横指):长8.9 cm,宽8.4 cm,厚8.6 cm。子宫大、形态饱满,后壁见低回声团块,大小约2.8 cm × 3.3 cm × 2.3 cm,界欠清,略外突,回声不均;余肌层回声增粗、不均匀,以后壁为著,宫腔线不清晰,内膜厚约0.8 cm。宫颈见多个囊性结节,较大者1.4 cm × 0.8 cm × 0.7 cm,界清,内透声好,后方回声增强。宫体右上方见囊性回声,大小约11.4 cm × 7.1 cm × 6.1 cm,界清,透声可,内见分隔;宫体左侧见囊性回声,大小约3.8 cm × 3.5 cm × 3.3 cm,界清,透声可(见图4)。
1.6. 病理
检查所见:1) 全子宫+左侧输卵管,已剖开,宫体大小:12 × 10 × 7 cm,宫颈管长3cm,外口直径2.5 cm,尚光滑,内膜厚0.1~0.2 cm,宫壁厚5~7 cm,结节状,局灶呈囊性,内容血凝块样物,左侧输卵管长7 cm,直径0.5 cm;2) 囊壁样组织一块,大小2.5 × 2.5 × 0.5 cm,内壁光滑,壁厚0.1~0.2 cm。病理检查结论:石蜡切片:1) (右附件)输卵管组织伴系膜囊肿形成;卵巢组织伴囊肿(内衬单层立方及纤毛柱状上皮)形成;2) 子宫腺肌病;3) 增生期子宫内膜;4) 左侧输卵管组织伴血管扩张、充血并出血;5) (左卵巢)单纯囊肿。
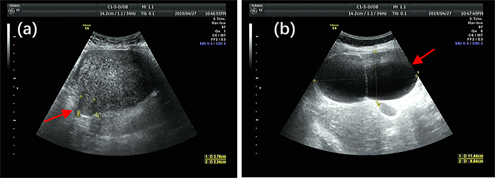
Figure 4. (a) Ultrasound posterior uterine fibroids; (b) Cyst on the upper right side of the uterine body
图4. (a) 超声子宫后壁肌瘤;(b) 宫体右上方囊肿
2. 讨论
2.1. 病理机制
McCune-Albright syndrome综合征(MAS)是由激活GNAS位点突变引起的典型疾病。G蛋白偶联受体(GPCR)及其配体,已被确定为成骨细胞形成和功能的关键调节因子,这是正常骨形成和体内平衡的两个关键步骤。人类GPCR家族包括超过340个非嗅觉受体和400个嗅觉受体 [1] [2] ,使其成为人类基因组中最大的受体类别。GPCR介导多种生物过程,并被多种类型的细胞外信号激活。GPCR的多样性及其对小分子的反应使其成为超过40%的现代药物的主要靶点 [3] 。GPCRs通过几种典型途径发出信号 [4] :其中,Gs和Gi通路分别通过作用于腺苷酸环化酶而增加或降低细胞内cAMP水平,而Gq通路通过激活磷脂酶c而增加细胞内钙。MAS是一种遗传疾病,其特征是骨多骨纤维发育不良(FD)、皮肤色素沉着和外周性性早熟。MAS患者可能患有其他内分泌疾病,包括库欣综合征、甲状腺功能亢进、肢端肥大症和乳腺、甲状腺和胰腺的实体器官恶性肿瘤。FD/MAS是由GNAS的获得性体细胞突变引起的,该基因编码刺激g蛋白(Gsα)的α亚基,导致受影响细胞中gs信号的组成性激活。这种突变发生在合子后,导致组织嵌合体,而不是通过种系遗传。由于这种嵌合体,FD的临床疾病范围从单一骨骼受累到多器官受累。最常见的原因是c.602G > a (p.R201H)或c.601C > T (p.R201C)位置的错义突变。这种突变导致Gsα蛋白的GTP水解酶结构域的氨基酸替代,抑制了内在的GTP酶活性,并导致细胞内cAMP水平持续升高。
2.2. 临床表现
(1) MAS的内分泌功能亢进主要表现为:促性腺激素非依赖性性早熟(外周性性早熟),该表现最为常见及典型,同时会导致提早出现第二性征。女孩子宫或卵巢较正常同龄儿大、阴道不规则出血过早出现并常伴复发性卵巢囊肿;男孩性早熟主要表现为阴茎增长和继发于睾丸间质细胞增生所致的双侧睾丸增大 [5] 。此外部分患者会伴有甲状腺功能亢进、生长激素升高或生长激素伴催乳素混合性升高。MAS也包括一些非内分泌病变,如心血管、肝脏、肾脏疾病等,病情比较复杂 [6] [7] 。
(2) 骨纤维异常增殖症,常多发,主要位于单侧,不会跨中线生长,X线摄影表现为多发类椭圆形或梭形骨质膨胀区,相应部位骨皮质变薄,其内密度呈磨玻璃、“丝瓜瓤样”或“地图样”改变。最常见于颅面骨和股骨近端 [8] 。临床会出现患侧肢体疼痛,活动障碍及病理性骨折,大部分患者常合并脊柱侧弯畸形;
(3) 皮肤咖啡色素斑,常位于发生骨质损害的同侧,一般不跨中线生长,边缘模糊不清,不高出皮肤,具体表现为一处或多处边界不规则、点片状大小不等、深黄色或黄棕色改变。典型三联征者比较少见约占24%,二联征者约占33%,三联征中的一种体征者约占40%。
2.3. 诊断
2019年,FD/MAS国际联盟发表相关指南,以帮助指导临床医生对FD/MAS的诊断和管理 [8] 。诊断FD/MAS的第一步是进行完整的骨骼和骨骼外评估,以确定疾病的程度。如果患者有FD并至少有一种骨骼外表现(皮肤色素沉着,外周性性早熟,甲状腺病变符合FD/MAS,生长激素过量,新生儿高皮质醇症)或没有骨骼受累,但有2种骨骼外表现。FD/MAS的准确诊断通常可以在完整的体格检查,结合骨骼、皮肤和内分泌系统的生化、激素和放射学评估后做出。只有在诊断不确定(即非典型放射学特征)或担心潜在恶性肿瘤时,才需要对FD病变进行活检。在这些情况下,可以检测受影响组织是否存在GNAS激活突变。如果样本具有较低的突变负担,则可能发生假阴性。由于疾病的嵌合性,外周血通常不足以用于诊断。下一代测序与较低的假阳性率相关。
2.4. 治疗
MAS的预后差异较大,因内分泌异常的程度、范围及病变骨受累的部位、程度而异。MAS的治疗主要是对症治疗,目前尚无有效根治该疾病的方法。儿童性早熟情况虽然对于月经后期及生育情况没有明显影响,但是会导致骨骺提前闭合,影响儿童生长发育。对于伴有骨折的患者,对症治疗,可以采用刮除术、手术矫正的方式进行治疗。对于患者日常生活的力量训练,如适当器械锻炼、游泳等均是很好增强肌肉训练的方式,可以有效减少患者骨折的风险。MAS的诊断需要临床医生对骨骼、内分泌、软组织、皮肤特征进行完整、全面评估后综合评判。
基金项目
济宁市重点研发计划(2023YXNS093)。
NOTES
*通讯作者。