1. 引言
在动物源食品日常检测工作中,我们日常监测的指标经常包含有氯霉素、氟甲砜霉素和五氯酚,结果显示,在动物源食品中三种药物时有被检出。氯霉素和氟甲砜霉素同属于酰胺醇类药物 [1] ,五氯酚作为除草剂类农药,由于这几种药物的不同功能在动物养殖过程中被广泛应用,在动物体内残留蓄积,被人过量食用后,会毒害人体的不同器官。在近几年的兽药残留抽检中,连续几年在蜂蜜检出氯霉素、在鸡蛋和腊肠等食品中检出氟苯尼考、在水产品,猪肝,猪肉,牛肉中检出五氯酚和超范围使用的情况,不合格率在3~4%左右 [2] 。在不同国家和地区对3种药物在动物源食品中的限量也作了明确规定,氯霉素、五氯酚为禁止使用的化合物。氟甲砜霉素为在不同生物体内也做了不同限量的规定。
目前动物源食品中氯霉素、氟甲砜霉素、五氯酚药物残留的测定仪器方法主要有酶联免疫法、高效液相色谱法(HPLC法) [3] [4] 、气质色谱法(GC法) [5] [6] [7] 、液相色谱串联质谱法(HPLC-MS/MS法) [6] - [11] 等,液相色谱串联质谱法是目前能准确测定这几种物质的主要仪器方法,测定此类药物的前处理方法主要有液液萃取法,固相萃取法 [11] - [15] ,QuEChERS (quick, easy, cheap, effective, rugged and safe)法 [16] [17] 。因液液萃取法步骤繁琐,固相萃取法成本过高,随着不同种类的新型吸附剂的开发,QuEChERS法在近年来也逐渐在兽残工作中得到应用,C18和具有良好除脂能力,但是针对性较差,在去掉基质干扰物的同时也会吸附目标物。已有研究表明,一些新的材料凭借其某些特殊的性能被用来作为新型吸附剂用于农残,抗生素和激素残留的检测。其中增强型脂质去除吸附剂(EMR)作为一种新型的吸附剂,采用特殊聚合物基质专门吸附脂质中C5及以上的碳链,能够有效地吸附脂肪类物质,大大降低样品的基质效应 [18] 。
现有国标检测方法采用不同的前处理过程,动物源食品中氯霉素和氟甲砜霉素的测定采用乙腈提取,正己烷净化,再过LC硅胶柱后上机检测,五氯酚是用碱性乙腈提取,过MAX柱子净化后,浓缩,定容后上机检测,整个检测过程时间繁琐,试剂成本高,采用固相萃取的净化方式虽然净化效果好,但是难以满足大批量样品测定,日常检测工作效率无法有效提升。鉴于上述原因,考虑到这3种物质都采用电喷雾负离子扫描模式测定,性质相似,本文希望以液相色谱串联质谱法为主要仪器设备,以QuEChERS法结合EMR吸附剂作为前处理方法,建立一种能同时测定动物源食品中氯霉素、氟甲砜霉素、五氯酚的检测方法,能够准确定性和定量3种物质,并能够节省检测时间和检测成本,缩短整个检测流程,适合大批量样品的处理。本实验拟以动物源食品中鸡肉,猪肝,牛肉等基质为研究对象,通过优化前处理提取试剂,净化试剂的选择和用量,色谱条件,质谱条件,并考察基质效应的影响,验证本文提供的检测方法能够达到预期的效果。目前QuEChERS在兽残检测的领域应用没有被广泛地开发,也希望本方法的开发为兽药残留的检测提供一种新的应用。
2. 实验部分
2.1. 主要仪器与试剂
1) 仪器配置:AB4500高效液相色谱质谱联用仪配ESI源,美国AB公司;CP512型电子天平,感量为0.01 g,奥豪斯仪器(上海)有限公司;涡旋振荡器:Multi Reax型,德国海道尔夫(Heidolph)公司,SIGMA 3K15高速冷冻离心机,氮吹仪,KS-300EI超声波清洗器,色谱柱均为安捷伦液质专用柱。
2) 试剂耗材:氯霉素、氟甲砜霉素、五氯酚、氯霉素氘代同位素内标标准物质、氟甲砜霉素同位素内标(纯度均大于99.0%,北京坛墨质检有限公司)。本实验所用的试剂材料都是实验室统一采购,其中甲酸、甲醇、乙腈为色谱纯试剂,生产厂商为阿拉丁;氯化钠、硫酸镁等为分析纯试剂,生产厂商为科隆化工;增强型脂质去除吸附剂:安捷伦科技股份有限公司;十八烷基硅烷键合硅胶(C18)和乙二胺-N-丙基硅烷化硅胶(PSA):上海规格为40 μm~60 μm,本实验所用样品鸡肉、牛肉、猪肝均来自日常检验样品。
3) 储备液的配制:分别精密称取氯霉素、五氯酚、氟甲砜霉素标准品适量,用甲醇溶解定容至50.00 mL容量瓶,标准储备液浓度为500 μg/mL,−18℃保存。
4) 应用液的配置:精确吸取氯霉素和五氯酚1.00 mL,氟甲砜霉素10.00 mL标准储备液(500 μg/mL)于同一100 mL容量瓶中,混匀后用50%甲醇水溶液定容,得到氯霉素和五氯酚5.00 μg/mL,氟甲砜霉素50.0 μg/mL混合标准溶液。
5) 基质溶液的配置:用空白样品基质稀释配制成不同浓度系列的混合标准工作液,其中氯霉素和五氯酚为0.5 ng/mL,1.00 ng/mL,2.00 ng/mL,5.00 ng/mL,10.0 ng/mL,氟甲砜霉素为5 ng/mL,10.0 ng/mL,20.0 ng/mL,50.0 ng/mL,100 ng/mL。
6) 内标的配制:分别精密称取氯霉素D5内标和氟甲砜霉素D3内标1 mg,置于100 mL容量瓶中,加甲醇溶解并稀释至刻度,配制成氯霉素D5和氟甲砜霉素D3 10.0 μg/mL的混合溶液,准确吸取1.00 mL置于100.0 mL容量瓶中,用甲醇稀释至刻度,摇匀,制成1.00 ng/mL的标准应用溶液,在每个基质标液中加入100 μL内标溶液,内标最终浓度为10.0 ng/mL。
7) 空白溶液:除不加试样外,均按试样同法操作,作为空白溶液。
2.2. 仪器工作条件
2.2.1. 色谱条件
色谱柱为Agilent EclipsePlus-C18柱(2.1 mm × 100 mm, 1.8 mm),流动相:A:水,B:乙腈,梯度洗脱见表1。流速:0.250 mL/min,温度:30℃,进样量:5 μL。

Table 1. Gradient elution conditions
表1. 梯度洗脱条件
2.2.2. 质谱条件
离子源:电喷雾离子源(ESI);离子源极性:负离子模式;检测方式:多反应检测(MRM);
毛细管电压:4.0 kV;雾化器(N2)压力:50 psi;干燥气(N2)温度:350℃;干燥气(N2)流速:10 L/min,见表2。

Table 2. Triple quadrupole ion pairs and related voltage parameter settings
表2. 三重四极杆离子对及相关电压参数设定表
注:*为定量子离子。
2.3. 实验步骤
2.3.1. 样品预处理
称取2 g (准确至0.05 g)样品于50 mL离心管中,准确加入混合内标100 μL,剧烈振荡2 min,加入15 mL 1%的甲酸乙腈溶液,超声提取10 min,然后8000 r/min离心3 min,取上清液于另一50 mL离心管中,加入1 g EMR吸附剂,旋涡1 min,然后8000 r/min离心3 min,取上清液各加2 g氯化钠和无水硫酸镁,振荡混匀100 s,然后8000 r/min离心1 min,收集上清液在40℃下用氮气吹至近干,加入1 mL 1%的甲酸乙腈复溶,旋涡30 s,过0.22 μm有机滤膜上机。
2.3.2. 定量方法
本方法定量采用内标法和基质曲线相结合的方法进行定量,其中氯霉素和氟甲砜霉素采用同位素内标,五氯酚采用外标法进行定量,主要是因为实验室没有五氯酚内标物质,以猪肝为基质作为考察对象,经过本方法前处理后,在最后加入复溶液中加入20 ng/mL混合标液,并与定溶液配制的20 ng/mL混合标液进行比较,结果表明,经过本方法处理的样液,各药物的基质效应0.70 ≤ M ≤ 1.0,说明本方法的前处理能有效降低基质效应,能够获得更准确的定量结果。
3. 结果与讨论
3.1. 提取剂的优化
动物源食品中主要来源于饲养动物和水产类动物的可供人食用的肉、蛋、乳及其制品和副产品,基质复杂,主要含有脂肪、蛋白质、脂肪、矿物质、维生素素等内源性物质 [19] ,一定程度上干扰目标物的分析,3种药物属于弱极性化合物,易溶于有机溶剂。本实验比较了乙酸乙酯、甲醇、乙腈、1%甲酸乙腈,1%甲酸甲醇5种不同提取溶液见表3。其中1%甲酸乙腈在提取3种目标物时效果最好,甲醇、乙酸乙酯、1%甲酸甲醇提取液比较浑浊,共萃物较多,乙腈提取液五氯酚的回收率只有20%左右。乙腈作为提取试剂对提取氯霉素和氟甲砜霉素没有影响,但是对提取样品的中的五氯酚有较大的影响,主要是因为样品中的五氯酚通常以五氯酚酸钠的形式存在,五氯酚酸钠易溶于水,在酸化条件下转化为五氯酚,五氯酚则难溶于水,易溶于有机试剂。实验证明当样品中加入1%甲酸乙腈,五氯酚的提取效率比纯乙腈高了60%。纯乙腈作为提取溶剂不能兼顾五氯酚和氯霉素、氟甲砜霉素的提取效率。因此本实验采用1%甲酸乙腈作为本实验的提取溶液。

Table 3. Comparison of recovery rates of five extractants in different matrices
表3. 不同基质中五种提取剂回收率的比较
3.2. 净化条件优化
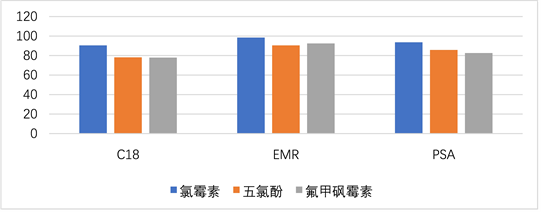
Figure 1. Comparison of spiked recovery rates of three purification agents in pig liver
图1. 猪肝中3种净化剂的加标回收率的比较
本实验通过加标回收率考察了C18,EMR,PSA,这3种常用净化剂的净化效果。结果表明:在鸡肉中适量的C18,EMR,PSA均能起到比较好的净化效果,回收率在90%以上,但是在猪肝等脂肪含量高的样品中,EMR净化剂展现的净化效果远超于C18和PSA,为了更好兼顾不同基质的净化效果,本实验选择EMR作为本实验的净化剂。为了进一步考察了不同添加量的净化效果,分别比较了在20 mg/L的混合标准溶液中添加EMR 1~5 g,结果表明:加入1 g EMR基本能满足肝脏类样品的净化。所以本实验最终确定加入1 g EMR吸附剂作为最终的添加量。具体见图1。
3.3. 色谱条件优化
3种目标物均为弱极性和中等极性化合物,本实验利用现有的柱子考察了Agilent EclipsePlus-C18柱(2.1 mm × 100 mm, 1.8 mm),Hypersil GOLD C18 (100 mm × 2.0 mm, 1.9 mm)和Agilent ZORBAX SB-C18 (2.1 × 100 mm, 1.8 mm) 3种色谱柱的分离效果,发现两3种柱子都能分离出目标物,获得满意的色谱图,Agilent EclipsePlus-C18柱的目标物出峰时间更短,从节约时间的角度考虑。选择了Agilent EclipsePlus-C18柱色谱柱作为分析柱。
本实验比较了甲醇水、乙腈水、乙腈乙酸铵、甲醇乙酸铵常用的适合负离子的流动相体系,结果发现,乙腈–水和乙腈乙酸铵体系,峰型比甲醇体系的更尖锐,分离效果更好,响应值更高,考虑到试剂成本的问题,选择乙腈水能满足本实验的分离要求。
3.4. 质谱条件优化
质谱条件的优化是考虑到不同仪器的性能,以及现有仪器的状态会对目标物的响应产生较大的影响,为了提高分析的灵敏度,将3种药物混合标准溶液稀释成200 ng/mL的浓度,用0.1 mL/min的流速将目标物注入电喷雾离子源,通过优化仪器的不同的参数,着重优化了影响目标物响应的去簇电压和碰撞能,使3种物质在负离子模式下响应最优,具体参数见表2。
3.5. 线性范围、回归方程、检出限和定量限
用空白基质溶液配制一系列浓度,绘制标准工作曲线,以定量离子响应3倍信噪比和10倍信噪比分别确定方法的检出限和定量限,通过表4可以看到3种药物在各自线性范围内相关系数 ≥ 0.995以上,线性相关良好,检出限,定量限,具体见表4,灵敏度满足实际检测的需要。

Table 4. Retention time, regression equation, correlation coefficient, linear range, detection limit (LOD) and quantification limit (LOQ) of three drugs
表4. 3种药物保留时间、回归方程、相关系数、线性范围、检出限(LOD)及定量限(LOQ)
3.6. 方法回收率和精密度验证
选取牛肉、猪肝不同基质阴性样品按上述方法进行操作,分别进行三水平六次重复性加标回收试验,其中,牛肉中氯霉素的回收率90.4%~105.8%,RSD为3.39%~5.49%,氟甲砜霉素的回收率80.0%~99.8%,RSD为1.10%~3.60%,五氯酚的回收率64.0%~84.4%,RSD为3.10%~7.10%,猪肝中氯霉素的回收率91.4%~102.3%之间,RSD为0.96%~2.36%,氟甲砜霉素的回收率83.9%~100.4%,RSD为1.90%~3.60%,五氯酚的回收率64.0~81.5%,RSD为3.10%~7.10%;具体见表5,表6。

Table 5. Recovery rates and relative standard deviations of three drugs in beef (n = 6)
表5. 牛肉中3种药物加标回收率和相对标准偏差(n = 6)

Table 6. Recovery rates and relative standard deviations of three drugs in pig liver (n = 6)
表6. 猪肝中3种药物加标回收率和相对标准偏差(n = 6)
3.7. 方法专属性
方法对比了空白样品和加标样品的离子提取色谱图(图2),图谱显示,空白样品中没有目标物的干扰,目标峰色谱图清晰无干扰。
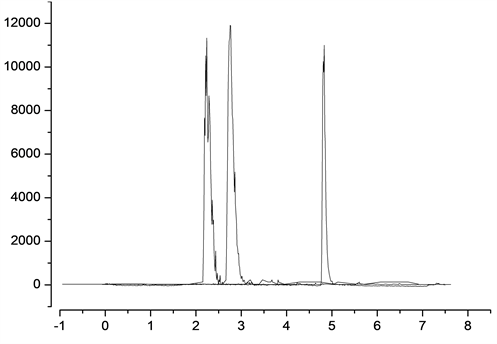 注:从左到右分别是五氯酚、氟苯尼考和氯霉素。
注:从左到右分别是五氯酚、氟苯尼考和氯霉素。
Figure 2. Standard extraction ion chromatography
图2. 标准提取离子色谱图
4. 结语
本文研究的内容是来自于平时检验技术的积累和总结,在日常检验工作中繁琐的前处理过程会严重影响实验室的效率和批量处理样品的速度,本方法的开发基于实验室现有的技术条件,仪器设备条件,检验日常工作的需求,对现有国标GB3168.20-2022,GB23200.92-2016进行方法优化和改良,本实验建立的基于LC/MS法快速测定动物源食品中3种药物残留检测方法,通过1%甲酸乙腈分步提取,提取剂用EMR吸附剂净化,在负离子模式下进行定性和定量分析,能显著降低样品的中基质效应,准确测定动物源食品中氯霉素、氟甲砜霉素和五氯酚的残留含量,本方法前处理简单,重现性好,回收率高。本方法由于缺少五氯酚内标物质,没有对五氯酚内标方法进行验证,从五氯酚的回收率和不同基质响应来看,五氯酚的基质效应非常强,特别是肝脏样品中回收率较低,所以建议有条件买到五氯酚内标的实验室尽可能添加五氯酚内标进行检测。
NOTES
*通讯作者。