1. 引言
门静脉狭窄(portal vein stenosis, PVS)是肝移植术后常见血管并发症之一。活体肝移植中,供体与受体门静脉管径不匹配会发生PVS,严重时致门静脉血流量明显降低,影响肝再生与功能,甚至导致移植后的肝失功或受体死亡 [1] 。门静脉血流动力学变化,尤其是壁面切应力,在血管疾病中对内皮功能产生不利影响。内皮功能障碍和异常血流动力学改变在门静脉高压症中起重要作用,门静脉高压症可能导致门静脉相关疾病,如门静脉血栓形成 [2] 。然而,关于门静脉系统中流量的分布、壁面切应力的分布,在临床医学测量上具有很大的局限性。彩色多普勒超声是临床监测PVS的重要手段,其具有快速、可重复性好、可进行非侵入性的连续测量等特点 [3] 。但是其只能对门静脉主干位置处血流速度进行监测,而对于门静脉二级分支,由于血管过细,如通往左右肝叶门静脉左右分支血流速度无法测得,且在PVS发展的初期,超声监测往往具有滞后性,无法及时监测到门静脉内的血流速度变化 [4] 。而PC-MRI计算血流速度的主要弊端是测量时间较长,并且由于磁共振的空间分辨率有限,在结构复杂的血管中,尤其是靠近血管壁的血流受到空间分辨率的影响,难以得到精确的速度信息。而计算WSS对靠近血管壁的血流速度精度要求很高,因此很多研究者采用了建立计算流体动力学(computational fluid dynamics, CFD)模型的方式,间接测量结构较为复杂的血管WSS [5] 。
计算流体动力学数值仿真在心血管疾病、颈动脉疾病和颅内动脉闭塞疾病的诊断中近年来发展迅速。通过求解具有一定边界条件的Navier-Stokes方程来测量虚拟血压梯度以及血流分布。基于计算流体动力学的血压梯度测量在颅内和冠状动脉(如心脏血流储备分数(FFR))评估方面取得了显著的成功 [6] 。但在肝血管系统的研究较少,可能有两个主要的原因。首先,精确的CFD模拟高度依赖于血管解剖的精确重建和流入速度的测量,但肝静脉和门静脉的解剖结构获取具有难度。其次,由于肝血管及其门静脉结构复杂,计算效率是其应用于临床常规的另一个限制因素。
如今,在有关肝脏及门静脉的相关研究中,已经证实了门静脉整体流量分布对于门静脉高压以及相关肝脏疾病研究的重要性 [7] 。在Joseph N. Benoit等人的研究中,就证实了大鼠门静脉狭窄模型中“向前”和“向后”的血流机制对门静脉压力增加的贡献 [8] 。在已进行的门静脉数值模拟相关研究中,基于CFD技术来对肝移植术后的门静脉狭窄病例治疗管理的相关研究已经在进行 [3] ,在Svetla Petkova等人的研究中,借助CFD技术分析了门静脉高压有无血栓形成情况下的血液流动状态 [9] 。但是还未有人结合数值模拟技术针对不同狭窄程度的大鼠门静脉的血流分布及壁面切应力分布进行研究,且门静脉狭窄后的血流分布及壁面切应力分布在医学诊断和病情发展过程中起着至关重要的作用。
本文以五组不同狭窄程度下的大鼠门静脉为例,应用有压管道流动CFD模拟技术对不同狭窄程度下的大鼠肝门静脉血液流动进行数值仿真,并利用医学多普勒实测正常大鼠门静脉主干流速进行了验证。基于医学CT影像与超声实测以及CFD数值模拟技术分析了五种不同狭窄程度下大鼠门静脉血流分布以及壁面切应力分布的变化。
2. 实验和方法
2.1. 不同程度PVS大鼠医学生成方法
选取健康成年SPF级雄性SD (Sprague-Dawley)大鼠10只作为实验对象,7~14周龄,体重约为200~400 g,饲养于四川大学华西科技园动物实验中心,饲养间恒温(23℃~25℃),12 h明暗交替。且给以其一周自适应的时间。
所有动物模型的建立由同一经验丰富的外科医生在无菌条件下完成。参照HIGGINS等介绍的手术方法进行70%肝切除手术,游离门静脉和肝周韧带后,切除肝中叶及左外叶,并用电子天平称量切除肝脏湿重。术后1 h皮下注射50 U的低分子肝素。肝切除后不同程度PVS模型制备,切除肝脏后游离门静脉主干,于门静脉入肝分支以下、脾静脉与门静脉汇合处近心端约2 mm处,以微血管测量尺测量预结扎部位门静脉管径,根据拟制作PVS程度计算狭窄处管径,据此选取不同型号针头,用丝线将门静脉与针头作为整体一同结扎,之后快速旋转抽出针头,此时门静脉管径即为针头外径,从而建立不同程度PVS [10] 。
最终选择中度狭窄范围内的大鼠门静脉狭窄率分别为57%、60.4%、61.39%、62.55%、64.13%的五组进行CFD数值仿真研究。
2.2. 大鼠门静脉CT影像及超声流速获取过程
1) 影像
为了得到清晰的造影图像,本研究向大鼠门静脉打入了造影剂,采用Philips iU22超声诊断仪,高频探头L12-5,频率5~12 MHz,对中度PVS组大鼠于术后1天分别随机选取6只行肝脏及门静脉扫查。
2) 边界条件
为了得到提取门静脉入口流量数据,先是在CT图像上由一个有经验的放射科医生手工标记出正常组及各PVS组门静脉入口位置横截面,采用频谱多普勒对各PVS组分别测量其截面处最大值流速值,测量时根据血管走行方向和内径调节取样容积为0.5 mm,在不产生噪音信号前提下将增益调至最大,矫正声束与血流之间夹角 < 60˚,门静脉入口截面流速均由一个有经验的放射科医生采用盲法进行扫查,所有结果测量3次取平均值。并通过Poiseuille定律将其整个截面流速分布离散出。
3) 验证条件
与提取门静脉入口流量数据类似,采用频谱多普勒对正常组及各PVS组分别测量狭窄处截面和狭窄前截面最大流速,并计算PVVR:PVVR = 狭窄处截面最大流速/狭窄前截面最大流速。测量时亦采用上述方法,所有结果测量3次取平均值。
2.3. 基于CT影像的三维建模技术
CT数据以医学数字成像和通信(DICOM)格式传输并分析。门静脉周围血管分布复杂,肝静脉等会对其提取造成干扰,该研究中门静脉模型由人工手动还原提取。
通过CT提取大鼠门静脉及其周围毛细血管左右支干。由于CFD数值仿真在很大程度上取决于几何形状,因此重建大鼠门静脉模型的策略在我们的工作中是基础和原创的。结合医学经验以及已进行的CFD数值仿真结果,门静脉一级分支以下分支及周围毛细血管对门静脉狭窄结果判定影响很小,因此在该研究中通过模型简化只保留了门静脉主干以及左右两个一级分支作为出口。且在造影质量较差的区域根据大鼠门静脉实际体型对其进行人工修复,修复的首要准则是尽可能还原实际模型的真实性,避免人为操作对模型的影响。最终得到的计算模型如图2所示,提取模型的过程如图1所示(以正常大鼠门静脉模型为例)。
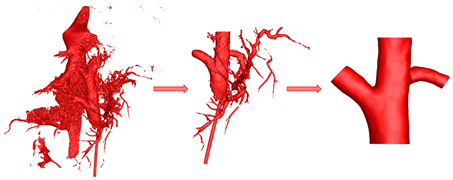
Figure 1. Extraction process of normal rat portal vein model
图1. 正常大鼠门静脉模型提取过程图
通过CT提取大鼠门静脉及其周围毛细血管。由于CFD数值仿真在很大程度上取决于几何形状,因此重建大鼠门静脉模型的策略在我们的工作中是基础和原创的。结合医学经验以及已进行的CFD数值仿真结果,门静脉一级分支以下分支及周围毛细血管对门静脉狭窄结果判定影响很小,因此在该研究中通过模型简化只保留了门静脉主干以及左右两个一级分支作为出口。且在造影质量较差的区域根据大鼠门静脉实际体型对其进行人工修复,修复的首要准则是尽可能还原实际模型的真实性,避免人为操作对模型的影响。最终得到的计算模型如图2所示。

Figure 2. From left to right, normal, 57% and 62.55% stenotic portal vein models in rats
图2. 从左至右依次为大鼠正常、57%以及62.55%狭窄门静脉模型
2.4. 数值模拟
2.4.1. 控制方程
我们的研究应用了一个假定为静止不可压缩流体的三维N-S方程,如下所示:
(1)
(2)
其中u为流速,p为压力,μ为动态粘度,ρ为血液的密度,假设血液为牛顿流体,μ = 0.0035 Pa∙s,ρ = 1060 kg/m3。F是体积力向量,当我们忽略血液的重力时,F被设为0。公式1表示牛顿第二定律的动量守恒,公式2表示连续性的约束,这是不可压缩流体。
由于雷诺数比较小,经计算最大雷诺数约为1059,我们在这里只使用层流模型,而不是湍流和非牛顿模型,或流固耦合(FSI)模型。另一方面,虽然在CFD模型中,血管的几何形状非常重要,而且不可否认,使用FSI会更加精确,但PVS病理模型的管壁顺应性明显降低,使得我们的刚性管壁假设更加合理和高效。
2.4.2. 边界条件
入口为门静脉入口,通过盲法扫查,结果测量3次取平均值,最终确定57%、60.4%、61.39%、62.55%、64.13%狭窄率门静脉模型入口截面最大流速分别为13.6 cm/s、12.1 cm/s、12.3 cm/s、13.9 cm/s、10.9 cm/s。
出口是门静脉上支左右一级支干作为出口,这里设置了参考压力。由于HVPG是根据气球充气前后的压差计算的,所以它与参考压力的绝对值无关。为了与临床测量相似,并遵循生理条件,将出口压力定值设为0 mmHg。
2.4.3. 网格的绘制
以正常大鼠门静脉模型为例,将之前已经处理好的三维门静脉模型导入ICEM CFD 2021 R1中进行处理。根据此门静脉模型整体实际尺寸,设置网格最大可能尺寸为0.1 mm,限定网格最小尺寸为0.02 mm,且在门静脉血管壁边界处采用多层加密六面体网格,便于更准确地捕捉相关边界层的数值。最终用约为538,848个网格点和1,317,948个网格(其中包含四面体和六面体网格)将正常大鼠三维门静脉模型划分完成,见图3。

Figure 3. Schematic diagram of portal vein grid in normal rats
图3. 正常大鼠门静脉网格示意图
2.4.4. 求解器
使用了Ansys Fluent的层流流体模块进行有限元模拟。且使用了基于压力的直接求解器来计算该研究中的流体动力学模型。为了避免内存不足的错误,我们将迭代减少到10,000次。方程中有两个因变量耦合,即压力场和速度场。并利用代数多重网格(AMG)求解器在每个节点处求得这两个值。
3. 验证
以正常的大鼠门静脉模型为例,给出了其数值仿真的结果,结合管流层流的客观规律,并于医学上已经测得相关数据进行对比,其中包括门静脉主干流速分布,对该研究的可靠性进行验证,见图4、图5。
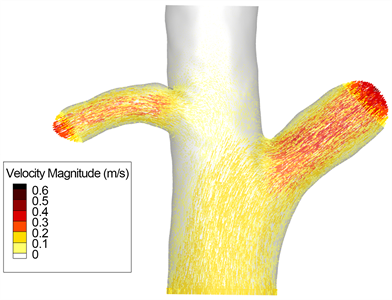
Figure 4. Flow velocity distribution of portal vein in normal rats
图4. 正常大鼠门静脉整体流速分布图
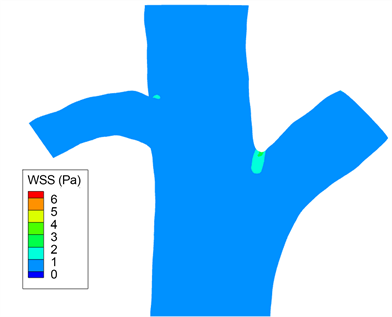
Figure 5. Wall shear stress distribution of portal vein in normal rats
图5. 正常大鼠门静脉整体壁面切应力分布图
1) 与经验公式比较
基于圆管层流的基本规律验证数值模拟大鼠门静脉血液流动的正确性,以正常大鼠的门静脉模型为例,我们可明显看出随着血液在静脉主干内的充分流动,整个门静脉血液流动满足Poiseuille分布,即在血管中心位置处血流速度较大,随着逐渐靠近血管边壁,受到血管壁粘滞力的作用,血流速度不断减小,并逐渐接近于0。且由图4可明显看出,正常大鼠的门静脉流动满足该层流客观规律。
2) 与彩色超声多普勒实测比较
分析正常大鼠的门静脉模型数值仿真的流量分布,进一步验证数值模拟的准确性。截取大鼠门静脉主干上最大流速截面可得到门静脉主干处最大流速为14.9 cm/s,超声实测得到的门静脉主干处最大流速为13.5 ± 1.3 cm/s,误差约为10.37%。实际上,数值模拟的结果和医学实测结果误差范围在30%以内,对于临床医学的参考就已具有重大意义。且在之前已进行过的研究中表明,正常SD大鼠门静脉流速为(15.60 ± 3.53) cm/s [11] 。以上均佐证了该数值模拟的可靠性。
经过验证发现大鼠门静脉数值模拟结果与医学实测结果高度吻合。说明了该研究通过数值模拟分析不同狭窄程度大鼠门静脉整体血流量及壁面切应力分布具有可靠性。且基于CFD技术的优越性,对于医学上不能测得或者不方便测得的整体流量分布及壁面切应力分布等数据,通过CFD技术可以方便快捷的获得,并且基于数值模拟得到的数据进行诊断和预测。
4. 结果与讨论
本节给出了正常组以及不同狭窄程度的大鼠门静脉仿真结果。且就大鼠门静脉狭窄程度的不同对门静脉整体流量分布以及整体壁面切应力分布的影响进行了讨论,在下面论述中,分别比较了正常组和大鼠PVS程度为57%、60.4%、61.39%、62.55%以及64.13%下的门静脉流量分布和壁面切应力分布,见图6~9,分析了不同PVS程度下大鼠门静脉上述指标的变化及可能对肝再生发育产生的影响。

Figure 6. Distribution of normal, 57% and 60.4% stenotic portal veins flow velocity in rats
图6. 大鼠正常、57%以及60.4%狭窄门静脉流速分布图

Figure 7. 61.39%, 62.55% and 64.13% stenotic portal veins flow velocity distribution in rats
图7. 大鼠61.39%、62.55%以及64.13%狭窄门静脉流速分布图
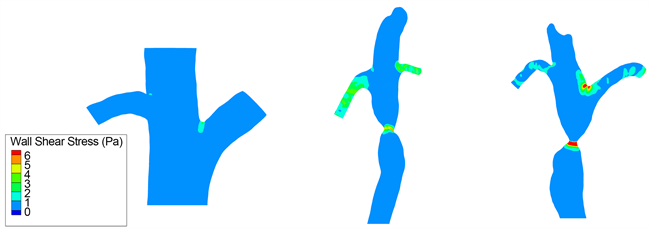
Figure 8. Distribution of WSS in normal, 57% and 60.4% stenotic portal veins in rats
图8. 大鼠正常、57%以及60.4%狭窄门静脉WSS分布图
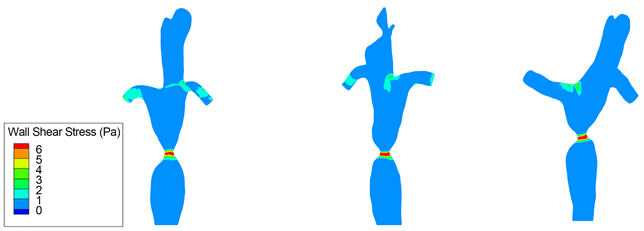
Figure 9. 61.39%, 62.55% and 64.13% stenotic portal veins WSS distribution in rats
图9. 大鼠61.39%、62.55%以及64.13%狭窄门静脉WSS分布图

Table 1. Summary of numerical simulated flow in the portal vein of rats with different degrees of stenosis
表1. 不同狭窄程度大鼠门静脉数值模拟流量汇总

Table 2. Summary of numerical simulated flow rates in the portal vein of rats with different degrees of stenosis
表2. 不同狭窄程度大鼠门静脉数值模拟流速汇总

Table 3. Summary of WSS for numerical simulation of portal veins with different degrees of stenosis
表3. 不同狭窄程度门静脉数值模拟WSS汇总
1) 狭窄程度对大鼠门静脉流量比的影响
由表1对不同狭窄程度大鼠门静脉血流量分布进行分析对比,不难看出,随着大鼠门静脉狭窄程度的增加,门静脉整体血流阻力增大,总体过血流量逐渐减少,正常大鼠与门静脉狭窄程度为57%、60.4%、61.39%、62.55%以及64.13%的门静脉总体过血流量依次为37.25 cc/min、25.66 cc/min、22.74 cc/min、19.18 cc/min、17.12 cc/min、15.99 cc/min。
正常大鼠门静脉右支与左支血流量比值一般在3~4之间。由表1分析在大鼠门静脉中度PVS发展过程中,门静脉右支与左支血流量比值相比于正常情况下是逐渐减小的,大鼠门静脉狭窄程度为57%、62.55%、64.13%的右支过血流量分别为19.69 cc/min、18.69 cc/min、16.81 cc/min,左支过血流量分别为12.45 cc/min、5.18 cc/min、4.05 cc/min,右支血流量所占比例越来越小,右支与左支流量的比值由正常大鼠门静脉的3.81逐步发展为2.25、1.93、1.75、1.68、1.47。
基于上述结果,我们可以合理分析,在大鼠门静脉处于中度狭窄情况下,随着大鼠门静脉狭窄程度的不断增加,门静脉总过血流量逐渐减少,由于门静脉左支与右支过血流量比值的不断减小,门静脉左支过血流量受到的影响较大,左肝叶供血不足的情况比较严重,而右支会相比于左支受到的影响会小一些。而这个结果也和人体病患门静脉高压彩色多普勒检测结果有着相同的原理 [12] 。
且基于数值分析软件对大鼠门静脉的狭窄程度与左右支流量比值进行相关性分析以及公式率定,最终得到如下结果:
其中p1 = 0.00066,p2 = −0.122,p3 = 7.398,p4 = −145.3。Z代表大鼠门静脉左支与右支的过血流量比值,X代表大鼠门静脉狭窄程度。和方差SSE = 0.002907,确定系数R2 = 0.9915。
2) 狭窄程度对大鼠门静脉PVVR比值的影响
狭窄处与狭窄前门静脉血流速度(portal venous velocity, PVV)比值(PVV ratio, PVVR)是诊断PVS的重要指标之一,PVVR ≥ 4:1时可以考虑PVS [13] 。由表2对不同狭窄程度大鼠门静脉流速分布进行分析对比,正常大鼠门静脉实际上没有狭窄部位,所以其前中后部位的流速是一样的,在14.0 cm/s附近波动。大鼠门静脉进入中度狭窄范围内后,可从图7明显看出,从大鼠门静脉入口到狭窄处,受到血流阻力的影响,门静脉会出现一定程度的膨胀。狭窄处的流速出现激增,大鼠门静脉狭窄程度为57%、60.4%、61.39%、62.55%以及64.13%的狭窄处最大流速分别为75.8 cm/s、72.7 cm/s、72.2 cm/s、74.5 cm/s以及80.3cm/s,流速并未随着狭窄程度的增大一直增加,是因为随着狭窄程度的增加,门静脉整体过血能力下降,过血流量亦随之减少。
正常大鼠门静脉的PVVR值一般在1附近,而当PVVR值大于4时可判定为门静脉狭窄。不同于流速,PVVR值作为一个比值,消除了因门静脉整体过血流量变小造成的影响,利用其讨论门静脉狭窄具有可靠性。大鼠门静脉狭窄程度为57%、60.4%、61.39%、62.55%以及64.13%的PVVR值分别为4.51、6.67、7.22、7.78以及8.40。随着门静脉狭窄的逐渐发展,PVVR值逐渐增大。
基于上述结果,我们可以合理分析,在大鼠门静脉处于中度狭窄情况下,随着大鼠门静脉狭窄程度的不断增加,门静脉狭窄处血流受到的阻力变大,过流不畅,导致狭窄前门静脉主干有所膨大,且流速滞缓,PVVR值也随之逐渐增大。
且基于数值分析软件对大鼠门静脉的狭窄程度与PVVR值进行相关性分析以及公式率定,最终得到如下结果:
其中a = −1.375e+09,b = −4.654,c = 13.76。Z代表PVVR值,X代表大鼠门静脉狭窄程度。和方差SSE = 0.001494,确定系数R2 = 0.9998。
3) 狭窄程度对大鼠门静脉切应力分布的影响
通过图7及表3对不同狭窄程度大鼠门静脉WSS分布进行分析对比,壁面切应力这一指标在医学实测过程中具体数值波动较大,通过现有测量手段很难得到其准确值,因此我们根据数值模拟结果这里对其进行分析。正常大鼠门静脉的主干壁面切应力在0.2 Pa附近波动,且分布均匀,无应力集中区,当大鼠门静脉狭窄发展到中度范围后,狭窄区域则会出现明显的应力激增,狭窄程度为57%、60.4%、61.39%、62.55%以及64.13%的狭窄处最大WSS分别为7.36 Pa、7.74 Pa、7.93 Pa、8.21 Pa和8.97 Pa,由此可见大鼠门静脉在中度狭窄范围内,门静脉最大值在7 Pa附近波动,且随着狭窄程度的逐步增加,狭窄处最大壁面切应力值也有所增大。
5. 结论
本研究基于大鼠门静脉医学实验和CFD数值模拟技术,对大鼠门静脉中度狭窄范围内狭窄程度分别为57%、60.4%、61.39%、62.55%以及64.13%的五组病理进行了研究。首先基于医学实验生成门静脉狭窄程度分别为57%、60.4%、61.39%、62.55%以及64.13%的大鼠门静脉模型,测得入口流速作为数值模拟的进口边界条件,且从CT图中提取出数值模拟计算所需门静脉模型,对所提取模型进行数值模拟的计算、结果验证以及结论分析总结。数值模拟结果发现血流动力学因素如流速、压力、壁面切应力、流动对壁面的冲击状况等因素与门静脉狭窄的发展密切相关,且门静脉狭窄程度的不同对门静脉左右分支过血流量以及左右肝叶的生长造成直接影响。最后根据数值模拟的结果率定出大鼠门静脉在中度狭窄范围内狭窄程度与左右分支过血流量比的函数关系,以及大鼠门静脉狭窄程度与PVVR值的函数关系。
NOTES
*通讯作者。