1. 前言
乙酰乳酸合成酶(Acetolactate synthase简称ALS或Acetohydroxyacid synthase,简称AHAS)活性抑制效果分析是揭示新研发抑制剂作用机理、评价抑制效果指标的试验方法之一。其中,离体法分析方法是常用的鉴定除草活性、作用机理的试验手段。
离体法ALS活性试验步骤比较繁琐、试验条件苛刻、费时费工。目前普遍接受的ALS活性检测步骤是由Ray T.B. (1984)提出的方法 [1],试验步骤包括低温提取植物体内含ALS蛋白质及蛋白质含量测定→试管内酶促反应→反应产物3-羟基丁酮的显色反应及吸光度测定步骤。其中,低温提取含ALS蛋白质提取步骤细分为定量取试验材料→加入液氮及缓冲液(提取液A)研磨→过滤→离心(15 K rpm)→提取上清液(粗蛋白)→半饱和态硫酸铵蛋白质沉淀→再次离心(20 K rpm,沉淀物为半精蛋白)→缓冲液(B)溶解→溶解液过柱(Sephadex G-250层析柱)→获得蛋白质溶液层(精酶)。
为准确、快速、简便测定新化合物的除草活性,作者检索、分析了国内为重点的近期抑制剂对ALS活性抑制效果相关的公开论文35篇的试验方法,发现多数论文采用了简化部分试验步骤的方法。在中国知网提供的国内离体法测定ALS活性论文35篇中,采用标准离体法测试步骤提取精蛋白测定ALS活性的论文3篇 [2] [3] [4],采用提取半精蛋白步骤测定ALS活性的论文14篇 [5],采用提取粗蛋白步骤测定ALS活性的论文2篇 [6] [7],同时加FAD和DTT配置缓冲液的3篇 [8] [9],只加DTT配置缓冲液的2篇 [10] [11],还有减低离心速度的、没详细叙述ALS蛋白提取过程的、没标注3-羟基丁酮的显色反应及吸光度空白对照的共14篇。
对此,本文为准确、简便、快速测定ALS活性,提供优化的试验方法及理论依据,分析了不同ALS酶蛋白提取方法提取的ALS蛋白对酶促反应结果的差异性,探讨了DTT替代FAD的可能性。
2. 试验材料与方法
2.1. 试验材料
ALS提取材料:福莱2号玉米杂交种。盆栽,置于恒温培养箱,在30℃条件下无光培养5 d,黄化幼苗作为提取ALS材料。
化学试剂:磷酸氢二钾,磷酸二氢钾,丙酮酸钠,FAD,TPP,DTT,MgCl2,H2SO4,肌酸,甲萘酚,氢氧化钠,标准蛋白质和3-羟基丁酮等。
ALS靶标除草剂:苄嘧磺隆,邻-XX基---(正在研发的新磺酰脲类抑制剂,由青岛科技大学团队提供)。两种除草剂处理剂量:2 µmol/ml
仪器:低温离心机(Allegra X-30R),气相色谱仪(GC-6890气相色谱仪),日立高效液相色谱仪(日本Hitachi公司),UV1102紫外分光光度计,超声波清洗机,Sephadex G-25层析柱(Sigma公司),控温光培养箱、恒温热水器以及其他常规设备仪器。
2.2. 试验方法
2.2.1. 离体法测定ALS活性
标准缓冲液试剂配制:参考吴等提出的方法配制 [4] pH 7.5的蛋白提取液缓冲液(buffer A)和pH 7.0的酶促反应缓冲液(buffer C)。含DTT缓冲液中的DTT浓度:0.1 mmol/L。
ALS提取:酶提取过程始终保持0℃~4℃下进行。取30℃暗培养7 d的玉米嫩芽2 g剪碎片放入研磨内,到入酶提取缓冲液A 12 ml,研磨至匀浆,滤纸过滤,在4℃离心(10 K rpm、30 min),取上部澄清液作为粗酶(粗蛋白);粗酶加同量饱和硫酸氨、再次离心(10 K rpm、30 min),用缓冲液A溶解沉淀物获得与粗蛋白等量的半精酶;半精酶过Sephadex G-25层析柱获得与粗蛋白等量的精酶。
蛋白定量:
1) 考马斯亮蓝的配制:参照Bredford的方法配制。
2) 蛋白质含量测定方法:将提取的粗酶液4 µl稀释50倍至200 µl,加入4 ml考马斯亮蓝工作液,37℃温浴30 min,冷却至室温,595 nm波长下比色,据标准曲线计算其浓度(µg/mL)。吸光值(Y)与蛋白质浓度(X)标准曲线数学模型:Y = 0.0022X − 0.0021,R2 = 0.9976。
ALS活性体外(in vitro)测定:参考吴明根等测定方法 [3] 将酶促反应–显色反应的样品在525 nm波长下比色,测定3-羟基丁酮含量表示ALS活性活性强度(μmolacetoin/mg protein∙h)。吸光值(Y)与3-羟基丁酮浓度(X)标准曲线数学模型:Y = 0.0092X − 0.0093,R2 = 0.9996。
其中:调零样品1 (CK0)是标曲无3-羟基丁酮显色液,调零样品2 (CK2)是酶促反应前加浓硫酸酶失活的反应–显色液。
2.2.2. 气相色谱法测定3-羟基丁酮产物
参照练敏、Yixiao Fan等提出的试验方法 [12] [13] 配制标准溶液,进样得到不同浓度3-羟基丁酮的峰面积,绘制标曲吸光值(Y)与3-羟基丁酮浓度(X)标准曲线数学模型(Y = 2E + 06X – 38045, R2 = 0.9984)。取分别含有DTT和FAD辅酶的ALS酶促反应样品0.1 ml用乙醇稀释至1 ml,然后根据样品色谱图中的3-羟基丁酮的峰面积计算其含量。
毛细管气相色谱柱:agiLent SE-54 (30 m, 0.32 mm)弱极性,气化室温度:150℃,检测器温度:200℃,柱温:50℃,维持3分钟,10度/分,升至150度。
2.2.3. 高效液相色谱法测定提取蛋白中的FAD含量
参照韦京豫等提出方法 [14] 配制FAD的标准溶液,进样得到不同浓度FAD的峰面积,绘制标曲吸光值(Y)与FAD浓度(X)标准曲线数学模型(Y = 212.2X + 7109, R2 = 0.9980)。取1 g样品加入6 ml超纯水研磨至匀浆,过滤,将液体10,000 r/min离心30 min,离心后留上清液作为ALS粗酶;粗酶加等体积饱和态硫酸铵沉淀,12,000 r/min离心15 min,超纯水溶解获得半精酶;半精酶过Sephadex G-25层析柱,超纯水定容至粗蛋白同量为精酶(精蛋白)。将粗酶、半精酶、精酶过滤膜后进行液相分析。
色谱柱:kromasiL-C18 (4.6 mm × 250 mm, 5 μm);检测器:紫外检测器;检测波长450 nm;流动相:甲醇–乙酸铵(35:65);流速1 ml/min;柱温为25℃。
3. 试验结果与分析
3.1. 不同提取过程的ALS蛋白量差异
以玉米暗箱培养的幼苗为材料,首先分别通过标准缓冲液(提取液)提取粗蛋白、半精蛋白、精蛋白,测定提取液蛋白质浓度结果(表1),均获得含有不同浓度蛋白质的提取液。统计分析结果,标准缓冲液提取的粗蛋白与精蛋白浓度有显著性差异(表1),说明随提取ALS蛋白过程的延长和精制,发生蛋白量的损失。相对粗蛋白,半精蛋白和精蛋白过程中蛋白损失率分别为13.4%和22.6%左右。

Table 1. Protein concentration of standard buffer and H2O extracts from maize seedling
表1. 玉米幼苗体内标准缓冲液和水提的蛋白质浓度
注:不同英文字母表示在0.05水平下的显著性差异,下同。
3.2. 粗蛋白ALS、半精蛋白ALS、精蛋白ALS的酶促反应效果
不同提取法提取的ALS蛋白作为催化酶进行离体法ALS酶促反应结果,检测到的反应液3-羟基丁酮含量与添加的蛋白提取类型不同有差异,同时吸光度调零样品的不同而出现很大差异(表2)。统计分析结果,总的酶促反应趋势为粗蛋白酶促反应体系中的3-羟基丁酮总量、蛋白质中固有的量、酶促反应生成的量以及ALS活性强度大于半精蛋白和精蛋白酶促反应体系,半精蛋白又大于精蛋白酶促反应体系;其次是不管粗蛋白还是半精蛋白、精蛋白,以CK0 (以标曲0点)调零测定和以CK2 (酶促反应前加浓硫酸酶失活)调零测定的正常酶促反应液的总量(CK1)、实际酶促生成量(CK4)有差异,当以CK0调零测定正常酶促反应液的总量(CK1)值应该是酶促反应前蛋白携带的固有量(CK2) + 实际酶促生成量(CK4)的总和值;CK2:CK4的量比大约为1:1,分别占酶促反应液总量(CK1)的45%和55%。
本文认为粗蛋白酶促反应体系3-羟基丁酮含量高的原因是半精蛋白和精蛋白精制过程中剔除了部分固有3-羟基丁酮和部分蛋白质,因此当同体积定容提取的粗蛋白、半精蛋白、精蛋白质溶液加入到反应液时,后两者附带进入酶促反应液的ALS蛋白和固有的3-羟基丁酮量少于粗蛋白,出现加粗蛋白的ALS催化酶反应体系中3-羟基丁酮总含量相对高的现象。

Table 2. Comparison of enzymatic reaction between crude protein, Semispermic protein and pure-protein ALS
表2. 粗蛋白ALS与半精蛋白、精蛋白ALS酶促反应效果的比较
注:CK1:以CK0 (以标曲0点)调零测定的正常酶促反应液样品;CK2:以CK0调零测定的酶促反应前预先加硫酸使酶失活的样品;CK3:以CK0调零测定CK1和CK2的3-羟基丁酮吸光值差代入3-羟基丁酮标曲数学模型公式计算的3-羟基丁酮量。CK4:以CK2 (酶促反应前加浓硫酸酶失活)调零测定的正常酶促反应液样品(CK1)。
由于作为ALS蛋白加入到酶促反应液的提取蛋白中存在携带的3-羟基丁酮,所以选择正确的525 nm吸光度调零样品是消除误差的关键。以已知特性的苄嘧磺隆和新合成的邻-XX基苯磺隆化合物作为ALS靶标除草剂,测定其抑制ALS活性结果(表3,表4),以标曲0点样品调525 nm吸光度零点测定时,抑制率值小于以加浓硫酸酶失活样品CK2调零的抑制率值(表3,表4)。理论上CK2反应体系中不能进行酶促反应,只存在蛋白携带的固有的3-羟基丁酮,因此以CK2调零测定的抑制率才能真实地反映抑制剂对ALS活性的抑制效果,当CK0调零测定时,相对CK2调零测定出现3-羟基丁酮含量值高而抑制率下降现象。
为了进一步验证是否在提取的粗蛋白溶液中存在3-羟基丁酮,采用气相色谱法测定玉米粗蛋白ALS酶促反应的3-羟基丁酮含量。测定结果(表5),酶促反应预先停止的CK2反应液能够检测出比较高浓度的3-羟基丁酮,含量接近正常酶促反应结束的(CK1)的60%左右,统计分析结果,酶促反应前后的三羟基丁酮含量有显著性差异而DTT和FAD缓冲液之间没有显著性差异。

Table 3. Comparison of inhibitory effect of inhibitors under different zero setting conditions
表3. 在不同调零条件下抑制剂抑制效果的比较

Table 4. Influence of different blank samples for zero-adjusted on determination value of 3-hydroxybutanone
表4. 不同空白样品调零对抑制率测定值的影响
注:*表示横向比较的显著性差异。

Table 5. The content of 3-hydroxybutanone in the reaction solution of crude protein extracted from corn was added
表5. 加入玉米粗提取蛋白的反应液3-羟基丁酮含量
3.3. DTT替代FAD辅酶缓冲液的可行性分析
二硫苏糖醇(Dithiothreitol,简称DTT)是氧化还原功能类似于辅酶FAD的一种结构简单的有机小分子(图1),常作为巯基化DNA的还原剂和去保护剂,在DNA溶液中加入DTT可以降低DNA的二聚化,DTT也常常被用于蛋白质中二硫键的还原,可用于阻止蛋白质中的半胱氨酸之间所形成的蛋白质分子内或分子间二硫键 [15] [16]。试验结果,采用仅含有DTT的缓冲液(包括提取缓冲液A、酶促反应缓冲液C)提取粗蛋白,进行酶促反应也能催化生成3-羟基丁酮(表6),统计分析结果,两种体系提取、反应的粗蛋白固有的3-羟基丁酮含量CK2之间、酶促反应生成量CK4之间差异不显著。
上述试验结果,DTT代替FAD的酶促反应也能检测出3-羟基丁酮。常理认为FAD作为ALS的辅酶与ALS蛋白牢牢结合在一起,在蛋白质提取过程中不容易两者分离,不能排除提取蛋白中含有FAD的可能性。对此采用高效液相色谱法,测定了以纯水作为提取液提取玉米幼苗粗蛋白、半精蛋白、精蛋白中的FAD含量。试验结果,粗蛋白、半精蛋白、精蛋白提取液中,确实含有痕量的FAD (表7),其含量相当于加入缓冲液添加FAD浓度(FAD 10 μmol/L)的1/10量,半精蛋白中含有1/1000、精蛋白中含有1/3000量。

Table 6. Comparison of effects of between the FAD buffer and DTT buffer on the ALS enzymatic reaction
表6. 含FAD、DTT缓冲液对ALS酶促反应效果的比较

Table 7. Content of FAD in crude protein, Semispermic protein and pure protein extracted from maize seedlings by water
表7. 水提取玉米幼苗粗蛋白、半精蛋白、精蛋白中的FAD含量
由于FAD作为ALS辅酶分子在ALS活性中心与特定位置的氨基酸残基分子对接,对接亲和力、稳定性强(图1(A)、图1(B)),所以本试验的离心速度、蛋白质沉淀过程、过柱等分离方法很难从蛋白质中分离除掉对接的FAD分子。所以目前的研究结果不能完全认定DTT完全取代FAD空间位、起到了与FAD相同功能。但上述多种试验结果证明,在离体法试验中,不管粗蛋白、半精蛋白还是精蛋白作为ALS酶促反应的催化酶时,DTT替代FAD也能完成丙酮酸转化生成3-羟基丁酮的酶促反应。
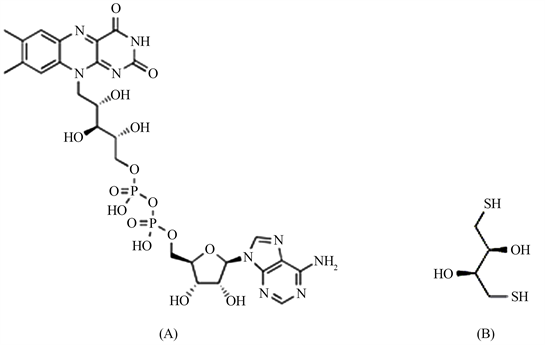
Figure 1. MolecuLar structures of fLavin adenine dinucLeotide (FAD) (A) and DithiothreitoL (DTT) (B)
图1. 黄素腺嘌呤二核苷酸分子结构(A),二硫苏糖醇分子结构(B)
4. 讨论与结论
常用的离体法ALS活性检测试验是属于试验步骤比较繁琐、试验条件苛刻、费时费工的酶活性试验之一。因此,后期很多论文作者在ALS活性测定试验中采用了比较简化的步骤,其中很多论文试验是在ALS蛋白酶过程中采用了省略Sephadex G-25层析柱纯化过程的简化方法 [5],甚至简化到省略粗蛋白沉淀、省略Sephadex G-25层析柱纯化过程的粗蛋白的 [6] [7],还有缓冲液、反应液中添加FAD和DTT加的 [8] [9],只加DTT的 [10] [11] 等。
试验结果,作为玉米暗培养的幼苗试材时,因提取的蛋白质是粗蛋白、半精蛋白或精蛋白,所获得的蛋白质含量有差异,表现出粗蛋白法提取液的蛋白质浓度最高,半精蛋白法次之,精蛋白法最低趋势。
比较不同提取方法所提取的粗蛋白、半精蛋白或精蛋白对ALS活性影响,首先粗蛋白、半精蛋白或精蛋白溶液固有的3-羟基丁酮量含量大小排序为粗蛋白质的浓度最高,半精蛋白的次之,精蛋白的最低趋势;酶促反应生成的3-羟基丁酮量含量大小排序也是粗蛋白质的浓度最高,半精蛋白的次之,精蛋白的最低趋势。如果粗蛋白代替精蛋白作为ALS酶,可省时省工,但必须以酶促反应之前预先加硫酸备制的样品调零,消除粗蛋白溶液固有的3-羟基丁酮的吸光度。否则出现偏差,导致抑制剂抑制效率的降低误差。比如,假设当固有3-羟基丁酮含量(CK2)和酶促反应生成量(CK4)比为1:1,而抑制剂的实际抑制效果100%时,如果标曲空白调零点时公式计算的抑制效果只能为50%。所以调零样品以预先加硫酸的调零方法消除固有量CK2 = 0,才能得到真实的抑制效果100%。
值得关注的是DTT替代FAD的缓冲液体系中,酶促反应生成的3-羟基丁酮含量类似于FAD缓冲液体系。如果DTT替代可行,不仅节省试验成本,而且可进一步揭示ALS与辅酶FAD的相互作用机理,探讨除草剂抑制作用机理与辅酶FAD的关系具有重要意义。范等 [2] 试验结果,离体法酶促反应体系中缺FAD时,没检测到3-羟基丁酮的生成量,而陈以峰等 [10] 试验结果DTT替代FAD也能促进酶促反应。
本试验结果,以DTT替换辅酶FAD配制缓冲液不影响酶促反应。无论提取的是粗蛋白、半精蛋白还是精蛋白,提取液中含有一定量的FAD。其中,粗蛋白当中的含量缓冲液添加FAD浓度(FAD 10 μmol/L)的1/10相当量,半精蛋白中含有1/1000、精蛋白中含有1/3000相当量的FAD。虽然在离体法测定ALS活性体系中,DTT替代FAD的缓冲液对ALS蛋白的提取及酶促反应效果类似于FAD的缓冲液的效果,但毕竟提取蛋白液中含有FAD分子,因此不能说明DTT完全替代FAD功能。
按照酶学理论酶分子和辅酶下分子对接是具有高度专一性,在植物细胞内丙酮酸转化3-羟基丁酮的酶促反应过程中,辅酶FAD、TPP与ALS活性中心的氨基酸残基对接完成氧化还原过程。在功能特性上虽然DTT与FAD具有相似的还原性,但分子结构相差甚大,而且DTT并不是ALS辅酶分子。在本文离体法ALS活性试验中,DTT替代辅酶FAD、与植物中提取的ALS蛋白共同催化生成3-羟基丁酮,说明起到了与FAD-ALS复合物相同的功能。假设在In vitro酶促反应体系中,DTT小分子与ALS活性中心氨基酸残基对接形成与FAD-ALS复合物结构相似的DTT-ALS复合物,则DTT与ALS是如何对接形成复合物,对接位是否与FAD相同等需要进一步究明,同时还需要深层次揭示酶与辅酶专一性对接理论。
总之,在30℃条件下暗培养5 d的玉米黄化幼苗作为提取ALS材料时,可以不用液氮直接用提取液碾磨(4℃条件),可以离心速度降低到10 K rpm;可以用粗蛋白作为酶促反应的ALS蛋白。
粗蛋白提取步骤提取的粗蛋白ALS酶促反应效果好于半精蛋白,半精蛋白好于精蛋白,但粗蛋白作为酶促反应的ALS蛋白进行酶促反应测定3-羟基丁酮吸光度时,必须以酶促反应之前预先加硫酸备制的样品调零,否则出现偏差,导致抑制剂抑制效率的降低误差。
在离体法测定ALS活性体系中,DTT替代FAD的缓冲液对ALS蛋白的提取及酶促反应效果类似于FAD的缓冲液的效果。
基金项目
国家自然科学基金(编号:31760521)。
NOTES
*通讯作者。