1. 引言
着色性干皮病(xerogpimentosum, XP)是一种常染色体隐性遗传病,是经紫外线照射后皮肤发生光敏感,继而出现皮肤脱屑、褐色斑点及斑块,甚至可致皮肤癌、眼部损伤及内脏肿瘤的1种罕见疾病 [1] [2]。XP是第一个被发现的与损伤DNA修复缺陷有关的疾病 [3],可累及各种族人群,以日本人和中东人发病率最高。通过细胞融合技术发现,将不同XP患者的成纤维细胞相互融合形成的杂种细胞可以重新获得损伤DNA修复的能力,提示我们XP具有多型性且各型之间互补 [4]。美国国家生物技术信息中心(The National Center for Biotechnology Information, NCBI)的生物医学信息检索系统PubMed (http://www.ncbi.nlm.nih.gov/pubmed/)目前显示涉及XP的致病基因包括XPA、XPB(ERCC3)、XPC、XPD(ERCC2)、XPE(DDB1)、XPF(ERCC4)、XPG(ERCC5)、XPH(POLH)、XPI(ERCC1)。角化棘皮瘤(keratoacanthoma)是一种生长迅速的皮肤肿瘤,好发于中老年 [5]。本研究对确诊的1例XP伴眼周角化棘皮瘤患者的临床、组织病理学以及基因学特点进行分析,旨在探讨着色性干皮病的基因认识以及角化瘤的病理。
2. 研究对象与方法
2.1. 研究对象病史采集
研究对象为常州市中医院就诊的1个着色性干皮病患者(图1)。生活在江苏常州,71岁女性,否认家族史,否认近亲结婚史。临床表现为面部可见大小不等、形状不规则的褐色色素沉着斑及色素脱失斑,左眼下睑下方近鼻根部,2个月内迅速长出一条状肿物垂直于皮肤面,状如香烟,大小为18 mm × 4 mm × 4 mm,其根部皮肤轻度红肿,皮肤表面见灰褐色斑片,肿物边界清晰。双眼鼻侧球结膜及其下组织增生至角膜缘内约5 cm,颈部宽约4 cm。双眼晶状体浑浊。本研究严格遵循赫尔辛基宣言,所有研究均征得患者的知情同意。
2.2. 实验方法
2.2.1. 手术切除肿物以及标本处理
行左眼下睑皮肤新生物切除 + 皮瓣修补术。切除肿物长度约2 cm,切面呈灰褐色,质硬。切除的标本经4%甲醛固定,常规脱水、包埋、切片、脱蜡,苏木精–伊红(HE)染色,于光镜下观察。术后一周复查拆线并进行电话随访。
2.2.2. 外周血DNA提取
采用苯酚/氯仿/异戊醇法提取外周血中基因组DNA,并对DNA进行质量检测:① 取5 μL DNA溶液1%琼脂糖、1 × TAE缓冲溶液电泳(电压120~180 V)检测,单一条带说明DNA完整无降解,有明显的条带说明浓度可以满足PCR要求;② Nanodrop测定所有血样DNA浓度和纯度,取OD260/OD280比值1.6~1.9纯度要求的DNA。将DNA浓度稀释到50 μg/ml,登记后放入−20℃冰箱保存备用。
2.2.3. 引物设计
设计引物软件用Primer Premier 5,一般参数:引物长度在18~30 bp;Tm值在55~65度,退火温度在60℃左右;GC含量40%~70%;要特别注意避免引物二聚体和非特异性扩增的存在;PCR扩增产物长度:位点测序引物在150~300 bp左右,外显检测引物离外显子上下游150 bp左右;目的基因测序的PCR产物条带一般不超过1200 bp。
2.2.4. XP基因序列扩增
突变筛查采用高通量测序技术对9个遗传性XP相关基因(XPA、XPB(ERCC3)、XPC、XPD(ERCC2)、XPE(DDB1)、XPF(ERCC4)、XPG(ERCC5)、XPH(POLH)、XPI(ERCC1))进行突变筛查,用NextSeq500 (美国Illumina公司)测序仪进行高通量测序。从GenBank获取基因组序列(https://www.ncbi.nlm.nih.gov/gene)。引物软件用Primer Premier 5设计引物,引物序列见表1~9。
采用PCR法扩增其编码区,引物序列和PCR退火温度。以基因组DNA为模板,通过PCR反应对目的片段进行扩增。PCR反应体系为30 μl,包括模板基因组DNA1μl (50 ng/μl),10 × Buffer缓冲液5 μl,10 mmol/L脱氧核糖核苷酸(dNTP) 5 μl,Taq DNA聚合酶0.25 μl,上、下游引物各0.5 μl (10 mmol/L)。反应条件为:95℃预变性3 min,95℃变性30 s,退火63℃~53℃ 30 s,72℃延伸45 s,共20个循环。电泳检测PCR产物(图1)。将PCR产物送上海生工生物工程股份有限公司测序。测序仪为3730DNAsequencer。进行双向测序;对正向测序发现双峰或杂峰及BLAST后DNA变异样本进行2次独立PCR产物正反向测序予以验证。
2.3. 序列比对以及突变分析
将上述基因片段的测序结果与Genebank中获取XP基因序列进行比对,使用DNAstar软件(DNASTAR Inc, Madison, WI)中SeqMan程序进行分析。用Mutation Taster (http://www.mutationtaster.org/)在线生物信息学软件分析突变位点序列的保守性以及变异是否有害。
3. 结果
3.1. 组织病理学检查结果
切除肿物送组织病理学检查结果示,表皮角化过度,真皮浅层慢性炎性细胞浸润,HE染色镜下见肿物表面过度角化,边缘表皮增生向中央包绕,底部呈假上皮瘤样增生,形成不规则的上皮团块及角化物,肿物与周围界限清楚,周围间质内可见大量淋巴细胞、嗜酸性粒细胞及组织细胞浸润(图2)。患者术后半年电话随访肿物未复发。
3.2. 基因测序结果
经基因序列分析发现,在XP基因外显子内,该患者cDNA碱基出现改变(图3~7)。检测到的突变分别位于cDNA的:
XPB基因第14外显子的第260位碱基,患者该位点存在一个杂合的点突变,碱基由A变为G,导致编码的氨基酸由赖氨酸(Lys, K)变成精氨酸(Arg, R) (图3);第14外显子的第312位碱基,患者该位点存在一个杂合的点突变,碱基由A变为G,突变前后编码的氨基酸不变,该突变为无义突变(图4);
XPC基因第8外显子的第39位碱基,患者该位点存在一个杂合的点突变,碱基由T变为C,突变前后编码的氨基酸不变,该突变为无义突变(图5);第9外显子的第506位碱基,患者该位点存在一个杂合的点突变,碱基由T变为C,导致编码的氨基酸由亮氨酸(Leu, L)变成丝氨酸(Ser, S) (图6);第16外显子的第211位碱基,患者该位点存在一个杂合的点突变,碱基由A变为C,导致编码的氨基酸由丝氨酸(Ser, S)变成精氨酸(Arg, R) (图7);
XPD基因第6外显子的第108位碱基,患者该位点存在一个杂合的点突变,碱基由C变为A,突变前后编码的氨基酸不变,该突变为无义突变(图8);
XPF基因第11外显子的第488位碱基,患者该位点存在一个杂合的点突变,碱基由C变为T,导致编码的氨基酸由脯氨酸(Pro, P)变成亮氨酸(Leu, L) (图9);
XPG基因第2外显子的第50位碱基,患者该位点存在一个杂合的点突变,碱基由C变为T,导致编码的氨基酸由苏氨酸(Thr, T)变成甲硫氨酸(Me) (图10);第4外显子的第48位碱基,患者该位点存在一个杂合的点突变,碱基由C变为T,突变前后编码的氨基酸不变,该突变为无义突变(图11);第8外显子的第108位碱基,患者该位点存在一个杂合的点突变,碱基由C变为G,导致编码的氨基酸由亮氨酸(Leu, L)变成缬氨酸(Val) (图12);第15外显子的第346位碱基,患者该位点存在一个杂合的点突变,碱基由C变为G,导致编码的氨基酸由苏氨酸(Thr, T)变成甲硫氨酸(Met) (图13);
XPI基因第3外显子的第33位碱基,患者该位点存在一个杂合的点突变,碱基由C变为T,突变前后编码的氨基酸不变,该突变为无义突变(图14)。
MutationTaster在线生物学信息软件对以上7个错义突变分析,得出“phylop”和“phastcons”值(phylop为正数即保守,数字越大越保守,负数即不保守。phastcons是一个0~1的值,越接近1越保守,越接近0越不保守。)
XPB基因第14外显子,c. 260A > G (p. Lys 87 Arg),“phylop”和“phastcons”值分别为“−0.609”和“0”。该位点序列不保守,变异对蛋白影响不大。
XPC基因第9外显子,c. 506T > C (p. Leu169Ser),“phylop”和“phastcons”值分别为“0.207”和“0.995”。该位点序列保守,变异为有害突变。
XPC基因第16外显子,c. 211A > C (p. Ser 71 Arg),phylop”和“phastcons”值分别为“0.897”和“1”。该位点序列保守,变异为有害突变。
XPF基因第11外显子,c. 488C > T (p. Pro 163Leu),phylop”和“phastcons”值分别为“−4.574”和“0”。该位点序列不保守,变异对蛋白影响不大。
XPG基因第2外显子,c. 50C > T (p. Thr17Met),phylop”和“phastcons”值分别为“−0.189”和“0.978”。该位点序列不保守,变异对蛋白影响不大。
XPG基因第8外显子,c. 706C > G (p. Leu 236Val),phylop”和“phastcons”值分别为“0.122”和“0.058”。该位点序列低度保守,变异为轻度有害突变。
XPG基因第15外显子,c. 346C > G (p. Thr117Met),phylop”和“phastcons”值分别为“0.178”和“0.053”。该位点序列低度保守,变异为轻度有害突变。

Table 1. Primer sequence of XPA gene amplification
表1. XPA基因扩增的引物序列


Table 2. Primer sequence of XPB(ERCC3) gene amplification
表2. XPB(ERCC3)基因扩增的引物序列

Table 3. Primer sequence of XPC gene amplification
表3. XPC基因扩增的引物序列


Table 4. Primer sequence of XPD(ERCC2) gene amplification
表4. XPD(ERCC2)基因扩增的引物序列

Table 5. Primer sequence of XPE(DDB1) gene amplification
表5. XPE(DDB1)基因扩增的引物序列

Table 6. Primer sequence of XPF(ERCC4) gene amplification
表6. XPF(ERCC4)基因扩增的引物序列

Table 7. Primer sequence of XPG(ERCC5) gene amplification
表7. XPG(ERCC5)基因扩增的引物序列

Table 8. Primer sequence of XPH(POLH) gene amplification
表8. XPH(POLH)基因扩增的引物序列

Table 9. Primer sequence of XPI(ERCC1) gene amplification
表9. XPI(ERCC1)基因扩增的引物序列
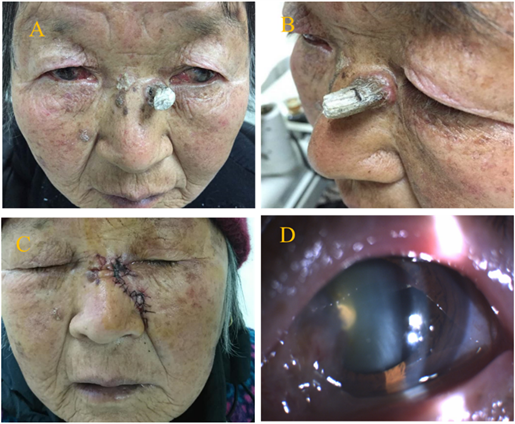 (A) (B) 面部密集分布的的雀斑样色素沉着点,左眼下眼睑见一肿物;(C) 患者术后面部照片; (D) 患者同时患者慢性睑缘炎、翼状胬肉及白内障。
(A) (B) 面部密集分布的的雀斑样色素沉着点,左眼下眼睑见一肿物;(C) 患者术后面部照片; (D) 患者同时患者慢性睑缘炎、翼状胬肉及白内障。
Figure 1. Photos of the patient’s face, tumor and anterior segment
图1. 患者面部、肿物以及眼前节照片
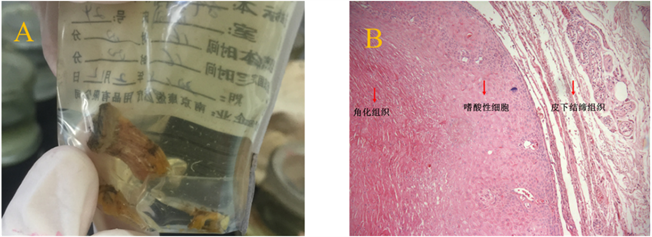 (A) 手术切除后组织;(B) H-E染色显微镜下观察:肿物表面过度角化肿物与周围界限清楚,周围间质内可见大量淋巴细胞、嗜酸性粒细胞及组织细胞浸润(×200倍)。
(A) 手术切除后组织;(B) H-E染色显微镜下观察:肿物表面过度角化肿物与周围界限清楚,周围间质内可见大量淋巴细胞、嗜酸性粒细胞及组织细胞浸润(×200倍)。
Figure 2. Tumor tissue and pathological section
图2. 肿物组织及病理切片
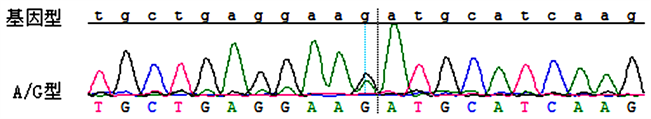 第260位碱基出现A > G杂合性改变:c. 260A > G (p.Lys87Arg)。
第260位碱基出现A > G杂合性改变:c. 260A > G (p.Lys87Arg)。
Figure 3. Sequencing results of exon 14 of XPB gene
图3. XPB基因外显子14测序结果
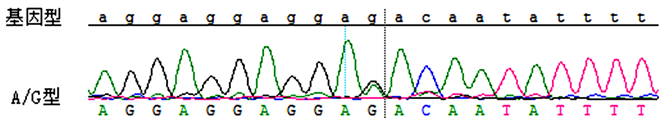 第312位碱基出现A > G杂合性改变:c. 312A > G (无义突变)。
第312位碱基出现A > G杂合性改变:c. 312A > G (无义突变)。
Figure 4. Sequencing results of exon 14 of XPB gene
图4. XPB基因外显子14测序结果
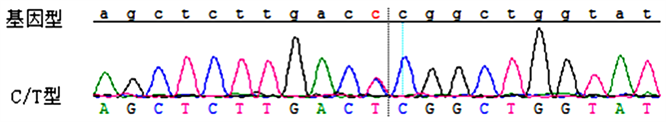 第39位碱基出现T > C杂合性改变:c. 39T > C (无义突变)。
第39位碱基出现T > C杂合性改变:c. 39T > C (无义突变)。
Figure 5. Sequencing results of exon 8 of XPC gene
图5. XPC基因外显子8测序结果
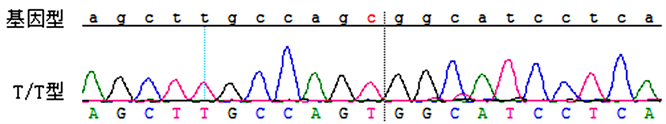 第506位碱基出现T > C杂合性改变:c. 506T > C (p. Leu169Ser)。
第506位碱基出现T > C杂合性改变:c. 506T > C (p. Leu169Ser)。
Figure 6. Sequencing results of exon 9 of XPC gene
图6. XPC基因外显子9测序结果
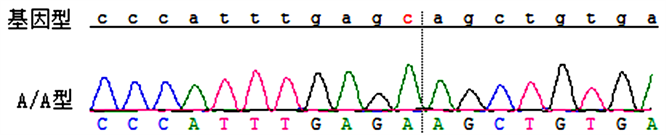 第211位碱基出现A > C杂合性改变:c. 211A > C (p. Ser71Arg)。
第211位碱基出现A > C杂合性改变:c. 211A > C (p. Ser71Arg)。
Figure 7. Sequencing results of exon 16 of XPC gene
图7. XPC基因外显子16测序结果
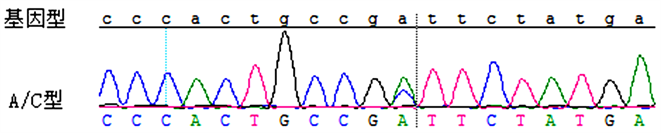 第108位碱基出现C > A杂合性改变:c. 108C > A (无义突变)。
第108位碱基出现C > A杂合性改变:c. 108C > A (无义突变)。
Figure 8. Sequencing results of exon 6 of XPD gene
图8. XPD基因外显子6测序结果
 第488位碱基出现C > T杂合性改变:c. 488C > T (p. Pro 163Leu)。
第488位碱基出现C > T杂合性改变:c. 488C > T (p. Pro 163Leu)。
Figure 9. Sequencing results of exon 11 of XPF gene
图9. XPF基因外显子11测序结果
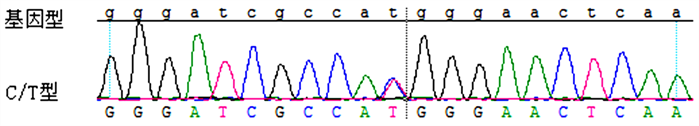 第50位碱基出现C > T杂合性改变:c. 50C > T (p. Thr17Met)。
第50位碱基出现C > T杂合性改变:c. 50C > T (p. Thr17Met)。
Figure 10. Sequencing results of exon 2 of XPG gene
图10. XPG基因外显子2测序结果
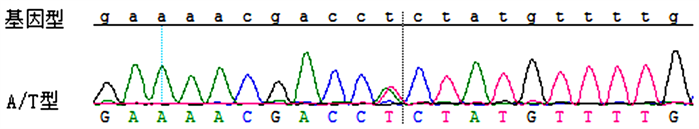 第48位碱基出现A > T杂合性改变:c. 48A > T (无义突变)。
第48位碱基出现A > T杂合性改变:c. 48A > T (无义突变)。
Figure 11. Sequencing results of exon 4 of XPG gene
图11. XPG基因外显子4测序结果
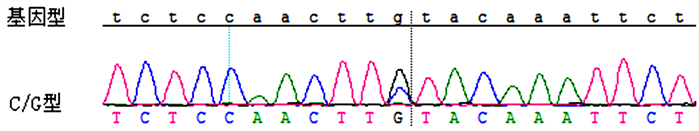 第706位碱基出现C > G杂合性改变:c. 706C > G (p. Leu236Val)。
第706位碱基出现C > G杂合性改变:c. 706C > G (p. Leu236Val)。
Figure 12. Sequencing results of exon 8 of XPG gene
图12. XPG基因外显子8测序结果
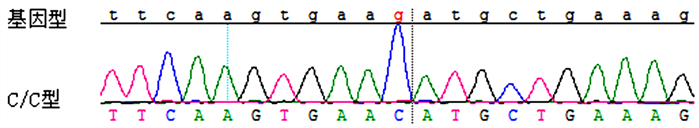 第346位碱基出现C > G杂合性改变:c. 346C > G (p. Thr117Met)。
第346位碱基出现C > G杂合性改变:c. 346C > G (p. Thr117Met)。
Figure 13. Sequencing results of exon 15 of XPG gene
图13. XPG基因外显子15测序结果
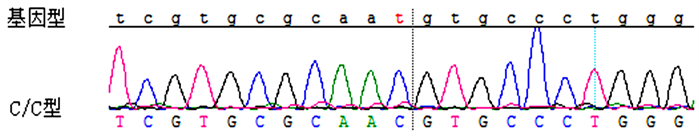 第33位碱基出现C > T杂合性改变:c. 33C > T (无义突变)。
第33位碱基出现C > T杂合性改变:c. 33C > T (无义突变)。
Figure 14. Sequencing results of exon 3 of XPI gene
图14. XPI基因外显子3测序结果
4. 讨论
XP系一种罕见的常染色体隐性遗传病,发病率低,XP是因皮肤对紫外线照射引发的DNA脱氧胸腺嘧啶二聚体切除修复缺陷 [1] [2]。该病多于幼年时发病,75%患者发病年龄为生后6个月至3岁,临床表现主要为:发病初期在皮肤暴露部位,如颜面部、口唇部、颈部及小腿等部位出现雀斑和皮肤发干,类似日光性皮炎,继而出现持久性网状毛细血管扩张。且在红斑基础上可出现大小不等的灰色或灰褐色斑片、雀斑样皮损或点状色素脱失斑,有时可见结痂性和大疱性损害 [6] [7]。随着年龄增长,可致眼部损害,如结膜炎、角膜新生血管化、干眼、角膜瘢痕、睑外翻、睑缘炎、结膜黑色素沉着和白内障等,头颈部皮肤多发性肿瘤、内脏肿瘤及神经损害等,并可于3~4年内出现恶性肿瘤 [2] [8]。XP无明显种族差异,近亲结婚为该病的危险因素之一 [9]。XPA,XPE负责识别DNA中的光产物,功能上XPA验证蛋白质是否处于正确位置,然后核酸酶XPG和XPF切割两侧损伤的DNA并用完整的DNA替换。通常情况下核苷酸切除修复包括转录偶联修复以及整组修复。XPC和XPE蛋白只在整组修复中起到作用,其他的XP蛋白在两个修复过程中都有作用。因此XPC、XPE基因缺陷的患者症状相对轻一点,一般不会出现神经异常 [10]。按分型标准 [11],XP分为3型:典型XP、类着色性干皮病型和XP变异型。典型XP的发病早(均在5岁前),皮损遍及全身,DNA修复功能缺陷;XP变异型,患者有典型XP症状,同时伴发育迟缓、智力低下等神经精神症状;类着色性干皮病,虽有典型XP症状,但发病晚,皮损局限于暴露部分,症状较轻。本患者面部密集雀斑,同时伴有慢性睑缘炎、翼状胬肉、白内障等眼部损害,可诊断为XP。但发病年龄较晚,且无明显神经精神症状,属类着色性干皮病型。可能与患者采取了较好的防护措施、以及致病基因突变为XPC未能引起严重蛋白表达改变有关。
角化棘皮瘤是一种生长迅速的皮肤肿瘤 [5],其介于良性与恶性肿瘤之间,亦有学者倾向于其为恶性肿瘤,认为是一种高分化的鳞状细胞癌 [12] [13]。角化棘皮瘤好发于中老年人皮肤暴露在日光照射部位,如面部、头颈部、前臂和手背部等 [5]。角化棘皮瘤的组织病理学特征为表皮凹陷如火山口样,其中充以角栓,底部表皮凸增生呈条索状向真皮内不规则延伸,增生表皮内可见角化珠。火山口周围表皮呈唇样突出,有细胞质嗜酸性淡染的体积大的鳞状细胞伸向真皮,可见核分裂象,真皮内炎性细胞浸润明显。本例患者长于左眼下睑下方近鼻根部,切除肿物送组织病理学检查结果均证实为角化棘皮瘤。XP与角化棘皮瘤的发生均与日光暴晒有关,但XP是否可诱发角化棘皮瘤尚待进一步研究证实。
基金项目
常州市科技项目(CJ20190062)。
NOTES
*通讯作者。