1. 引言
污水处理过程中,有机物是异养微生物进行新陈代谢的必要物质和能量来源,因此,碳源是决定反硝化进程及系统脱氮能力与效率的关键因素 [1]。在缺氧条件下,反硝化细菌利用有机碳作为电子供体并提供的能量还原硝酸盐,释放出分子态氮(N2)或一氧化二氮(N2O)以达到脱氮的效果。目前我国大部分城镇污水处理厂普遍面临着原污水碳氮比低而无法满足正常生物脱氮碳源需求的问题 [2],尤其进入低温季节,情况更为严重。因此,生物脱氮除磷所需的碳源不足是我国城镇污水厂的共性问题 [3],为提高系统反硝化脱氮效率同时满足日益严峻的出水排放标准,向生化系统中投加碳源已成为一种趋势 [4]。国外对碳源的研究主要集中在三个方面,分别是固体碳源,气体碳源和工业废水,污泥水解上清液及垃圾渗滤液等高浓度有机废液为碳源 [5]。国内目前常用的碳源一般为糖类、甲醇、乙酸、乙酸钠等,此外还有化工碳源以及某些行业取得中间产物或废料残渣等同样可以作为外加碳源。
虽然以上外加碳源可以有效提高反硝化过程的脱氮效果,但外加碳源使用的同时也增加了污水处理厂的运营成本。而且不同的外加碳源对系统的反硝化过程影响不同 [6] [7] [8]。因此选择一种价格合适且能够极大提高脱氮效果的外加碳源对污水处理厂至关重要。
神美科技有限公司是一家立足于水环境治理技术、以环保处理药剂为支撑,集研发、生产、销售、技术服务为一体的环境治理整体方案解决商。神美技术团队从碳源在水体中的消耗、吸收、利用途径角度出发,以小分子有机酸盐、单糖发酵中间体、催化酶、微生物营养盐、促生剂为原料,研发并生产出一系列用于污水脱氮工艺中的生物促进型多核碳源专利产品。
神美多核碳源系列为污水脱氮过程中提供快速、中速、慢速三类反硝化能量/电子供体组分。
1) 快速和中速碳源组分主要消耗于生化前段反硝化和释磷工艺,保证反硝化脱氮效率;
2) 微生物促生剂和活跃剂与快速、中速碳源组分协同增效,可以增强微生物的繁殖和活跃能力,降低碳源吸收率;
3) 慢速碳源组分主要消耗于生化工艺中、后段;提高微生物对污水盐度、pH值耐受度,缩短微生物驯化时间,提升系统抗负荷冲击能力,持续为微生物功能的稳定性提供能量。
该多核碳源不仅价格低、易获取,而且COD含量可调(2 × 105~13 × 105 mg/L);适用于不同水质的污水脱氮处理,定制化产品,提高出水指标与药剂投加的反应联动,减少碳源的冲击性过量投加。现场投加时,可有效降低数据反应时间,增加碳源投加量调控密度,缩小投加量调控范围,最大程度上控制无效投加、延时过量投加等问题,最终实现水厂药剂运营的降本增效。
为了研究神美多核碳源相比传统单一碳源在脱氮性能和运行方面的优势,同时避免时间和空间上更换碳源由于季节、水量、运行工况所产生的差异性,神美科技有限公司在秦皇岛某污水处理厂进行了同期生产性对比试验。通过生产性平行对比试验,对比多核碳源与乙酸钠及葡萄糖的脱氮效果,同时研究其对于系统稳定运行的影响。
2. 水厂概况
2.1. 水厂简介
处理污水以生活污水为主,同时接收和处理附近污泥处理厂的污泥液。设计规模22万吨/日,分两期实施,一期规模10万吨/日。生化段工艺为改良型多级AO工艺,数量2座;深度除磷工艺为高效沉淀池,数量2座。
2.2. 水厂水质
水厂进、出水水质如下表1:

Table 1. Designed incoming and outgoing water quality of the water plant
表1. 水厂设计进、出水水质
注:表中除pH单位为无量纲,其余指标单位均为mg/L。
2.3. 工艺简介
水厂污水经粗格栅后经进水泵房提升至中细格栅,再经曝气沉砂池后进入生物池,然后经二沉池沉淀,再经中间提升泵房提升至高效沉淀池进行处理,再经活性砂滤池过滤,流入回用水池,最终排入人工河。其中生物池由多级AO组成,生物池进水流向依次为前置反硝化段–厌氧段–第一缺氧段–第一好氧段–第二缺氧段–第二好氧段,其中设计停留时间为:前置反硝化:厌氧:一缺:一好:二缺:二好 = 1.5:1.5:4.8:7.01:2.0:0.63 h,故试验期间实际停留时间约为设计值的2倍。试验期间,碳源投加点位根据对比试验中碳源自身特性及水力停留时间投加在第一缺氧段或第二缺氧段,具体工艺流程图1所示。
3. 碳源投加试验方案
3.1. 运行条件
1) 碳源加药系统的改造
碳源加药利用原厂加药系统,并进行如下改造:由试验前的贮存同一种药剂同时向两组生物池投加同种药剂,改造为两种药剂分别单独贮存,通过管路开关的切换,实现在药剂贮池和加药泵不变换的情况下两系列生物池所投加碳源种类的对调。并可实现分别向两组生物池投加不同碳源以及碳源种类的切换。(改造由神美科技完成)
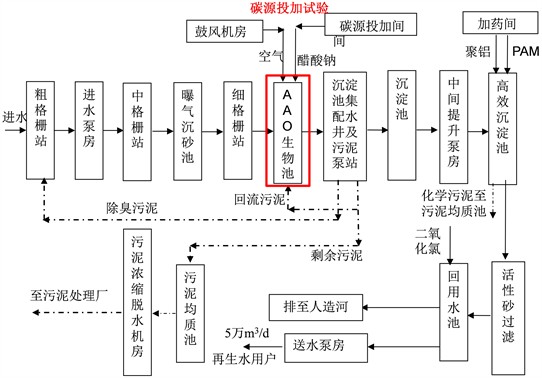
Figure 1. Process flow chart of water plant
图1. 水厂工艺流程图
2) 运行条件
采用平行试验的方式进行对比,即在一期的1个系列中投加多核碳源,第2个系列投加乙酸钠、葡萄糖参照对比,两个系列的操作条件完全一致,通过研究出水水质比较脱氮效果。第一阶段对比多核碳源与乙酸钠;第二阶段对比多核碳源与葡萄糖。
操作条件:
a) 2个系列内回流、外回流能够独立运行,进水量一致;
b) 多核碳源与乙酸钠、葡萄糖可向任意一个系列投加(可对调)。
3.2. 药剂投加方案
由于实际运行中碳源投加量较大,为尽可能优化碳源成本,降低试验水厂的负担和出水超标风险,生产性试验期间,试验方案采用控制两座生物池出水TN。
3.3. 评价方法
1) 主要评价指标
进出水COD、BOD、TN,碳源投加量,运行费用。
2) 参考评价指标
抗冲击负荷能力,碱度,MLSS,污泥粘度,污泥产量和脱水性能,进水溶解性COD与颗粒COD比例,TP,反硝化比速率验的方式进行对比。
3) 数据测定周期
见下表2测定周期表。

Table 2. Periodic table of data measurement
表2. 数据测定周期表
3.4. 试验时间
多核碳源与乙酸钠对比:2019年12月17日至2020年1月13日。
多核碳源与葡萄糖对比:2020年2月17日至2020年4月27日,其中2020.3.28日双沟调换。
3.5. 试验要求
生产性试验期间,水厂出水达到一级A排放标准,即出水标准COD < 50 mg/L,TN < 15 mg/L。
3.6. 比对碳源产品及量化指标
如表3,通过多核碳源与常规碳源的对比生产试验,以出水TN含量和运行费用的对比为核心,综合分析试验中主要指标和参考指标的异同,评价水质达标前提下投加多核碳源在技术和经济方面的优势。

Table 3. Comparison table of technical parameters of polynuclear carbon source, sodium acetate and glucose
表3. 多核碳源和乙酸钠、葡萄糖技术参数对比表
3.7. 多核碳源与乙酸钠反硝化速率小试
取生化池污泥进行反硝化速率小试试验,结果见表4所示。


Table 4. Denitrification rate data of multinuclear carbon source and sodium acetate
表4. 多核碳源与乙酸钠反硝化速率数据
通过室内反硝化小试实验可以得知:
1) 在同等加药量条件下,0~30 min内,乙酸钠相对多核碳源具有较快的响应速度(图2)。这主要是由于乙酸钠为小分子有机物,易于被微生物利用和降解。在生产性试验运行中,乙酸钠几乎不需要进行驯化,在极短的时间内可快速完成反硝化反应。
2) 在30~240 min内,多核碳源的反硝化作用持续,与乙酸钠逐渐拉开差距。
3) 将碳源投加量换算为COD投加量,则
38 mg/L、
70 mg/L,将0~360 min中每个时间节点消耗的
换算为
,结果见表5,反应初始时,
为8.05、
为15.59,反应终点时
为4.59、
为3.98。可见,反应过程中碳源充足,且初始时多核碳源较乙酸钠更加富余,但反应速率略却低于乙酸钠,由此可以推断该小试试验的初始COD浓度并不是影响后续硝化反应的主要因素。
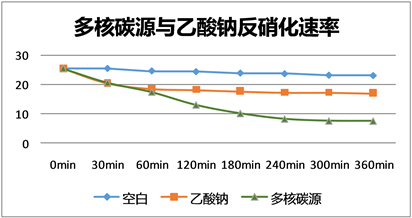
Figure 2. Comparison of denitrification rate between multi-nuclear carbon source and sodium acetate
图2. 多核碳源与乙酸钠反硝化速率对比

Table 5. Carbon to nitrogen ratio in denitrification process
表5. 反硝化过程碳氮比
4) 分析后期两者反硝化能力出现差距的原因:由于乙酸钠为单一组分,在前期提供电子释放完能量后,后期出现能量不足,反硝化速率明显降低的现象,后期的脱氮速率显著降低。而多核碳源在后期供能中体现了一些优势。
5) 试验水厂一段缺氧区停留时间4.8 h,二段缺氧区停留时间2.0 h。因此,现场投加时,乙酸钠适宜投加于二段缺氧区,快速去除TN。而多核碳源适宜投加于一段缺氧区或者二段缺氧区。
3.8. 多核碳源与葡萄糖的反硝化速率对比
由于微生物对于葡萄糖需要一定时间适应,因此在更换碳源期间,对比试验正式开始前,通过葡萄糖掺兑多核碳源投加的方式对微生物进行驯化。驯化期间不断监测活性污泥的反硝化速率,通过对比驯化不同阶段的反硝化速率来表征驯化的终点,试验数据如表6和图3所示。


Table 6. Sludge denitrification rate test during glucose domestication
表6. 葡萄糖驯化期间污泥反硝化速率试验
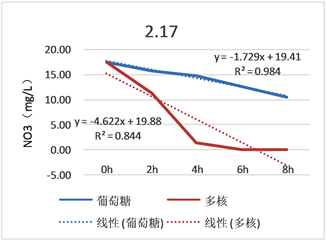
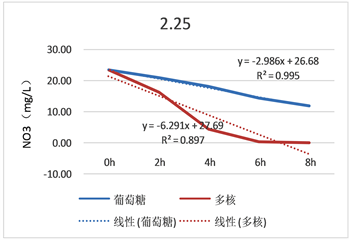
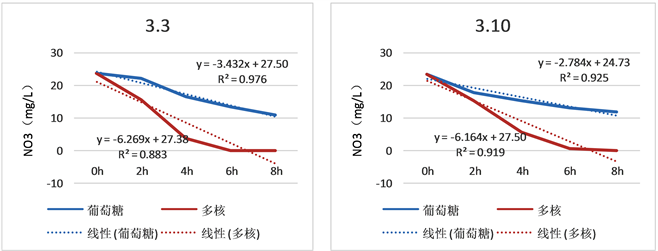
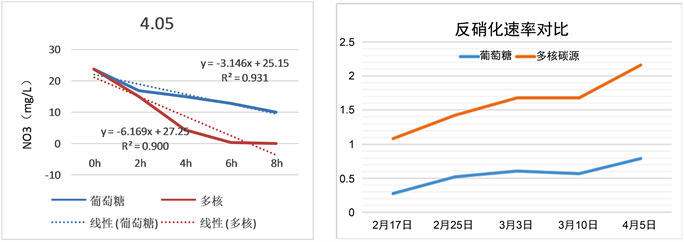
Figure 3. Judging the end point of domestication
图3. 驯化终点判定
小试数据分析如下:
1) 2.17~3.27,1#生物池投加多核碳源,2#生物池投加葡萄糖,从图3中葡萄糖和多核的反硝化速率来看,从2.17号开始,随着驯化时间的延长,两种碳源的反硝化速率逐渐增大,至3.10数据变化不大,反硝化速率基本上平稳,初步判定葡萄糖和多核的驯化期基本结束,3.10起2#生物池全部投加葡萄糖,3日后进入稳定期(即3.13~3.27)。
2) 3.30生物池碳源调换后,于4.05测定一次反硝化速率,之后并未加测。葡萄糖的反硝化速率并未减弱,保险起见,设定对调后的驯化时间为两周,之后为稳定期(即4.13~4.27)。
3) 对比4.05和3.10的反硝化速率结果可以看出,两种碳源的反硝化速率均有所提升,分析原因有以下两点:① 入春后,水温逐渐升高,微生物活性增加,故反硝化速率有所提升;② 剩余污泥排放的增大,老化污泥逐渐被新活性污泥置换,新活性污泥反应活性较强。
4) 如不考虑亚硝酸盐氮的累积,稳定期内多核碳源的反硝化速率是葡萄糖的2.8倍左右,多核碳源具有较高的反硝化速率。
5) 葡萄糖反硝化曲线的R2均在0.9以上,线性较好,说明投加葡萄糖的污泥反硝化速率在反应过程中较为稳定,故葡萄糖不适宜作为应急投加碳源。由于代谢时间较长,葡萄糖宜投加于一段缺氧区。
4. 生产性试验数据分析
4.1. 多核碳源与乙酸钠生产性试验数据
4.1.1. 试验期间进水C/N
由图4可以看出,多核碳源与乙酸钠对比期间处于冬季,两个系列生物池水温10℃~11℃,平均10.3℃,进水C/N和B/N比分别为2.86~13.35 (平均7.65)、1.06~6.63 (平均3.67)。根据神美科技服务运行水厂碳源投加经验,水温12℃以上,BOD/TN ≥ 3不投加碳源;水温12℃以下,按BOD/TN = 4的比例投加碳源。试验期间,水温低于12℃,进水B/N波动较大,B/N平均3.67,需补充碳源以保证TN达标。
4.1.2. 投加位置
多级AO后置缺氧池实际停留时间4 h,多核碳源与乙酸钠两种药剂完全满足后置缺氧投加需求,且在后置缺氧投加能充分发挥原水碳源潜能,故乙酸钠和多核碳源在后置缺氧展开平行试验对比。
4.1.3. 生物池脱氮效果
多核碳源与醋酸钠生产性试验划分为驯化段(12.17~12.26)和稳定段(12.27~1.07)两部分,具体生产性试验沿程数据如下图5所示:

Figure 4. The carbon-nitrogen ratio of influent water during the comparison of multi-nuclear carbon source and sodium acetate
图4. 多核碳源与乙酸钠对比期间进水碳氮比

Figure 5. TN Removal effect diagram of multi-nuclear carbon source and sodium acetate
图5. 多核碳源与乙酸钠TN去除效果图
1) 试验驯化期间通过调整系统进水、内外回流的平衡,使得两个系列生物池二缺进水达到大致相同,如图5醋酸钠与多核碳源试验期间稳定期所示,1#生物池稳定期二缺进水TN平均为15.76 mg/L,2#生物池稳定期二缺进水TN平均为16.21 mg/L,数据波动率相差2.15%,结合表4数据,可认为双沟进水及运行参数大致相同。
2) 大试期间通过控制两系列生物池出水TN相接近为原则,来对比醋酸钠和多核碳源的投加量,大试稳定期间,1#生物池(投加醋酸钠)生物池出水TN平均为12.00 mg/L,2#生物池(投加多核碳源)生物池出水TN平均为11.09 mg/L,数据波动率相差8.80%,相应的碳源投加量如下图6所示:
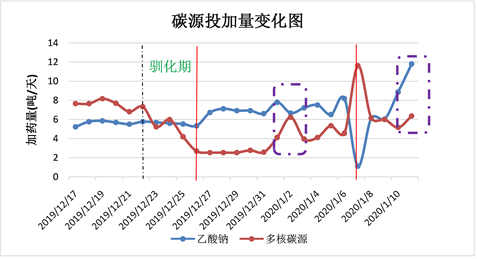
Figure 6. Comparison of carbon source dosage
图6. 碳源投加量对比图
4.1.4. 碳源使用效率及经济性对比
分析图7可以看出,生产性试验稳定期乙酸钠投加量为6.96 t/d,吨水处理成本为0.316元;多核碳源投加量为3.67 t/d,吨水处理成本为0.261元;投加多核碳源比投加乙酸钠降本17.41%。
乙酸钠单位碳源脱氮量为129.68 kgN/t碳源,多核碳源单位碳源脱氮量为257.90 kgN/t碳源,单位碳源脱单量提升49.71%。
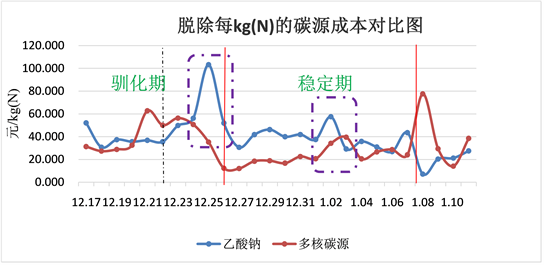
Figure 7. Comparison of carbon source utilization efficiency and economy
图7. 碳源使用效率及经济性对比图
4.1.5. 多核VS醋酸钠MLSS变化
1) 分析图8得知12.26~1.09多核碳源与醋酸钠对比期间,多核碳源的MLSS低于醋酸钠6.87%。
2) 多核碳源与醋酸钠对比期间,由于1.13进水异常,导致系统崩溃,多核碳源与乙酸钠的换沟实验未如期进行。
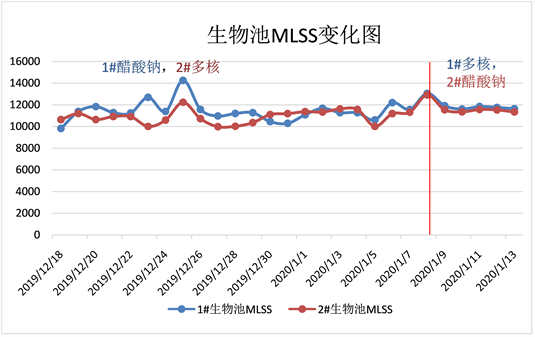
Figure 8. Change trend of multi-nuclear carbon source VS sodium acetate MLSS
图8. 多核碳源VS乙酸钠MLSS变化图
多核碳源与乙酸钠对比试验期间,水厂总出水各项指标均达到一级A排放标准,现将各项对比数据汇总成表7如下:

Table 7. Summary table of comparison data between multi-nuclear carbon source and sodium acetate
表7. 多核碳源与乙酸钠对比数据汇总表
备注:日脱氮量 = (进水TN − 出水TN) * 水量;消耗C/N = [(进水COD − 出水COD) * 水量 + 碳源投加量 * 自身COD值]/日脱氮量;单位碳源脱氮量 = 日脱氮量/加药量;吨水处理成本 = 供货单价 * 加药量/水量;脱氮率 = (进水TN − 出水TN)/进水TN * 100%;单位碳源脱氮量提升率 = (单位碳源脱氮量(多核碳源) − 单位碳源脱氮量(乙酸钠))/单位碳源脱氮量(多核碳源) * 100%;降本 = (吨水处理成本(乙酸钠) − 吨水处理成本(多核碳源))/吨水处理成本(乙酸钠) * 100%。
4.16. 结合小试及大试生产性试验,多核碳源优势原因分析
醋酸钠作为一种单一组分,其水解产物为小分子物质,固定COD值的微生物能量/电子供体,因其提供的能量主要用于反硝化脱氮和微生物繁殖增长两部分,当微生物受进水水质变化冲击,丰度发生变化时,更多的能量用于维持微生物丰度,反硝化脱氮的能量势必减少,造成其投加后的功能分配与现场运行工艺匹配度降低,致使出水无法保证达到平稳的脱氮效果。
4.2. 多核碳源与葡萄糖的试验数据分析
4.2.1. 试验期间进水碳氮比
多核碳源与葡萄糖对比试验跨冬,两个系列生物池水温10.6℃~13.8℃,平均12.07℃,进水C/N和B/N比分别为2.07~9.81 (平均4.13)、1.23~4.60 (平均2.00)。试验期间,水温逐渐高于12℃,但进水B/N波动较大,B/N平均2.00 (<3),需补充碳源以保证TN达标。
由图9可以看出,多核碳源与葡萄糖对比试验跨冬,两个系列生物池水温10.6℃~13.8℃,平均12.07℃,进水C/N和B/N比分别为2.07~9.81 (平均4.13)、1.23~4.60 (平均2.00)。试验期间,水温逐渐高于12℃,但进水B/N波动较大,B/N平均2.00 (<3),需补充碳源以保证TN达标。
4.2.2. 投加位置
因葡萄糖属于慢速分解大分子碳源,反硝化停留时间>4 h,为充分发挥碳源利用潜能及对比试验的合理公平性,故多核碳源和葡萄糖的对比试验投加在前置缺氧池。
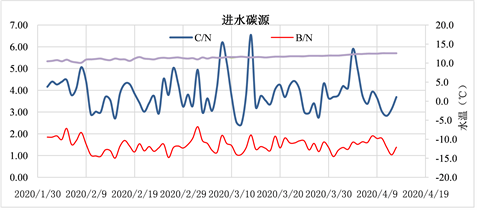
Figure 9. The carbon-nitrogen ratio of influent water during the comparison of multi-nuclear carbon source and glucose
图9. 多核碳源与葡萄糖对比期间进水碳氮比
4.2.3. 生物池脱氮效果
多核碳源与葡萄糖生产性试验划分为驯化段(2.17~3.12)和稳定段(3.13~3.27),3.28双沟调换,驯化段(3.29~4.12),稳定段4.13~4.27 (稳定期)具体生产性试验沿程数据如下图10所示:
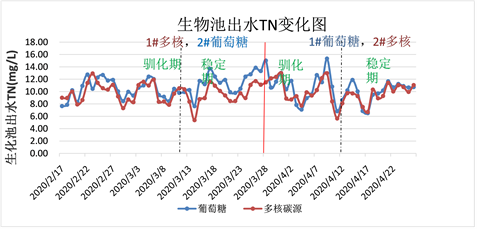
Figure 10. The removal effect of multi-nuclear carbon source and glucose TN
图10. 多核碳源和葡萄糖TN去除效果图
大试期间通过控制两系列生物池出水TN相接近为原则,来对比葡萄糖和多核碳源的投加量,大试稳定期间,对调前1#生物池(投加多核)生物池出水TN平均为9.54 mg/L,2#生物池(投加葡萄糖)生物池出水TN平均为11.53 mg/L,数据波动率相差17.3%;对调后1#生物池(投加葡萄糖)生物池出水TN平均为10.06 mg/L,2#生物池(投加多核碳源)生物池出水TN平均为9.70 mg/L,相应的碳源投加量如上图11所示。
4.2.4. 碳源使用效率及经济性对比
分析图12可以看出,多核碳源投加量为2.48 t/d,吨水处理成本为0.19元;葡萄糖投加量为3.74 t/d,吨水处理成本为0.24元;投加多核碳源比投加乙酸钠降本20.83%;
多核碳源单位碳源脱氮量为317.20kgN/t碳源,葡萄糖单位碳源脱氮量为197.17 kgN/t碳源,单位碳源脱氮量提升37.84%;
总出水COD指标控制在8~30 mg/L之间,平均值为13.89 mg/L;总出水TN控制在8~14 mg/L之间,平均值为10.71 mg/L。
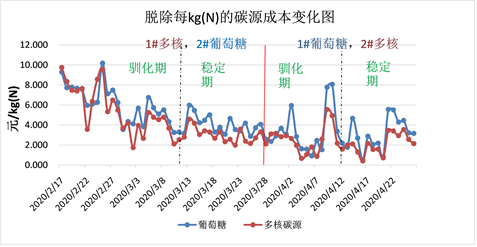
Figure 12. Comparison of carbon source utilization efficiency and economy
图12. 碳源使用效率及经济性对比图
4.2.5. 碳源产泥量比对效果
如图13多核碳源VS葡萄糖MLSS变化可知:
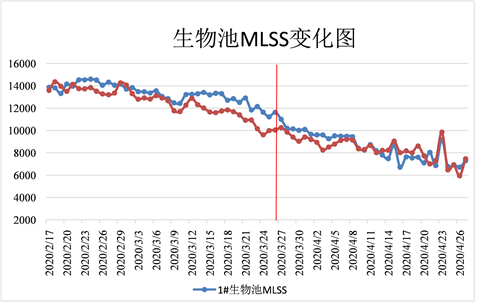
Figure 13. Change trend of multi-nuclear carbon source VS glucose MLSS
图13. 多核碳源VS葡萄糖MLSS变化图
1) 2.17~3.10 (1#生化池投加葡萄糖,2#生化池投加多核碳源),葡萄糖掺兑多核碳源驯化阶段,多核碳源与葡萄糖的污泥浓度差异性较小,多核碳源MLSS低于葡萄糖3.7%。
2) 3.11~3.27葡萄糖与多核碳源正式比对期间,MLSS差距开始逐步拉大,多核碳源MLSS低于葡萄糖10.5%。
3) 3.28~4.27双沟调换后,由于多核碳源的产泥量低的优势,两生物池的MLSS差距开始逐步降低。
4) 多核碳源与葡萄糖的产泥量比对是基于双方规定的比对时间方案进行,长期比对投加,多核碳源的产泥量优势将更加突出。
试验期间出水稳定达标。多核碳源与葡萄糖对比数据汇总如下表8:

Table 8. Summary of comparison data between multi-nuclear carbon sources and glucose
表8. 多核碳源与葡萄糖对比数据汇总
备注:同表7中备注。单位碳源脱氮量提升率 = (单位碳源脱氮量(多核碳源) −单位碳源脱氮量(葡萄糖))/单位碳源脱氮量(多核碳源) * 100%;降本 = (吨水处理成本(葡萄糖) − 吨水处理成本(多核碳源))/吨水处理成本(葡萄糖) * 100%。
4.2.6. 结合小试及大试生产性试验,多核碳源优势原因分析:
A) 与生化工艺匹配度高,反硝化过程中,COD利用率高
神美多核碳源以低于葡萄糖30%的COD贡献量,总氮去除率却高于固体葡萄糖,且控制出水COD更低,表明神美多核碳源作为微生物反硝化能量/电子供体,反硝化脱氮过程中COD利用率更高,脱氮效率高,与生化系统各工艺参数匹配度高。
B) 污泥增量降低
葡萄糖作为大分子碳源,分解速率慢,脱氮效率低,靶向作用差,所以固体葡萄糖提供多余的COD必然是被微生物吸收消耗进而转化成污泥增量,相比之下,长期运行多核碳源可以降低污泥增量。
5. 结论
通过多核碳源与乙酸钠及葡萄糖的生产性对比试验可以看出:
1) 以多核碳源作为外加碳源比以乙酸钠作为外加碳源,单位碳源脱氮量提高了49.71%,投加成本降低了17.41%。
2) 以多核碳源作为外加碳源比以葡萄糖作为外加碳源,单位碳源脱单量提高了37.84%,投加成本降低了20.83%。
3) 以多核碳源作为外加碳源比C/N均低于以乙酸钠或葡萄糖做为外加碳源的C/N,主要得益于多核碳源中的微生物促生剂和益生因子,产品组分中的微生物促生剂和益生因子是产品开发过程中,通过大量正交试验筛选出的微生物营养盐组分,对反硝化微生物具有靶向促进作用,投加应用中优先满足反硝化菌种的繁殖增长及保持丰度活性所需的能量,降低反硝化菌种对碳源(COD)的消耗吸收,使更多的碳源(COD)参与到微生物脱氮过程,从反硝化机理上提高了碳源的综合利用效率,从而产泥率更低;多核碳源与乙酸钠对比试验期间,多核碳源平均MLSS低于乙酸钠6.87%,多核碳源与葡萄糖对比试验期间,多核碳源平均MLSS低于葡萄糖10.5%,长期持续投加,多核碳源的优势将更加突出。
4) 多核碳源区别于常规碳源(乙酸钠、葡萄糖、甲醇、淀粉等)单一组分、脱氮效率单一等缺点,生物促进型碳源以不同组分碳源在各流程段的消耗和综合利用,通过复配微生物促生剂和益生因子强化微生物多样性及丰度,均衡持续为反硝化提供COD,控制降低微生物因繁殖增长而消耗的碳源量,同时提升系统抗负荷、抗波动冲击能力。而且降低了碳源的投加成本,在保证水厂出水稳定达标的前提下,可以实现水厂的降本增效,具有较高的市场推广价值。