1. 引言
脱硝工艺是指通过一定方法将大气中的NOx还原成无害的氮气以降低NOx排放量 [1] 的工艺。目前,控制NOx排放量的主要技术为选择性催化还原(SCR)法 [2],该工艺最初于1961年由Cohn首先发现并申请专利,于20世纪80年代在日本实现工业化,随后在欧洲和美国开始广泛应用,该方法以NH3、CO、H2和烃类等为还原剂,在较低的温度(280℃~420℃)下将烟气中的NOx还原成为N2和H2O。
催化剂是SCR法的核心,分为蜂窝式、板式及波纹式催化剂三类。大部分催化剂都以锐钛矿型TiO2为载体,含量在80%~90%,V2O5 (含量1%~5%)、WO3 (含量5%~10%)为活性成分 [3]。但在实际运行中,烟气飞灰中所含的K、Na、Ca、As和P等会导致催化剂的中毒,恶劣的工作环境会导致催化剂物理堵塞、磨损烧结、比表面积下降、活性成分流失等 [4] [5]。2016版《国家危险废物名录》将废SCR催化剂(钒钛系)归为“HW50废催化剂”,从2014年底开始,全国SCR脱硝设施每年将产生1.2万吨的废SCR催化剂,且产生量将不断增加,据统计到2019年,每年产生量将达到20万吨(约30万立方米),如此大量的危险废物会给国家土壤和水体带来非常大的环境威胁 [6] [7]。如果可以通过工艺方法对废SCR催化剂再利用,具有很高的环境效益和经济效益。
废SCR催化剂回收的方法多种多样,归纳起来可以分为酸浸法、苏打盐焙烧、碱浸法等。与其他的方法相比,酸浸法在以下两个方面具有优越性:(1) 只需要采用酸等一些常规的原料,价格低廉,提取成本低;(2) 无需在高温下进行焙烧,对设备要求低,能耗低。Erust [8] 等人使用硫酸、草酸和柠檬酸3种不同的浸出液分别添加过氧化氢回收硫酸厂废催化剂中的钒,在最佳浸取条件下,柠檬酸0.1 mol·L−1、H2O2 0.1 mol·L−1、温度70℃、时间2 h、S/L = 1:25时,钒的浸取率可达95%,H2O2可以与金属钒形成可溶性的络合物,从而提高钒的浸出效率。李力成,王磊 [9] 等比较了盐酸、硫酸、硝酸和草酸对废SCR催化剂中钒的浸取效果,通过比较,浸取钒效果由大到小为盐酸、草酸、硫酸、硝酸,另外,浓度对其硫酸浸取钒量影响最大,浓硫酸的浸取效果是稀硫酸的2.8倍,同时温度则对草酸的浸取钒效果影响最为明显,酸处理可恢复废催化剂比表面积,经浓草酸处理后的比表面积可增大为60.8 m2/g,提高了39.6%。本文通过硫酸溶液浸取废SCR催化剂,考察酸浸过程中各工艺条件如硫酸浓度、还原剂浓度、浸出时间、浸出温度、液固比等对钒浸出率的影响,确定最佳工艺条件,再通过两段逆流浸出进一步提高钒的浸出率,并探究了浸取机理。
2. 实验部分
2.1. 试剂和仪器
硫酸,分析纯;亚硫酸钠,分析纯。
L5S型紫外分光光度计,上海精密仪器仪表有限公司。
2.2. 实验方法
2.2.1. 废SCR催化剂的表征
废SCR催化剂的元素组成由荷兰PANalyrical公司生产的X射线荧光光谱仪分析(XRF)。用H3BO3做粘合剂,电流10~160 mA,电压30 KV,采集时间3 min,角度准确度小于0.001˚。
X射线衍射(XRD)仪为德国Bruker生产,型号D8-Advance,测试条件:Cu靶,Kα射线,步长0.05˚·step−1,管电流40 mA,管电压40 kV,扫描角度2θ = 20˚~60˚,扫描速度为10˚·min−1。
X射线光电子能谱(XPS)分析仪型号为赛默飞Thermo ESCALAB 250XI,测试时,将样品制成1 cm × 1 cm的压片样品,样品结合能由C 1 s校正,采用XPS-Peak软件进行分化拟合。
2.2.2. 浸出过程
先将废SCR脱硝催化剂置于100℃的电热恒温干燥箱中干燥12 h,然后将干燥后的原料进行破碎、研磨、筛分,取粒径在120目~140目之间的废催化剂进行后续实验。采用硫酸溶液浸取废SCR脱硝催化剂中的钒。取1.0 g废SCR催化剂放入烧杯中,加入一定量的硫酸溶液,搅拌混合均匀,烧杯放到恒温加热磁力搅拌器中恒温浸取,反应温度在±1℃内保持恒定。浸取一定时间后,冷却至室温,常压过滤,滤液定容至250 mL容量瓶备用,滤渣收集留用。取定容后的滤液2.00 mL于烧杯中,通过5-BR-PADAP分光光度法法测定其吸光度。最后,根据钒标准曲线求出钒的浓度,进而得到钒浸取率。
其中,ci为浸出液中钒的浓度,v是浸出液的体积,m是废SCR脱硝催化剂的质量,wi为废SCR脱硝催化剂中钒的质量分数。
3. 结果与讨论
3.1. 废SCR催化剂的表征分析
实验用废SCR催化剂取自安徽思凯瑞环保科技有限公司,呈蜂窝状,由XRF分析其元素组成,由表1可以看出其钒元素含量为0.74%。

Table 1. Chemical composition of waste SCR catalyst
表1. 废SCR催化剂的化学组成
图1所示XRD谱图中出现了锐钛型TiO2的特征衍射峰,但WO3和V2O5的特征衍射峰却没有出现,说明催化剂并没有发生烧结而导致载体的晶型发生改变,也表明催化剂中的活性组分在催化剂表面分散均匀,WO3和V2O5以高度分散或无定形态分布在载体的表面,或者以固溶体形式存在于载体中。
由图2可看出,在结合能为516.9 eV、515.6 eV、514.5 eV处的3个峰位分别归属于V5+、V4+和V3+,分别占比为34.02%、63.85%和2.13%,由于活性组分V在反应过程中是V5+变为V4+再变为V3+,而通常认为V5+和V4+具有催化活性,V3+并没有催化活性。V5+和V4+含量总共占到了97.87%,V3+仅有2.13%,这说明催化剂失活的原因不是活性组分V5+和V4+的减少。

Figure 1. XRD patterns of the waste SCR catalysts
图1. 废SCR催化剂的XRD图

Figure 2. XPS spectra of V 2p of the waste SCR catalyst
图2. 废SCR催化剂的V 2p谱图
由图3可知为废SCR催化剂Ti 2p的XPS谱图,在结合能分别位于458.8 eV和464.6 eV处的两个锋味分别对应了Ti 2p 3/2和Ti 2p 1/2,纯TiO2中Ti4+的结合能为458.8 eV,这说明废SCR催化剂中Ti主要以TiO2的形式存在。
3.2. 硫酸溶液浸取废SCR催化剂
3.2.1. 浸出温度对钒浸出率的影响
在硫酸溶液和废SCR催化剂的液固比5 (ml/g),硫酸浓度8%,亚硫酸钠量7% (占催化剂质量),浸出时间为60 min的条件下,探究浸出温度对钒浸出率的影响。所取浸出温度分别为50℃,60℃,70℃,80℃,90℃。实验结果如图4所示。

Figure 3. XPS spectra of Ti 2p of the waste SCR catalyst
图3. 废SCR催化剂的Ti 2p谱图
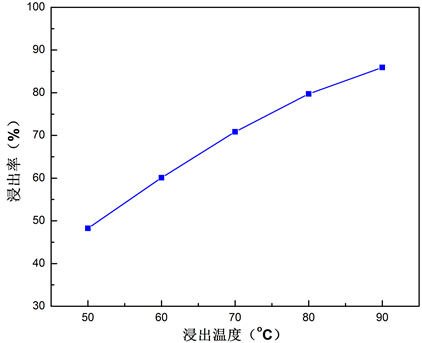
Figure 4. The leaching rates of vanadium with different temperature conditions
图4. 浸出温度对钒浸出率的影响
由图4可以看出,当浸出温度从50℃升高到90℃时,钒浸出率的上升趋势明显,说明浸出温度对该体系的浸出率具有显著影响。这主要是因为温度影响分子的运动速率,温度升高,分子运动速率加快。同时,溶液的粘度随温度升高而降低,单位时间内反应物分子碰撞次数增多,固液之间的传质速率增大,故温度上升钒的浸出率增大。但随温度不断上升,浸出设备负荷也会随之变大,在浸出温度80℃时,浸出率已达到79.71%,故认为最适浸出温度为80℃。
3.2.2. 液固比对钒浸出率的影响
在硫酸浓度8%,亚硫酸钠量7%,浸出时间为60 min,浸出温度80℃的条件下,探究液固比对钒浸出率的影响。所取液固比分别为3 ml/g,5 ml/g,7 ml/g,9 ml/g,11 ml/g实验结果如图5所示。

Figure 5. The leaching rates of vanadium with different liquid-solid rations
图5. 液固比对钒浸出率的影响
由图5可知,随着液固比的增大,浸出率呈上升趋势,但变化较为缓慢,在液固比7 ml/g后浸出曲线几乎水平。当液固比3 ml/g时,浸出率为76.50%,当液固比5 ml/g时,浸出率达到79.71%,而液固比为11 ml/g时,浸出率为83.84%。这是由于液固比增加,废SCR催化剂与溶液间的接触面积增大,使得反应介质的扩散增大并使反应更完全,促进了钒的浸出 [10]。同时工业生产既要考虑浸出率,也要考虑成本核算,由于故最佳液固比选为5 ml/g。
3.2.3. 硫酸浓度对钒浸出率的影响
在硫酸溶液和废SCR催化剂的液固比5 (ml/g),浸出温度为80℃,亚硫酸钠量7%,浸出时间为60 min的条件下,探究硫酸浓度(3%,5%,8%,10%,12%)对钒浸出率的影响如图6所示。

Figure 6. The leaching rates of vanadium with different sulfuric acid concentration
图6. 硫酸浓度对钒浸出率的影响
由图6可得出结论,随着硫酸浓度的增加,钒的浸取率变化不大。当硫酸浓度由3%升高到8%时,对应的钒浸取率由59.03%提高到79.71%,继续增大硫酸浓度至12%时,钒的浸出效率基本达到平衡。这主要是因为pH越小越有助于破坏SCR废催化剂的颗粒结构,同时使得V2O5发生表面质子化反应生成VO2+,促进反应进一步进行,故最佳酸浸的硫酸浓度为8%。
3.2.4. 还原剂亚硫酸钠量对钒浸出率的影响
在硫酸溶液和废SCR催化剂的液固比5 (ml/g),浸出温度为80℃,硫酸浓度为8%,浸出时间为60 min的条件下,探究亚硫酸钠量(3%,5%,7%,9%,11%)对钒浸出率的影响如图7所示。

Figure 7. The leaching rates of vanadium with different sodium sulfite concentration
图7. 亚硫酸钠浓度对钒浸出率的影响
由图7可知,当亚硫酸钠浓度小于7%时,随着酸浓度的不断变大,浸出率不断上升,继续增加亚硫酸钠浓度时,浸出率出现下降。这可能是因为亚硫酸钠增多时,过量的亚硫酸钠与硫酸发生氧化还原反应产生SO2气体,使得反应的还原性下降,实际上在实验过程中,也可以观察到体系有气泡的出现。故还原剂亚硫酸钠最佳浓度为7%。
3.2.5. 浸出时间对钒浸出率的影响
在硫酸溶液和废SCR催化剂的液固比5 (ml/g),浸出温度为80℃,硫酸浓度为8%,亚硫酸钠量7% (催化剂质量的)的条件下,探究浸出时间(15 min,30 min,45 min,60 min,90 min)对钒浸出率的影响如图8所示。
由图8可知,随着反应时间增长,钒的浸出率逐渐升高。反应1.0 h时,钒的浸取率达到79.74%;继续增大浸取时间,钒的浸取率提高不大,反应1.5 h时,钒的浸取率为81.17%,没有明显提高。说明浸出时间为1.0 h时,钒的浸取基本达到平衡,继续增加反应时间,钒的浸取率变化不大,且反应时间越长,耗能也会逐渐增加,故最佳的浸取时间为1.0 h。
3.3. 两段逆流浸出
通过对废SCR催化剂一系列单因素考察钒的浸出率,最终得最佳工艺条件为:浸出温度80℃,浸出时间1.0 h,硫酸浓度8%,液固比5:1,亚硫酸钠浓度7%。在此最佳工艺条件下,得到钒浸出率为79.74%。钒浸出率并不太高,一次浸出难以达到85%以上的浸出率。为了提高钒的浸出率,因而本文对废SCR催化剂的两段逆流浸出 [11] [12] [13] 进行了考察,废SCR催化剂的两段逆流浸出的工艺流程如图9所示。
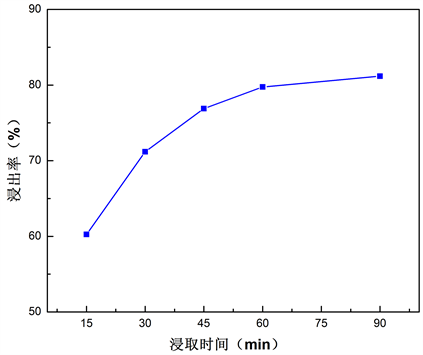
Figure 8. The leaching rates of vanadium with leaching time
图8. 浸出时间对钒的浸出率的影响

Figure 9. Two-stage countercurrent leaching process of waste SCR catalyst
图9. 废SCR催化剂两段逆流浸出工艺流程
废SCR催化剂两段浸出的具体工艺路线为:
(1) 称取一定量的废SCR催化剂,按照液固比5 ml/g,浸出温度80℃,硫酸浓度为8%,亚硫酸钠量为废催化剂质量的7%,浸出时间为30 min,在磁力搅拌器中浸出。
(2) 浸出后的浆料通过固液分离得到含有较高剩余酸度的浸出液作为第一段浸出的浸出液,按照液固比5 ml/g,浸出温度80℃,浸出时间为30 min,在磁力搅拌器中浸出新的废SCR催化剂,第一段浸出后的浆料经过固液分离后可以直接进入到萃取工序,过滤得到的滤渣作为第二段浸出原料,按照液固比5 ml/g,浸出温度80℃,硫酸浓度为8%,亚硫酸钠量为废催化剂质量的7%,浸出时间为30 min,在磁力搅拌器中再次浸出,以此循环废SCR催化剂的二段逆流浸出实验,实验结果见表2。

Table 2. Two-stage countercurrent leaching results
表2. 两段逆流浸出结果
由表2看出,第2段的浸出后的滤液变成第1段的浸出剂,第二段浸出反应后溶液的pH比第一段浸出后溶液的pH有下降,这主要是因为反应消耗了溶液中的H+。经过5组二段逆流循环试验,浸出率基本稳定在89%左右,这主要是因为两段逆流循环浸出与单次搅拌浸出相比,酸中的H+得到了充分利用,使得钒和废SCR催化剂实现了有效的分离。
3.4. 浸出机理
硫酸浸取废SCR脱硝催化剂的实验主要涉及溶解、缔合和氧化还原反应,而WO3和TiO2在浸取过程中不发生氧化还原反应,仅发生缔合和络合反应,由XPS分析(如图2)可知废SCR脱硝催化剂中钒主要以V2O3、V2O4和V2O5形式存在,分别约占2.13%、63.85%和34.02%,并且由于亚硫酸钠强还原性,主要发生以下3个反应 [14] [15]:
该反应不是一步完成的,浸出机理可以由3个反应单元 [16] 组成:(1) 首先,V2O3、V2O4和V2O5溶解,主要发生表面质子化反应,释放出水溶性阳离子VO+ 2、VO2+、VO+ (方程(1)),该过程是通过硫酸浓度和固液比来促进废SCR催化剂选择性浸取钒过程的溶解平衡的 [17]。(2) 然后,生成的VO2+、VO2+、VO+会与溶液中的硫酸根离子还有硫酸氢跟离子形成缔合,并在快速阶段达到缔合平衡,并且由于标准氧化还原电位Eθ (SO42−/SO32−) = −0.936 V,VO2+易与SO2− 4发生氧化还原反应生成VOSO4(方程(2))。(3)同时,由于Eθ (VO2+/VO+)=0.309 V、Eθ (VO2+/VO2+) =1.00 V,VO+ 2能够快速与VO+反应生成VO2+ [18] (方程(3))。因此,浸出溶液中钒的稳定存在形式为VOSO4,图10显示了不同种类的VOx与硫酸反应过程的示意图。
(1)
(2)
(3)

Figure 10. The Process diagram of sulfuric acid and vanadium pentoxide
图10. 硫酸与五氧化二钒反应过程图
4. 结论
(1) 用硫酸溶液浸出废SCR催化剂,硫酸浓度为25%时,浸出率为54.53%。在此基础上,使用Na2SO3做还原剂对废SCR催化剂进行酸浸处理,考察了浸出温度,液固比,硫酸浓度,还原剂用量,浸出时间对浸出率的影响,同时得出最佳浸出条件,浸出温度80℃,浸出时间60min,硫酸浓度8%,液固比5:1,亚硫酸钠浓度7%,在此最佳工艺条件下,得到钒浸出率为79.74%。在单次浸出的基础上,使用两段逆流浸出对废SCR催化剂进行处理,浸出率约提高9%,且H+得到充分利用。
(2) 酸浸还原处理废SCR催化剂的过程中,V2O5表面发生质子化反应生成VO+ 2,溶液中发生溶解、缔合以及氧化还原反应,催化剂中的VO+ 2能与VO+反应转化为VO2+,最终浸出液中钒以VOSO4形式存在。
NOTES
*第一作者。
#通讯作者。