1. 引言
作为一种良好的导电金属,银(Ag)复合材料已在许多领域得到了广泛使用。银络合物作为摩擦学应用的添加剂已引起广泛关注,因为有机配体稳定了银的高氧化态,从而促进了较低的分解温度。Guo等人 [1] 采用PLD技术制备了不同银含量的VN/Ag复合薄膜,研究了其在900℃高温下的微观结构、力学和摩擦学性能,结果表明,VN/Ag复合薄膜在宽温度范围内具有优异的润滑性能。Corrêa等人 [2] 研究了纳米银微粒在三种离子液体中的直接制备方法,该方法可制备均匀分散的纳米银微粒。Desanker等人 [3] 以油溶性三聚银吡唑配合物为润滑添加剂,研究了其在基础油PAO4中的高温摩擦学性能,试验结果表明,银配合物通过热重分解在摩擦副表面沉积金属银,从而降低了摩擦磨损。Hu等人 [4] [5] 研究了银前驱体型配合物作为添加剂在军用级润滑油中的摩擦学性能,结果表明,高温下银前驱体型配合物都表现出了更为优越的润滑性能,且最佳添加量为2%。Chung等人 [6] 合成了新型油溶性有机银分子,探讨了其在非极性基油中的性能,结果表明,其在非极性基础油中有很好的溶解性,并在高负载下表现出优异的减摩抗磨性能。Mccain等人 [7] 合成了系列膦基硼酸银前驱体型配合物,运用AACVD法在玻璃以及钢表面生成银薄膜,并分析了银薄膜的摩擦学性能。
有机配体的功能是将金属银传递和释放到固定温度节点。金属银纳米颗粒较难合成,且需要稳定的悬浮液或表面活性剂以避免纳米颗粒聚集,而AgNO3在440℃时分解,该温度远高于机油的典型工作温度。考虑到银有机配合物易于合成,环境稳定性和相对较低的分解温度,本研究选择了银有机配合物代替纯银金属纳米颗粒或无机银盐作为添加剂。前驱体,是获得目标产物前的一种存在形式,大多是以有机–无机配合物或混合物固体 [8] [9] 存在,也有部分是以溶胶形式 [10] [11] [12] 存在。这些银有机复合添加剂的预期用途是用于在极高温度下运行的重型车辆或机械中,可能会遇到液体润滑剂不足的情况,此时使用固体润滑剂补充基础油将有助于提高润滑性能。
在本文中,合成了一系列三种银配合物,对三种银配合物分别进行了热重分析(TGA),并对银络合物的分解产物进行了X射线衍射分析。三种银吡唑甲基吡啶配合物属于同一簇化合物但具有不同的配体,可通过改变配体结构来调节分解温度,该配体结构是为特定的添加剂应用量身定制的。
2. 银配合物的制备
2.1. 实验设备
制备系列银配合物的仪器设备主要有:电子天平、旋转蒸发仪、磁力搅拌器和超声波清洗机等。
电子天平能够准确称量并快速显示物体的质量,常用于微量物质的精确称量,图1是JM-B2002型电子天平。该仪器的最大承重为200 g,分辨率为0.01 g,去皮范围为200 g,称台尺寸为Ф110 mm。生产厂家:诸暨市超泽衡器设备有限公司。

Figure 1. Electronic balance (Model: JM-B2002)
图1. 电子天平(型号:JM-B2002)
银吡唑甲基吡啶配合物制备过程中涉及到浓缩与分离。旋转蒸发仪主要用于医药、化工和生物制药等行业的浓缩、结晶、干燥、分离及溶媒回收。图2是RE-5001型旋转蒸发仪,其原理为:在真空条件下,恒温加热,使旋转瓶恒速旋转,物料在瓶壁形成大面积薄膜,高效蒸发。溶媒蒸发经高效玻璃冷凝器冷却,回收于收集瓶中,大大提高蒸发效率,特别适用于高温容易分解变性的生物物品的浓缩提纯。

Figure 2. Rotary evaporator (Model: RE-5001)
图2. 旋转蒸发仪(型号:RE-5001)
本实验涉及到原材料需在溶液中的充分搅拌,图3是85-2型恒温磁力搅拌器。该仪器采用优质直流电机,噪音小,调速平稳,全封闭式加热盘可作辅助加热之用,可长期加热使用,其搅拌子由聚四氟乙烯和优质磁钢精制成,耐高温、耐磨、耐化学腐蚀、磁性强。其无极调速范围:0~2600 r/min,数显恒温:常温~100℃。生产厂家:上海晖创化学仪器有限公司。

Figure 3. Thermostatic magnetic stirrer (Model: 85-2)
图3. 恒温磁力搅拌器(型号:85-2)
图4是DZF-6020A型真空干燥箱,常用于一些物料和玻璃仪器的干燥。该设备工作温度范围为室温+10℃~200℃,真空度 < 133 Pa,工作室尺寸300 mm × 300 mm × 275 mm。生产厂家:北京市兴伟业仪器有限公司。

Figure 4. Vacuum drying oven (Model: DZF-6020A)
图4. 真空干燥箱(型号:DZF-6020A)
超声波清洗机用于银配合物制备过程中的的超声滴定处理,由于超声波频率高波长短,穿透力强,且真空泡破裂时会产生强大的冲击能,因此既能够清洗有隐蔽细缝和复杂结构的物品,也能够帮助物质均匀的分散。图5是613HT型超声波清洗机,该仪器的内槽尺寸为355 mm × 325 mm × 150 mm,容量为13 L,功率为360 W,频率为40 KHz,清洗温度为20℃~80℃。生产厂家:深圳市光点超声波设备有限公司。

Figure 5. Ultrasonic cleaning machine (Model: 613HT)
图5. 超声波清洗机(型号:613HT)
2.2. 实验试剂
银吡唑甲基吡啶配合物的制备采用两步法,即先合成实验所需的配体LH和Lme,然后由配体作为反应物分别合成最终所需的银吡唑甲基吡啶配合物。其中,LH为合成配合物1以及配合物3所需的反应物,Lme为合成配合物2所需的反应物。
配体合成实验所需的原料及试剂如表1所示。实验中所需的氢氧化钠40%水溶液,为购入氢氧化钠固体,然后与去离子水配制而成。无水硫酸钠为实验过程中干燥所需。

Table 1. Experimental materials and reagents for ligand synthesis
表1. 配体合成所需实验原料及试剂
第二步,使用配体LH及Lme分别合成银吡唑甲基吡啶配合物1~3,实验所需的原料及试剂如表2所示。实验的原料主要有:四氟硼酸银、硝酸银、丙酮、乙醚和己烷等,原料及试剂均来自阿拉丁试剂(上海)有限公司。

Table 2. Materials and reagents required for synthesis of silver pyrazole methylpyridine complex
表2. 银吡唑甲基吡啶配合物合成所需原料及试剂
2.3. 试剂制备
2.3.1. [Ag(LH)]n(BF4)n (配合物1)的制备
第一步,按以下方法合成配体LH [13]:2氯甲基-4-甲氧基-3,5-二甲基吡啶盐酸盐溶液(5 g)和吡唑(1.8 g)在甲苯(150 ml)中混合。接着,加入NaOH 40%水溶液(50 ml)和四正丁基氢氧化铵40%水溶液(30滴)的混合物后,使用Schlenk双排管,在搅拌下110℃回流4小时。待反应体系冷却至室温后,将反应物倒入在水溶液中,利用二氯甲烷进行萃取,重复萃取三次后,将有机层收集后加入无水硫酸钠,干燥并过滤。重结晶后在真空下除去溶剂,得到4.42 g无色微晶粉末(LH),其化学反应方程式如图6所示。
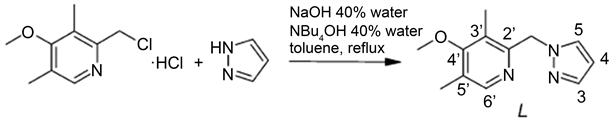
Figure 6. Synthesis of silver pyrazole methylpyridine complex LH
图6. 银吡唑甲基吡啶配体LH的合成
第二步,合成[Ag(LH)]n(BF4)n [14]:将AgBF4 (385 mg)在25 ml丙酮中的溶液加入到LH (500 mg)在25 ml丙酮中的溶液中。在常温下避光搅拌30分钟后,用旋转蒸发仪将溶剂真空浓缩,加入乙醚后沉淀出白色固体。通过过滤收集固体并干燥,最后得到625 mg白色微晶粉末(配合物1),产率为69%,其化学反应方程式如图7所示。其分子结构如图8所示,核磁共振氢谱数据为:1H NMR (300 MHz, acetone-d6):δ = 2.34 (s, 3H, CH3),2.51 (s, 3H, CH3),3.91 (s, 3H, CH3O),5.89 (s, 2H, CH2),6.56(t, J = 2.1 Hz, 1H, CH pyrazole),7.79 (d, J = 2.1 Hz, 1H, CH pyrazole),8.26 (d, J = 1.4 Hz, 1H, CH pyrazole),8.42 (s, 1H, CH pyridine) ppm。
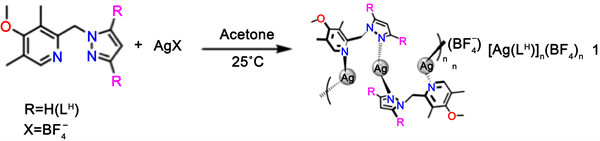
Figure 7. Synthesis of silver pyrazole methylpyridine complex 1
图7. 银吡唑甲基吡啶配合物1的合成

Figure 8. ORTEP diagram of silver complex 1
图8. 银配合物1的ORTEP图
2.3.2. [Ag(Lme)]2(BF4)2 (配合物2)的制备
第一步,按以下方法合成配体Lme:2-氯甲基-4-甲氧基-3,5-二甲基吡啶盐酸盐溶液(5 g)和3,5-二甲基吡唑(0.254 g)在甲苯(150 ml)中混合。然后,加入NaoH 40%水溶液(50 ml)和四正丁基氢氧化铵40%水溶液(30滴)的混合物,使用Schlenk双排管,在搅拌下110℃回流4小时。待反应体系冷却至室温后,将反应物倒入在水溶液中,利用二氯甲烷进行萃取,重复萃取三次后,将有机层收集后加入无水硫酸钠,干燥并过滤。重结晶后在真空下除去溶剂,得到4.2 g无色微晶粉末(Lme),其化学反应方程式如图9所示。

Figure 9. Synthesis of silver pyrazole methylpyridine complex Lme
图9. 银吡唑甲基吡啶配体Lme的合成
第二步,合成[Ag(Lme) ]2(BF4)2:将AgBF4 (730 mg)在50 ml丙酮中的溶液加入到Lme (1050 mg)在50 ml丙酮中的溶液中。室温下避光搅拌40分钟后,将溶剂真空浓缩,加入乙醚后沉淀出白色固体。通过过滤收集固体并干燥,得到970 mg乳白色微晶粉末(配合物2),产率为55%,其化学反应方程式如图10所示。其分子结构如图11所示,核磁共振氢谱数据为:1H NMR (300 MHz, acetone-d6):δ = 2.24 (s, 3H, CH3),2.31 (s, 3H, CH3),2.51 (s, 6H, 2 CH3),3.91 (s, 3H, OCH3),5.64 (s, 2H, CH2),6.16 (s, 1H, CH pyrazole),8.33 (s, 1H, CH pyridine) ppm。

Figure 10. Synthesis of silver pyrazole methylpyridine complex 2
图10. 银吡唑甲基吡啶配合物2的合成
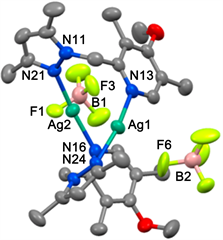
Figure 11. ORTEP diagram of silver complex 2
图11. 银配合物2的ORTEP图
2.3.3. [Ag(LH)(NO3)]2 (配合物3)的制备
第一步,合成配体LH (配合物1已制备)。第二步,合成[Ag(LH)(NO3)]2:将AgNO3 (725 mg)在10 ml水中的溶液加入到LH (1080 mg)在10 ml甲醇中的溶液中。接着,使用恒温磁力搅拌器在常温下避光将混合物搅拌30分钟。然后在真空下除去溶剂,边用超声清洗机超声,边缓慢滴入5 ml己烷,5分钟后,沉淀出白色固体,过滤收集并干燥,得到1320 mg的[Ag(LH)(NO3)]2,产率为73%,为白色微晶粉末,其化学反应方程式如图12所示。其分子结构如图13所示,核磁共振氢谱数据为:1H NMR (500 MHz, acetone-d6):δ = 2.29 (s, 3H, CH3),2.52 (s, 3H, CH3),3.86 (s, 3H, OCH3),5.75 (s, 2H, CH2),6.47 (t, J = 2.1 Hz, 1H, CH pyrazole),7.71 (d, J = 2.1 Hz, 1H, CH pyrazole),8.14 (d, J = 2.4 Hz, 1H, CH pyrazole),8.34 (s, 1H, CH pyridine) ppm。

Figure 12. Synthesis of silver pyrazole methylpyridine complex 3
图12. 银吡唑甲基吡啶配合物3的合成

Figure 13. ORTEP diagram of silver complex 3
图13. 银配合物3的ORTEP图
3. 银配合物的表征
首先,对制备得到的灰黑色产物进行了XRD定性分析,定性分析的目的是判定物质中的物相组成成分。图14~16分别是所得配合物1~3的XRD图。从图中可看出,3个银吡唑甲基吡啶配合物样品的衍射峰的位置及强度均与标准的粉末衍射卡片中的数据相一致,表明制备所得的三个产物纯度都是较高的。
通过扫描电子显微镜(SEM)对制备的三种银配合物表面形貌及尺寸进行了进一步表征。图17~19分别是配合物1~3的SEM图。从图17可以看出,配合物1为直径2 µm左右,长度在10 µm~40 µm之间的圆柱体。由图18可分析出,配合物2为直径1 µm左右的球体。由图19可得,配合物3为直径10 µm左右的球体结构。
4. 银吡唑甲基吡啶配合物的热重分析
使用耐驰公司生产的型号为TA的热重分析仪对合成物1~3进行热重量分析,评估他们热分解的性能和效率。大气压下,从30℃以5℃/min的速率升温至500℃,保护性气体为50 ml/min的氮气。
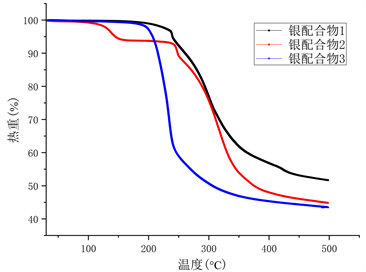
Figure 20. TGA thermogravimetric analysis of complexes 1-3
图20. 配合物1~3的TGA热重分析图
结果如图20所示,配合物1在239℃出现第一次失重。配合物2在110℃~150℃出现第一次分解,重量损失为5.97%,在230℃~250℃出现第二次分解,重量损失为6.18%,与纯银的质量百分比25.2%相吻合。配合物3在210℃~248℃的单一步骤中热解,产生黑灰色物质,伴随的重量损失为32%,这与纯银的重量百分比28.7%相吻合,另外的3.3%应是断裂的配合基质量。配合物3与配合物1、2相比,在较低温度下的失重增加,从分子结构来看,配位的NO− 3阴离子提供了中性的分子组装,而弱相互作用的BF− 4阴离子则形成了具有更强离子性质的配合物。此外,NO− 3是一种更强的氧化剂,可以帮助配体分解。
5. 结果与讨论
对热重之后的残余物质进行XRD分析,结果证实了金属银的存在。如图21所示,热重剩余材料的XRD分析与纯银XRD对比,可证实银配合物确实可分解出银单质。银是一种化学性质比较稳定,导电导热性能良好的贵金属,其质软、延展性好,是传统的固体润滑材料之一。银颗粒在摩擦过程中会形成金属银边界润滑膜,阻止金属摩擦副之间的直接接触,在摩擦过程中对磨损表面进行原位修复,并提供较小的剪切力,从而具备优异的润滑性能。且银微粒会沉积在摩擦表面形成一层物理吸附膜并在表面出现损伤时及时填补,样品油的抗磨减摩性能得到提高。而对于球形的微纳米颗粒,在接触表面之间可以起到类似“微轴承”的作用,将部分滑动摩擦变为滚动摩擦,从而降低摩擦系数。
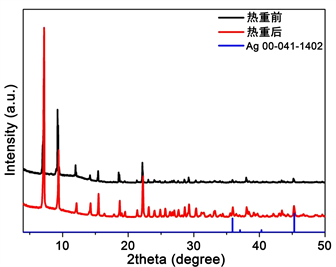
Figure 21. X-ray diffraction pattern of the decomposition product of pyrazole methylpyridine complex
图21. 银吡唑甲基吡啶配合物分解产物的X射线衍射图
6. 结论
本文合成了三种带有吡唑基甲基吡啶配体以及BF− 4 (配合物1和2)和NO− 3 (配合物3)抗衡阴离子的银配合物,并对其进行了表征,观察了其微观结构和尺寸大小。结果表明,配合物1是直径2 µm左右的圆柱形结构,配合物2和配合物3均为球形结构,直径分别为配合物1 µm和10 µm。本文中的三种银配合物,属于同一簇配合物,其具有化学成分相同,而热分解阈值不同的特点,因此,利用组份配比此系列银配合物所形成的润滑油添加剂,将可能实现润滑材料定温定量的分解,达到可控后备润滑的效果。热重分析结果表明,配合物1适用于250℃左右的高温环境,配合物2适用于120℃左右高温环境,配合物3适用于210℃左右较高温环境。最后,通过配合物热分解产物的X射线分析,证实了热分解产生了微米尺度金属银,可作为高温润滑油添加剂使用,增强油润滑系统的高温摩擦学性能,构建润滑颗粒自释放的后备润滑系统。
基金项目
本研究由国家自然科学基金(No.51875271)资助。
NOTES
*通讯作者。