1. 引言
近年来,重金属的广泛使用,如Cd2+和Pb2+,已造成严重的环境污染和健康问题 [1] 。因此,对重金属污染的防范与治理早已成为了各家环境学家重点研究课题之一。同时,选择一种抗干扰、快速、灵敏、选择性好、重复性高的检测方法也是各国科学家重点关注的问题之一 [2] 。随着现代电化学分析及技术的不断发展,电化学检测法相较于传统的光谱法和色谱法,因为其经济适用、检测准确灵敏而逐渐受到了实验室分析人员的青睐 [3] 。在各类电化学检测手段当中,微分脉冲伏安法(DPV)因其测量电流为法拉第电流,受干扰程度最小,所以在实验室中广泛运用。近年来,基于无机纳米材料、有机纳米材料和生物材料等新兴纳米和生物材料的电极修饰材料为测量重金属开辟了新的分析途径 [4] 。PEDOT具有良好的电化学稳定性和较高的导电性,是目前应用最广泛的导电聚合物之一。由于其独特的π共轭系统、较高的电导率、方便加工和容易成膜的特点 [5] ,PEDOT在许多领域都有较为广泛的运用,如能源储存、离子感应、电致变色、和生物传感器等 [6] 。g-C3N4是由氮取代的石墨六原子环单元组成的二维结构。由于其丰富的氮活性位点和独特的优越催化活性,已成为光催化、电致发光、生物传感的重要组成材料 [7] 。众所周知,氮等杂原子的掺杂会极大地改变碳材料骨架的电子结构,提高电化学性能。例如,掺杂N的石墨烯具有良好的催化性能,主要是因为sp2杂化类吡啶氮原子的孤对电子与石墨烯层的偶联作用。虽然g-C3N4具有类似于吡啶类氮的N原子,但g-C3N4的电导率较差,使其潜在的电化学催化性能大大降低。因此,g-C3N4纳米片通常要与具有更高导电性的材料结合,如石墨烯或CPs等 [8] 。本文采用化学氧化法制备了PEDOT聚合物和PEDOT/g-C3N4复合物应用于同时检测Cd2+和Pb2+。因为PEDOT高效的电荷转移能力、良好的可加工性以及主链中含有可吸附重金属的硫原子,将它与表面含有大量-NH和-NH2基团的g-C3N4进行复合后,可得到对重金属离子更为敏感的复合材料。因而在电化学检测重金属离子方面具有一定的实际应用价值。
2. 实验部分
2.1. 实验试剂及测试设备
3,4-乙撑二氧噻吩(EDOT) 99%百灵威科技有限公司;无水三氯化铁98%上海阿拉丁化学有限公司;尿素分析纯上海阿拉丁化学有限公司;醋酸钠(NaAc)分析纯天津致远化学试剂有限公司;醋酸镉分析纯天津致远化学试剂有限公司;醋酸铅分析纯天津致远化学试剂有限公司;冰醋酸(HAc)分析纯天津致远化学试剂有限公司;铁氰化钾分析纯天津致远化学试剂有限公司;氯化钾分析纯天津致远化学试剂有限公司;氯仿分析纯天津致远化学试剂有限公司;无水乙醇分析纯天津致远化学试剂有限公司。用NaAc和HAc制备了0.1 M的ABS缓冲液(pH = 4.5)。
红外光谱分析:德国BRUKER EQUINOX-55型傅立叶红外光谱仪,扫描波数范围为400~4000 cm−1。紫外可见吸收光谱(UV-vis)分析:美国UNICO UV-4802型紫外–可见光谱仪。X-射线粉末衍射测试:德国BRUKER AXS D8型X射线衍射仪,Cu-Ka辐射(λ = 0.15418 nm)为辐射源,扫描范围为2θ = 10˚~80˚。扫描电镜(SEM)分析:日本日立公司S-4800型场发射扫描电子显微镜(5 KV)。透射电镜(TEM)分析:日本HITACHI公司H-600型透射电子显微镜(100 KV)。电化学性能测试:上海辰华仪器有限公司电化学工作站CHI 660C化学工作站。
2.2. g-C3N4的合成
首先,在坩埚中加入10克尿素,放入马弗炉,以每分钟10˚C的升温速率加热至500˚C,随后保温2小时,再以每分钟10˚C的升温速率,加热到550˚C,再额外保温2小时。最后,将坩埚冷却到室温,得到黄色固体粉末,用无水乙醇和蒸馏水洗涤后,在烘箱中60˚C干燥,得到g-C3N4。
2.3. PEDOT/g-C3N4的合成
首先,将EDOT (0.3 g, 1 mmol)和加入30 mL氯仿中,随后加入一定量的g-C3N4并超声分散30分钟。另取无水氯化铁(0.65 g, 4 mmol)加入到5mL氯仿中,同时超声30分钟。然后,将两者超声完的反应液混合在一起,室温条件下搅拌24小时。最后,反应产物为一个黑色固体,过滤,依次用氯仿,蒸馏水和无水乙醇洗涤直至滤液无色,然后在真空条件下60℃干燥24小时,得到PEDOT/g-C3N4。以同样的方法,在不加入g-C3N4的情况下,得到PEDOT纯聚合物。
2.4. 电化学性能测试
首先是对玻碳电极(GCE)表面的清洁处理,将GCE在麝皮上进行抛光处理,所用的研磨剂为不同粒径大小的三氧化二铝(1.0, 0.3, 0.05 μm)浆料。然后将抛光好的电极分别用超纯水、浓硝酸、异丙醇依次超声洗涤,最后将电极放入40℃烘箱烘干备用。
修饰电极的制备通常分为悬浮液的制备和滴涂两个步骤。首先称取1 mg复合材料溶于4 mL异丙醇和超纯水的混合液中(1:1),超声处理30 min得到悬浮液。随后用十微升进样器吸取5微升悬浮液滴涂到处理好的电极表面,在室温下干燥。
循环伏安测试和微分脉冲测试均是在CHI 660C电化学工作站上进行。三电极体系由对电极(Pt)、参比电极(SCE)、工作电极(GCEs)组成。循环伏安法是在5 mM [Fe(CN)6]3−/4−和0.1M KCl (50 mL,体积比1:1)的混合溶液中进行,扫描量程为:−0.2~0.8 V;扫描速率为:50 ms。微分脉冲伏安法检测重金属离子是在PH = 4.5的ABS缓冲溶液中进行,电位范围是从−1.2 V增加到−0.2 V,脉冲宽度为50 ms,脉冲周期为100 ms。
3. 实验结果及讨论
3.1. 红外光谱分析
图1是g-C3N4,PEDOT和PEDOT/g-C3N4纳米复合材料的红外光谱图。在g-C3N4的光谱中,813 cm−1处的谱带被确定为平面三嗪环模式的弯曲振动。出现在890 cm−1处的弱峰可归因于交联七嗪的变形模式 [9] 。杂环中C-N和C=N的伸缩振动导致特征峰在1230~1650 cm−1范围内出现 [10] 。出现在3000~3500 cm−1区域的宽振动峰是由芳香族N-H键和未缩合氨基(-NH2)的伸缩振动引起的 [11] 。对于二元复合材料,如图所示,复合材料的主要振动带类似于PEDOT。在1515 cm−1和1320 cm−1处的特征峰分别是典型的C-C不对称伸缩振动和环间伸缩振动。约12,091,139和1088 cm−1的峰是乙二氧基中的C-O-C弯曲振动 [12] 。约974,918,833和693 cm−1处的谱带是噻吩环中C-S-C键的特征振动峰 [13] 。然而,在PEDOT/g-C3N4复合物中没有对应于g-C3N4的特征峰。原因可能是PEDOT的特征峰覆盖并接近g-C3N4的特征峰。
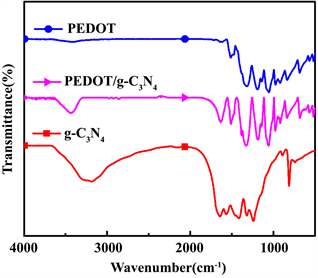
Figure 1. FTIR spectra of g-C3N4, PEDOT, PEDOT/g-C3N4
图1. g-C3N4, PEDOT, PEDOT/g-C3N4的红外光谱图
3.2. 紫外光谱分析
g-C3N4,PEDOT和PEDOT/g-C3N4复合材料的紫外–可见光谱如图2所示。从图中可以看出,g-C3N4
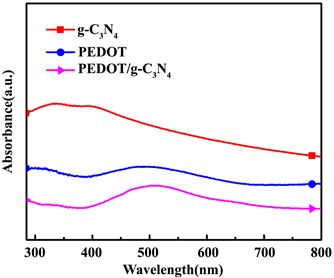
Figure 2.UV-vis spectra of g-C3N4, PEDOT, PEDOT/g-C3N4
图2. g-C3N4, PEDOT, PEDOT/g-C3N4的紫外光谱图
的吸收峰出现了在270至430 nm处,它们是碳氮化物的特征吸收峰。PEDOT和PEDOT/g-C3N4的吸收带出现在大约400~600 nm处可归因于聚合物共轭主链长度 [14] ,并且它们被指定为噻吩环的π-π跃迁产生的吸收峰。此外,PEDOT/g-C3N4在600~667 nm处的吸收峰归属于PEDOT的极化子和/或双极化子带 [15] ,这表明PEDOT和g-C3N4之间具有一定π-π相互作用。
3.3. XRD分析
图3 显示了g-C3N4,PEDOT和PEDOT/g-C3N4复合材料的XRD谱图。在图中,g-C3N4的衍射峰为27.3˚,这可以归结于石墨材料的(002)的衍射面上,是作为石墨结构的典型平面结构。PEDOT和PEDOT/g-C3N4的XRD图谱在约2θ = 26.2˚处也显示出特征峰,这是由于PEDOT分子间π-π堆积作用造成的。此外,由于FeCl4−在PEDOT和PEDOT/g-C3N4中的掺杂,该使得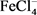 尖锐的衍射峰也出现在2θ ≈ 33˚, 35˚, 49˚和54˚等处 [16] 。
尖锐的衍射峰也出现在2θ ≈ 33˚, 35˚, 49˚和54˚等处 [16] 。

Figure 3. XRD patterns of g-C3N4, PEDOT, PEDOT/g-C3N4
图3. g-C3N4,PEDOT,PEDOT/g-C3N4的XRD图
3.4. 形貌分析
图4和图5分别为g-C3N4,PEDOT,PEDOT/g-C3N4的SEM和TEM图像。如图所示,g-C3N4表现出超薄的无规则叠层片状结构,PEDOT则显示出无规则的团状结构。对于二元复合物,则同样为无规则的团状结构。在图5(c)中,可以发现无规则的PEDOT包裹着薄片状的g-C3N4。

Figure 4. SEM images of (a) g-C3N4 (b) PEDOT (c) PEDOT/g-C3N4
图4. (a) g-C3N4 (b) PEDOT (c) PEDOT/g-C3N4的扫描电镜图

Figure 5. TEM images of (a) g-C3N4 (b) PEDOT (c) PEDOT/g-C3N4
图5. (a) g-C3N4 (b) PEDOT (c) PEDOT/g-C3N4的透射电镜图
3.5. 电化学性能测试
为了研究g-C3N4,PEDOT,PEDOT/g-C3N4的电化学活性,在5 mM [Fe(CN)6]3−/4−和0.1M KCl (50 mL,体积比1:1)的混合溶液中对不同的改性GCE进行循环伏安测试,如图6所示。从图中可以看出PEDOT/g-C3N4复合改性的GCE表现出比其他GCE更强的峰值电流,说明该比例的复合物具有较快的电子转移能力。这可以解释为加入g-C3N4得到的二元复合材料,具有更好的π-π叠加效应并且不会造成材料导电性下降。
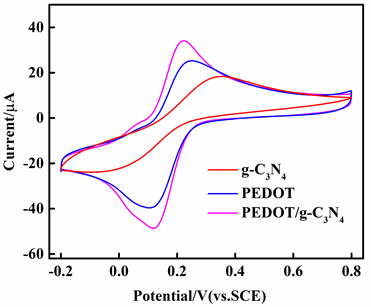
Figure 6. CV measured with g-C3N4, PEDOT, PEDOT/g-C3N4 composite-modified glassy carbon electrode (GCE) in a solution of 5 mM Fe(CN)63−/4− containing 0.1 M KCl
图6. g-C3N4,PEDOT, PEDOT/g-C3N4在5 mM Fe(CN)63−/4−和0.1 M KCl中的循环伏安图
图7为不同改性GCEs在0.1 M ABS (PH = 4.5)溶液中2 μM Cd2+和Pb2+的DPV曲线。如图所示,Cd2+和Pb2+的特征峰之间的距离足够宽,Cd2+和Pb2+的峰位分别约为−0.81 V和−0.58 V。如图所示,PEDOT/g-C3N4复合物改性GCE的溶出电流值的最高,主要原因是PEDOT/g-C3N4二元复合物发挥了各组分的协同作用,增强了复合材料的电化学性能,在一定程度上提高了溶出电流值。
为了系统地研究PEDOT/g-C3N4的电化学检测性能,采用DPV作为检测手段,在最优的参数设置下,研究了PEDOT/g-C3N4在0.1 M ABS (pH = 4.5)中对Cd2+和Pb2+的电化学检测性能。如图8所示,从图中可以发现PEDOT/g-C3N4对Cd2+和Pb2+均具有较好的线性检测范围,其中在−0.8 V附近出现的电流峰是Cd2+的电流峰,−0.6 V附近的电流峰是Pb2+的电流峰,并且这两个电流峰的位置没有相互叠加。
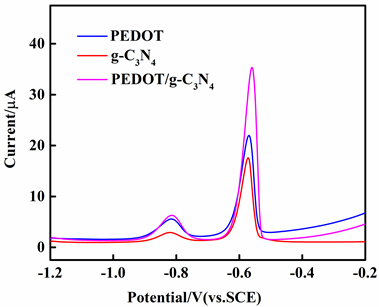
Figure 7. DPV of g-C3N4, PEDOT, PEDOT/g-C3N4 composite-modified GCE in 0.1M ABS (pH = 4.5) containing 2 µM of Cd2+ and Pb2+
图7. g-C3N4,PEDOT,PEDOT/g-C3N4修饰的GCE同时检测Cd2+和Pb2+ (2 µM) DPV的曲线图

Figure 8. DPV response of the PEDOT/g-C3N4 composite-modified GCE for the individual analysis of (a) Cd2+ over a concentration range of 0.1 - 3.6 µM; (b) Pb2+ over a concentration range of 0.1 - 2.8 µM. The inset shows their linear equations as well as correlation coefficient
图8. PEDOT/g-C3N4对Cd2+和Pb2+的单独检测的DPV曲线图;(a) Cd2+,线性范围是0.1~3.6 µM;(b) Pb2+,线性范围是0.1~2.8 µM;插图为其各自的浓度–电流曲线图
说明PEDOT/g-C3N4具有能够同时测定Cd2+和Pb2+的可能性。在图8的插图中,可以看出检测Cd2+的线性浓度范围为0.1~3.6 μΜ,相应的线性方程为y(μA) = 1.6021x + 0.2147 (R2 = 0.9923);检测Pb2+的线性浓度范围为0.1~2.8 μΜ。相对应的线性方程为y(μA) = 27.3213x + 5.1612 (R2 = 0.9844)。其中y(μA)代表阳极溶出的电流值,x代表加入Cd2+和Pb2+的量(μM)。Cd2+和Pb2+的最低检测限(LOD)分别为0.0384 μM和0.00641 μM (S/N = 3)。
为了同时测定Cd2+和Pb2+,在相同的实验条件下,研究了PEDOT/g-C3N4在0.1 M ABS (pH = 4.5)对同时检测Cd2+和Pb2+的线性关系。图9为PEDOT/g-C3N4检测Cd2+和Pb2+的DPV曲线图以及Cd2+和Pb2+的检测线性方程和相关系数。从图中可以得知,Cd2+和Pb2+的线性范围为0.1~2.8 μM,Cd2+和Pb2+的检出限为0.0547 μM和0.00794 μM。说明PEDOT/g-C3N4在一定浓度范围内,也可以对Cd2+和Pb2+同时检测。
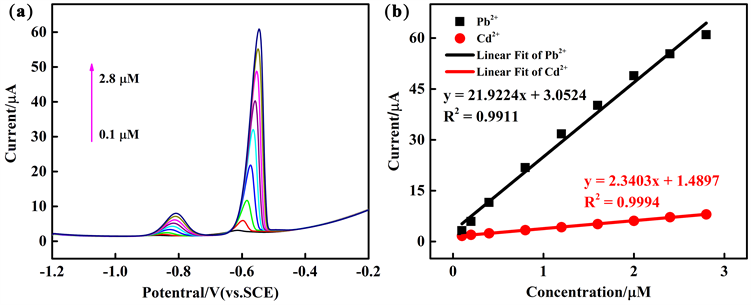
Figure 9. (a) DPV response of the PEDOT/10wt%g-C3N4 composite-modified GCE for the simultaneous analysis of Cd2+ and Pb2+ over a concentration range of 0.1 - 2.8 µM; (b) the respective calibration curves of Cd2+ and Pb2+
图9. (a) PEDOT/10wt%g-C3N4改性电极对Cd2+ (0.1~2.8 µM)和 Pb2+ (0.1~2.8 µM)同时检测的DPV曲线图;(b) 检测Cd2+和 Pb2+分别对应的浓度–电流曲线图
对PEDOT/g-C3N4修饰的电极进行离子干扰研究,从图10(a)可以看出,在1 μM Cd2+和Pb2+分析标准溶液中,加入浓度为5倍检测标准液的干扰金属阳离子如Zn2+, Ni2+, Na+, Mn2+, Li+, K+。结果表明,PEDOT/g-C3N4修饰的电极对部分金属具有较好的抗干扰能力,其检测Cd2+和Pb2+的峰值电流略有变化,误差低于±10%。图10(b)可以看出,复合物修饰电极在7天内具有较好的循环稳定性,对于同时检测Cd2+和Pb2+具有一定的实际应用价值。

Figure 10. Interference of (a) metal ions (10-fold concentration) on the peak currents of Cd2+ and Pb2+ simultaneous detection; (b)Stability curves of PEDOT/g-C3N4/GCE
图10. (a) PEDOT/g-C3N4改性电极的离子干扰图;(b) PEDOT/g-C3N4改性电极的循环寿命图
4. 结论
本文采用化学氧化法制备了PEDOT/g-C3N4复合材料,通过各种表征手段对其进行了结构分析同时应用于对Cd2+和Pb2+的电化学测定。结果表明,g-C3N4作为复合相的加入增加了活性位点(-NH)和(-NH2),增强了复合材料对Cd2+和Pb2+的吸附能力;同时PEDOT与g-C3N4之间相互的π-π作用,提高了复合材料的导电性,发挥出了各自组分的协同效应。最后的性能表明:复合材料对Cd2+的线性检测浓度范围为0.1~3.6 μΜ;Pb2+的线性浓度范围为0.1~2.8 μΜ;Cd2+和Pb2+的最低检测限(LOD)分别为0.0384 μM和0.00641 μM (S/N = 3)。PEDOT/g-C3N4复合材料有望在环境检测重金属离子方面有所发展。
基金项目
感谢国家自然科学基金(No. 21564014)。