1. 引言
近年来,随着印染、皮革等产业的快速发展,染料废水的排放量呈逐年上升的趋势,据统计,染料的年产量已经超过70万吨,每年有10%~15%的染料废水排放到环境中,对人体健康和生态环境造成的影响日益严重 [1] 。亚甲基蓝是一种有机染料,常作为麻、蚕丝织物、纸张的染色和竹的着色的化学染料 [2] ,由于这种染料含有稳定的苯环结构,并具有一定的毒性,其在废水中浓度高,色度深,排放量大,难降解 [3] ,已成为废水处理的一大难题,因此,去除水中过量的亚甲基蓝成为一个关键性的环境挑战问题 [4] 。目前许多技术已经应用于去除染料,如光催化降解 [5] ,生物降解 [6] ,离子交换 [7] 和化学沉淀法 [8] 等,但这些方法比较费时且成本较高。相反吸附法设备简单,具有效率高,操作简单,成本低廉等特点,因而被广泛应用 [9] 。
自然界中,储量大、生物相容性好、无毒的壳聚糖,其分子式为(C6H11NO4),是甲壳素脱乙酰化的产物,是一种多羟基和氨基的线性型高分子聚合物,含氧基团的存在,增加了其对染料的吸附能力 [10] 。壳聚糖具有许多的生物性能,如亲水性,生物降解性,生物相容性且无毒 [11] ,被广泛应用于去除金属离子 [12] 、染料 [13] 和蛋白质 [14] 等,在水处理领域具有良好的应用前景。但由于壳聚糖分子结构中的氨基、羟基之间有较强的氢键,致使其水溶性较差 [15] ,只溶于盐酸、硝酸、醋酸等一些稀酸,这给壳聚糖的应用带来极大的局限 [16] ,因此需要对其改性,交联后的壳聚糖获得了新的官能团、改变了对吸附剂的选择性,提高了吸附能力,其性质在不同程度上都会得到提高。
活性炭是比较特殊的碳质材料,是一类具有石墨微晶的无定形的碳 [17] 。主要化学成分是碳元素及少量的氢元素、氮元素、氧元素、灰分,含有丰富的官能团、巨大的比表面积以及发达的孔隙 [18] [19] ,因而利用其对印染废水的处理越来越得到重视。但因活性炭形状不均,回收较困难,造成了巨大的浪费,因此需要制备一种成形性较好且容易回收的多孔吸附材料。
本文采用交联,固化和冷冻干燥的方法制备了AC/CHI多孔小球。这种多孔小球充分结合了壳聚糖中的含氧官能团,活性炭的大量微孔及优异吸附性能等特点,不仅可以高效的去除亚甲基蓝,并且还不会造成二次污染。本文通过一系列的实验对多孔小球对亚甲基蓝的吸附性能和吸附机制进行了研究,通过SEM和FTIR等方式对多孔小球的化学结构性质和表面形貌进行表征分析,并研究了温度、吸附剂的加入量、吸附反应时间以及溶液初始pH等因素对吸附过程的影响。
2. 实验
2.1. 主要原料与仪器
活性炭(activated carbon):山东省青岛市场;壳聚糖(chitosan):上海蓝季科技发展有限公司;氢氧化钠(NaOH):江苏强盛功能化学股份有限公司;醋酸(CH3COOH):国药集团化学试剂有限公司;亚甲基蓝(MB):天津市广成化学试剂有限公司。
水浴恒温振荡器(SHZ-82A):上海双捷实验设备有限公司;紫外可见分光光度计(TU-1810):北京普析通用仪器有限公司;磁力搅拌器(85-2):上海双捷实验设备有限公司;电子天平(BSM224.4):上海卓京实验设备有限公司;真空冷冻干燥机(FD-1B-50):北京博医康实验仪器有限公司;电热鼓风干燥箱(101-1):龙口市电炉制造厂;PH计(PHS-3C型精密)。冰箱(BCD-215KAW):青岛海尔。
2.2. 壳聚糖溶液的制备
准确称取1.2 g壳聚糖粉末,溶于40 mL 2%的醋酸溶液中,于25℃恒温搅拌2 h,制成质量分数为3%的壳聚糖溶液(3%的壳聚糖溶液成形性最好)。重复以上操作,制备五份相同的溶液待用。
2.3. 活性炭/壳聚糖多孔小球的制备
分别将0.1 g、0.5 g、1.0 g、1.5 g、2.0 g的活性炭加入到壳聚糖溶液中,继续搅拌2 h后,将交联后的复合物分别用针管滴入到用300 mL质量分数为5%氢氧化钠进行小球成形固化,在氢氧化钠溶液中固化一天后,用去离子水清洗至pH值为6~7。将水洗后的AC/CHI多孔小球倒入培养皿中,用保鲜膜封好,放入冰箱中冷冻一晚上。将冷冻好的AC/CHI多孔小球,放入真空干燥机,干燥12 h制成样品。
2.4. 吸附剂的表征
通过Nicolet5700傅里叶变换红外光谱仪(FTIR)扫描其红外光谱,对AC/CHI多孔小球的表面官能团进行分析。采用TM-3000 扫描电子显微镜(SEM)对其表面形貌进行表征。
2.5. 吸附实验
通过实验测试了不同温度、吸附剂加入量、接触时间以及溶液初始pH对AC/CHI多孔小球吸附亚甲基蓝性能的影响,并对吸附等温线,吸附热力学和动力学进行了讨论,探究了AC/CHI多孔小球对亚甲基蓝的吸附机制。
首先将亚甲基蓝溶于蒸馏水,得到1000 mg/L的亚甲基蓝溶液。通过稀释,将浓度为1000 mg/L的亚甲基蓝溶液配制成所需的不同浓度的溶液,然后将10 g吸附剂加入到20 mL亚甲基蓝溶液中,其初始浓度从60~160 mg/L。将其放入恒温水浴振荡器中,在室温下振荡直至达到平衡。之后用紫外可见分光光度计测定平衡时亚甲基蓝的浓度。平衡吸附量可由以下公式计算:
(1)
其中,C0和Ce分别代表亚甲基蓝的初始浓度(mg/L)和平衡浓度(mg/L),W代表吸附剂的质量(g),V代表亚甲基蓝溶液的体积(mL)。
热力学研究时,分别在303、313和323 K的温度下,将10 mg吸附剂加入20 mL浓度为60~160 mg/L的亚甲基蓝溶液中进行吸附实验,直到吸附平衡,以此研究温度对吸附性能的影响。通过将不同质量的吸附剂(5~35 mg)加入到20 mL浓度60 mg/L的亚甲基蓝溶液中进行吸附,来研究吸附剂加入量对吸附性能的影响。通过将相同质量(20 mg)的吸附剂加入初始浓度相同(160 mg/L)但溶液的初始pH不同(3到11)的亚甲基蓝溶液中,探究pH值对亚甲基蓝吸附性能的影响。研究接触时间的影响时,将125 mg吸附剂加入到250 mL浓度为160 mg/L的亚甲基蓝溶液中,在预定的时间间隔内,取适量亚甲基蓝溶液,测定其浓度随时间段的变化,在时间t,吸附剂的吸附容量qt (mg/g)可用以下公式计算:
(2)
其中,Ct (mg/L)代表亚甲基蓝在时间t时的浓度。
3. 结果与讨论
3.1. 吸附剂的表征
图1(a)为在氢氧化钠溶液中固化后的AC/CHI多孔小球,表面光滑,含有水分。图1(b)为经过冰箱冷冻后的AC/CHI多孔小球,样品之间有一层薄薄的冰,将其连成一片。图1(c)为真空冷冻干燥机干燥之后的AC/CHI多孔小球的光学照片,可以看出冷冻干燥处理的AC/CHI多孔小球,由于升华作用,变得疏松多孔,形状大小均一。
图2(a)为壳聚糖的扫描电镜图,从图中看出壳聚糖具有层状结构而且其表面较为粗糙。图2(b)为AC/CHI多孔小球的扫描电镜图,随着活性炭含量的加入,AC/CHI多孔小球的表面逐渐出现更多的沟壑和褶皱且具有丰富的多孔结构,这使其比表面积和吸附位点大大增加,有利于提高吸附能力。
傅里叶变换红外光谱是定性确定特征官能团的最重要指数之一,图3为AC/CHI多孔小球的红外光谱图。图3(a)为壳聚糖的光谱图,在1077,1370,1593,2900,和3368 cm−1处有吸收峰,他们分别对应于C−O−C的伸缩振动,羧基中C−OH的伸缩振动,O−H的弯曲振动,C−H伸缩振动和−OH的伸缩振动。图3(b)为活性炭的红外光谱图,在1045,1160和1590 cm−1处有吸收峰,分别对应羧基和羰基C−O−C的伸缩振动,C−O的伸缩振动,C=C的伸缩振动,图3(c)为AC/CHI多孔小球的红外谱图,其官能团种类丰富,提高了材料的吸附性能。对比AC/CHI多孔小球与壳聚糖和活性炭的红外谱图可知,多孔小球包含活性炭和壳聚糖的所有吸收峰,由此表明活性炭和壳聚糖成功复合成AC/CHI多孔小球。
3.2. 不同活性炭含量对吸附性能的影响
图4为不同含量的AC/CHI多孔小球对亚甲基蓝吸附容量的比较。从图中可以看出,随着活性炭含量的增加,AC/CHI多孔小球对亚甲基蓝的吸附容量逐渐增加,随着活性炭的含量由0.1增加到到2 g时,吸附容量由129.71 mg/g增加到140.39 mg/g,吸附容量的逐渐增加主要归因于活性炭比例的增加,但如果继续增加活性炭,活性炭/壳聚糖的混合溶液将析出沉淀,不能完全溶解。所以接下来的吸附实验中都选择活性炭的含量为2 g,3%的壳聚糖溶液的多孔小球作为吸附剂,来讨论其吸附性能。

Figure 1. Photographs of AC/CHI (a) The curing; (b) The frozen in a refrigerator; (c) The freeze dried
图1. 活性炭/壳聚糖多孔小球的光学照片(a)固化后;(b)冷冻后;(c)干燥后

Figure 2. SEM images of (a) CHI; and (b) AC/CHI
图2. 扫描电镜图(a)壳聚糖;(b)活性炭/壳聚糖多孔小球

Figure 3. FT-IR spectra of (a) CHI; (b) AC; and (c) AC/CHI
图3. 红外光谱图(a)壳聚糖;(b)活性炭;(c)活性炭/壳聚糖多孔小球
3.3. 温度对吸附性能的影响
温度是决定吸附过程的重要因素之一。它影响吸附剂的物理化学性质和吸附分子的扩散速率,从而决定吸附容量 [20] 。本实验分别在303,313和323 K下研究了温度对AC/CHI多孔小球吸附亚甲基蓝的影响,结果如图5(a)所示,可以看出吸附容量随温度的升高而增加,这可能是由于较高的温度会增强AC/CHI多孔小球和染料分子之间的静电相互作用力,在亚甲基蓝平衡浓度为3 mg/L和323 K时,吸附容量达到313.18 mg/g。实验结果表明亚甲基蓝吸附在AC/CHI多孔小球上的吸附过程是一个吸热反应。
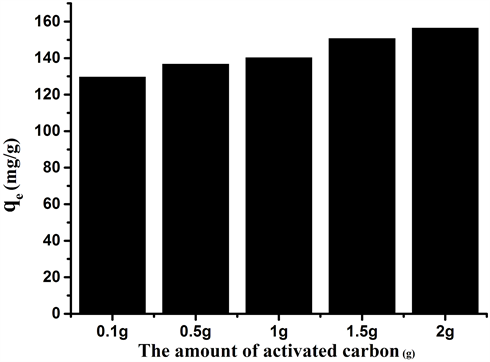
Figure 4. Adsorption of methylene blue with different AC content (initial methylene blue concentration: 160 mg/L, adsorption dose: 10 mg, temperature: 303 K, pH: 6.5)
图4. 不同活性炭含量对亚甲基蓝的吸附性能研究(初始亚甲基蓝的浓度:160 mg/L,吸附剂量:10 mg,温度:303 K,pH:6.5)
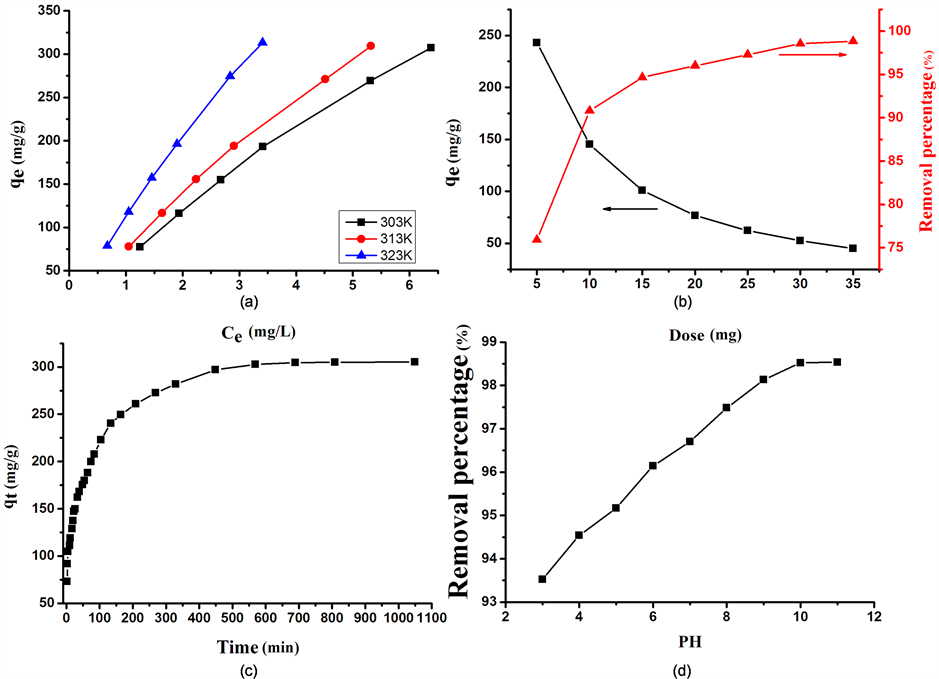
Figure 5. Effect of different factors on MB adsorbed by AC/CHI: (a) Temperature effect; (b) Dose effect; (c) Contact time effect; (d) pH effect
图5. 不同因素对活性炭/壳聚糖多孔小球吸附亚甲基蓝性能的影响:(a) 温度的影响;(b) 吸附剂量的影响;(c) 接触时间的影响;(d) pH的影响
3.4. 吸附剂加入量对吸附性能的影响
吸附剂加入量是影响吸附效率的另一重要参数。图5(b)显示了吸附剂加入量对吸附容量和去除率的影响,显然在初始阶段,随着吸附剂加入量的增加,去除率显著增加,这主要是因为增加的吸附剂量增多了可用吸附位点的数量 [21] 。随着接触时间延长,去除率变得缓慢增加,原因是由于饱和而不能获得更多的吸附位点。从图5(b)中还可以看出,随着吸附剂剂量增加,吸附容量降低。这可能是由于所有活性位点都被低剂量的AC/CHI利用。即,单位质量吸附剂吸附染料的量减少,导致活性位点利用率下降 [22] 。
3.5. 接触时间对吸附性能的影响
研究接触时间对AC/CHI多孔小球吸附亚甲基蓝的影响,亚甲基蓝的初始浓度为160 mg/L,温度为30℃,由图5(c)可以看出,随着接触时间从0增加到210分钟,AC/CHI多孔小球对亚甲基蓝的吸附容量迅速增加,因为有大量的空位吸附位点和可用的吸附剂表面积。在约570分钟时,吸附容量达到平衡,平衡吸附量为305.34 mg/g。之后,吸附速率开始逐渐减慢,主要是因为亚甲基蓝浓度下降,导致吸附驱动力下降和吸附剂表面活性吸附位点减少。
3.6. 溶液的初始pH值对吸附的影响
溶液的初始pH值是影响吸附过程的重要因素之一。它通过改变吸附剂和被吸附物表面官能团的质子化来影响吸附 [23] 。图5(d)显示了溶液的pH值(从3到12)对亚甲基蓝去除率的影响,去除率随pH值的增加而增大。亚甲基蓝是一种阳离子染料,含有带正电荷的季铵基(N+(CH3)2Cl−)。在较低的pH值下,氢离子和亚甲基蓝分子在相同的吸附活性位点上的竞争,导致AC/CHI多孔小球对亚甲基蓝分子的去除率较低 [24] 。此外,亚甲基蓝分子与氢离子之间存在静电斥力,降低了其吸附能力。当pH值升高时,在碱性环境中,氢离子竞争减弱。羟基和亚甲基蓝分子之间的静电引力,使得吸附能力变得更强,去除率增大。
3.7. 吸附等温线研究
很多数学模型已被用于描述吸附剂吸附量与溶液中残留浓度之间的关系。等温线模型的选择取决于吸附剂和吸附质的性质和类型 [25] 。朗缪尔模型和弗伦德里希模型是研究吸附平衡最常用的模型。在本实验中,采用朗缪尔模型和弗伦德里希模型进一步研究AC/CHI的吸附能力并分析吸附剂与被吸附质之间的反应。朗缪尔模型假设吸附是均匀发生在表面上的单层吸附,并且所有吸附位点都是相同的,相互独立。朗缪尔等温线的方程 [26] 如下:
(3)
其中,qmax (mg/g)是最大吸附容量,kL (L/g)是朗缪尔常数。对上述方程式的散点图进行线性拟合,可以得到一条线性的曲线如图6(a)所示,根据图中的曲线的斜率和截距可以得到qmax和kL的数值(见表1)。通过朗缪尔模型可以得出在303,313和323 K时的最大的理论吸附吸附容量分别为1101.25,1123.27和1194.33 mg/g。朗缪尔方程的决定系数R2 > 0.99,表明AC/CHI多孔小球对亚甲基蓝的吸附数据符合朗缪尔模型,主要为单分子层吸附。
无量纲平衡参数RL也可以用来描述朗缪尔等温线,其数学表达式为:
(4)
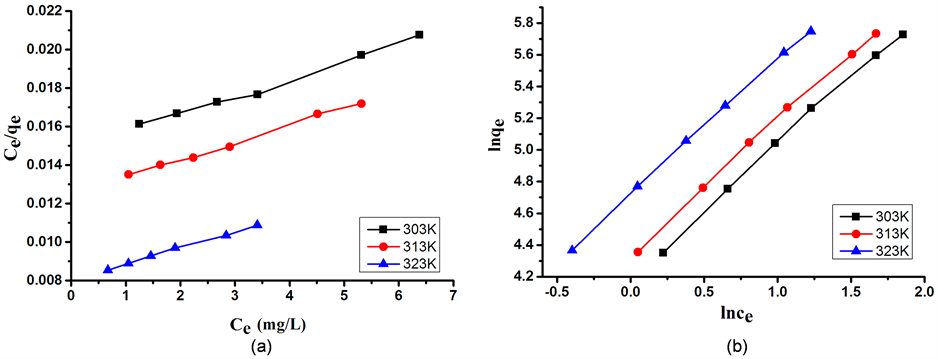
Figure 6. The equilibrium plots for the adsorption MB on to the AC/CHI: (a) Langmuir model equilibrium; (b) Freundlich model equilibrium plots
图6. 活性炭/壳聚糖多孔小球吸附亚甲基蓝的平衡模型:(a) 朗缪尔模型;(b) 弗伦德里希模型

Table 1. The adsorption isotherm constants of Langmuir and Freundlich model for MB onto AC/CHI
表1. 活性炭/壳聚糖多孔小球吸附亚甲基蓝的朗缪尔和弗伦德里希模型参数
其中,kL表示朗缪尔常数(L/mg),C0是初始亚甲基蓝浓度(mg/L)。RL值表示朗缪尔等温线是有利于吸附发生(0 < RL < 1),不利于吸附发生(RL > 1),呈线性(RL = 1),不可逆(RL = 0)。在实验中,所有RL值均在0和1之间,表明AC/CHI多孔小球对亚甲基蓝具有较好的吸附性能。
弗伦德里希模型假定吸附过程发生在非均匀表面上,方程 [27] 如下:
(5)
其中,KF (L/g)是一个与吸附容量有关的弗伦德里希常数,1/n是一个与吸附强度有关的溶剂参数。通过该模型拟合,可以得到一条线性曲线,如图6(b)所示,其中kF和1/n的值可以通过截距和斜率进行计算得出(见表1)。弗伦德里希方程的决定系数R2 > 0.99,说明AC/CHI多孔小球对亚甲基蓝也符合弗伦德里希模型。
朗缪尔和弗伦德里希等温线图和参数表明吸附符合两种模型,根据朗缪尔方程计算知,在pH为6和温度为323 K时,AC/CHI多孔小球的最大吸附量达到1194.33 mg/g。表明AC/CHI多孔小球是一种很有应用前景的吸附剂。由弗伦德里希方程计算知,1/n的值小于1,表明有利于吸附反应的进行。
3.8. 吸附动力学研究
几个动力学模型包括准一级动力学模型,准二级动力学模型和内部粒子扩散模型常用于评估吸附数据。
准一级动力学模型的方程 [28] :
(6)
其中k1 (1/min)是准一级吸附速率常数,qe和qt是达到吸附平衡和在时间t (min)时的吸附容量(mg/g)。通过log(qe − qt)对t的拟合直线(图7(a))的斜率和截距计算,得到k1和qe的数值(见表2)。虽然决定系数(R2)接近于1,但计算得到的qe (194.09 mg/g)和实验所得qe值(305.34 mg/g)有较大差异,表明准一级动力学模型不太适用于本实验。
准二级动力学模型的方程 [29] :
(7)
其中k2 (g/(mg min))是准二级吸附速率常数,通过t/qt对t的拟合直线(图7(a))的斜率和截距进行计算,得到k2和qe的数值。测定系数为0.9982,接近于1。且经过计算得到的qe值(314.47 mg/g)与实验所得qe值(305.34 mg/g)十分接近,表明准二级动力学模型能准确的描述AC/CHI多孔小球对亚甲基蓝的吸附动力学数据。这意味着吸附速率受化学吸附控制,并且吸附剂和被吸附物通过共享电子或共价力进行电子交换。
内部粒子扩散模型通常用于确定多孔结构中的速率控制步骤,其方程如下所示 [30] :
(8)
其中t1/2是时间的平方根,kid (mg/g min1/2)是内部粒子扩散模型常数和C与分子扩散边界层的厚度有关。通过qt对t1/2的拟合直线(图7(c))的截距和斜率计算,得出速率常数kid和C (见表2)。内部粒子扩散模型的决定系数R2在0.9605和0.6192之间,低于准二级方程。 曲线是非线性且截距不等于零,没有经过原点,这表明内部粒子扩散不是唯一的速率控制步骤,并且亚甲基蓝在AC/CHI多孔小球上的吸附是一个复杂的过程。
3.9. 吸附热力学研究
为了研究温度对AC/CHI多孔小球对亚甲基蓝吸附过程的影响,在不同温度下测定了AC/CHI多孔小球对亚甲基蓝的热力学参数。用Van’t Hoff方程 [31] 计算焓变(ΔH)和熵变(ΔS),如下:
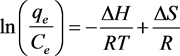 (9)
(9)
吉布斯自由能(ΔG)可以通过以下方程计算:
(10)
其中T(K)代表绝对温度,R (8.314 J/(mol K))代表通用气体常数。根据斜率和截距计算ΔH和ΔS的值(见表3)。ΔG是负值,表明吸附过程是自发的。此外,随着温度的升高,从303到323 K,ΔG相应地从−10.2降低到−12.6 kJ/mol,表明较高的温度更有利于吸附。ΔH (26.16 kJ/mol)的正值证实了AC/CHI多孔小球吸附亚甲基蓝相互作用是吸热过程。正熵变ΔS表明在吸附过程中固-液界面的吸附作用随机性增加 [32] 。
4. 结论
本文通过交联、固化和冷冻干燥的方法制备了壳聚糖/活性炭(AC/CHI)多孔小球,采用扫描电子显微镜(SEM)和傅里叶变换红外光谱仪(FTIR)对其表面形貌和化学结构性质进行表征分析,通过改变温度、吸附剂加入量、接触时间和溶液初始pH等因素,探究了AC/CHI多孔小球对亚甲基蓝的吸附性能。动力学研究结果表明,该吸附过程更符合准二级动力学模型。吸附等温线结果证明,朗缪尔,弗伦德里希模型

Figure 7. Adsorption kinetics of MB adsorbed by AC/CHI: (a) Pseudo-first-order model; (b) Pseudo-second-order model; (c) Intra-particle diffusion model
图7. 活性炭/壳聚糖多孔小球吸附亚甲基蓝的动力学模型:(a) 准一级动力学模型;(b) 准二级动力学模型;(c) 内部粒子扩散模型

Table 2. The parameters of pseudo-first-order, pseudo-second-order and intra-particle diffusion models
表2. 活性炭/壳聚糖多孔小球吸附亚甲基蓝的准一级和准二级动力学和内部粒子扩散模型拟合参数

Table 3. Thermodynamic parameters at different temperatures
表3. 不同温度下的热力学参数
都能对AC/CHI多孔小球吸附亚甲基蓝的数据进行很好的拟合(决定系数R2均在0.99左右)。按朗缪尔方程拟合得出,在323 K时能达到最大的理论吸附量为1194.33 mg/g。热力学参数则说明该吸附是一个吸热和自发的过程。
基金项目
国家自然科学基金(51672140和51573080),山东省自然科学基金(ZR2015EM038)和山东省泰山学者特聘专家(ts201511029)项目资助。
NOTES
*通讯作者。