1. 引言
糖类作为一种重要的能源物质,被广泛的应用于各个领域,因而受到各界的广泛关注。其中,糖类的检测是一个重要的研究方向。目前,传感法是最常见的一种葡萄糖检测手段。即利用传感器,对葡萄糖进行电催化氧化,根据电流与浓度的线性关系,得到葡萄糖浓度,从而实现葡萄糖含量的检测。该方法因为具有准确、快速、可靠等优点而被广泛应用 [1] 。此外,与传感过程类似,糖类还可作为燃料电池中的燃料,因其具有无毒、价格便宜等特点而受到广泛关注 [2] 。
根据电极传感器上负载物的种类,可以把电极分为酶电极和非酶电极。虽然酶电极传感器具有较高的灵敏度和一定的选择性,但是由于其较高的成本,且容易受到环境中的温度、pH和湿度的影响,故其应用受到了很大的限制 [3] 。而非酶传感器由于具有稳定性高、可重复使用等特点而得到广泛的应用。目前,已有许多将金属/金属氧化物纳米材料应用于化学传感器和生物传感器的报道。常见的用于构建非酶传感器的纳米材料,包括铂、金、钯、铜及它们的合金与氧化物等纳米材料 [3] 。其中,以铂、金、钯等贵金属材料构建的传感器,虽然具有着较高的灵敏度,但是由于其价格较高,因而应用受到很大限制。因此,发展一种新型、廉价、高效而又稳定性强的非酶传感器具有一定的意义。
铜及其氧化物是常见的非贵金属材料,因其在碱性条件下对糖类具有催化氧化性能而常常被应用于非酶葡萄糖传感器 [4] 。其中,Cu2O作为一种p型结构半导体,由于其独特的光电效应、低成本、不易中毒等特点已经被应用在许多领域中,如传感器、催化和能源等领域 [5] 。利用Cu2O所构建的传感器,可以实现对被测物的吸附(通过铜d-轨道中d-电子与待测物的结合),而不影响待测物的脱附过程,进而使得电极可以被重复利用 [6] 。然而,葡萄糖等有机分子在发生电催化氧化(即失去氢原子)的同时,会产生一定的化学吸附。这意味着材料相邻的活性位点会被葡萄糖占用,进而使得传感器的响应速度以及准确度有所下降。因此,将铜及其氧化物制备成传感器并用于葡萄糖的检测,受到了一定的限制。
研究表明,将Cu2O等纳米材料负载至一些比表面积较大,导电性较好的基底上,如碳纳米管 [7] 、石墨烯等材料 [8] ,可以实现纳米粒子的有效分散,增加其表面活性位点的数量,最终实现对葡萄糖催化氧化性能的提升。二氧化钛纳米管(TNTs)是一种常见的一维材料。因其具有较大的比表面积、优良的稳定性、且金属钛具有较好的导电性,被广泛的作为基底而用于催化传感等领域 [9] [10] 。作者此前以硫酸铜为铜源,在乳酸的水溶液条件中,采用恒电位电沉积法,成功制备了新型Cu2O改性螺旋状TiO2纳米管阵列传感器 [11] ,并将其应用于碱性条件下的葡萄糖检测 [12] 。在这里,我们在采用二次阳极氧化法制备出二氧化钛纳米管的工作基础上,通过控制更负的沉积电位,让Cu与Cu2O颗粒同时沉积在TiO2纳米管阵列上。期望能够利用Cu的良好导电性,以及Cu2O与TiO2的协同作用,能有效提升其对糖的催化氧化性能。我们探讨了CCT电极分别对葡萄糖、果糖和蔗糖的电催化氧化性能,并考察了将其应用于三种糖类检测的可能性,最后对不同糖类的催化氧化机理进行了分析。该材料对糖类展现出了较好的催化氧化性能,未来有望作为阳极材料用于生物燃料电池领域。
2. 实验
根据我们之前的工作,采用二次阳极氧化法制备得到TNTS,随后采用电沉积法制备CCT [12] ,其沉积电位控制为−1.4 V。采用DX-2700型X射线衍射仪记录样品的XRD图谱,其中扫描速率为0.05˚ s−1,角度范围为20˚至80˚;采用NanoSEM230场发射扫描电子显微镜获得材料形貌图像,其中施加的电流和电压分别为40 mA和40 kV。我们利用电化学工作站(CHI660B)进行循环伏安测试与电流计时法测试,电极体系为三电极体系。其中,CCT作为工作电极,铂片作为对电极,饱和甘汞电极(SCE)作为参比电极,电解液由2 mM的糖溶液和0.1 M的NaOH溶液组成的混合溶液。循环伏安曲线的电压范围为0到0.8 V (vs.SCE);电流计时曲线分别在葡萄糖、果糖和蔗糖的最佳氧化电位下进行,通过采用磁力搅拌提供对流传质以确保溶液均匀。初始250 s内每隔50 s加入10 μL 1 M的糖溶液,250 s后逐渐滴加40 μL 1 M糖溶液至1000 s,分别得到葡萄糖、果糖和蔗糖的计时电流曲线。
3. 结果与讨论
3.1. CCT电极的结构与形貌
TNTs在500℃下煅烧3 h,随后采用退火处理。这是因为预退火处理有利于TNTs负载Cu2O [13] ,故采用预退火处理电极。图1为TNTs与CCT电极的XRD图。图1(A)中2θ = 43.4˚和50.4˚的峰(a = 0.3615 nm)对应于立方晶型Cu (JCPDS-04-0836)单质的特征峰,而2θ = 36.5˚和29.6˚的衍射峰对应于立方晶型Cu2O的特征峰(JCPDS-65-3288)。以上结果可以表明,在−1.4 V电位下Cu2O与单质铜同时生成。图1(B)中2θ = 25.3˚和48.1˚处的峰对应于锐钛矿TiO2 (JCPDS-21-1272)的特征衍射峰,而其余较强的峰则为钛基底的特征衍射峰;图1(A)中同样保留了TiO2和钛基底的衍射峰,该结果表明Cu与Cu2O纳米粒子已成功地组装到TiO2纳米管上。
图2为TNTs与CCT电极的SEM图。其中TiO2纳米管的直径约为110 nm (图2(A))。而CCT电极表面有许多Cu与Cu2O簇状颗粒,粒径大小约为200 nm (图2(B))。仔细观察可以发现,颗粒基本覆盖在TNTS纳米管口处,也有少部分填充在管内。
3.2. 葡萄糖、果糖、蔗糖在CCT电极上的电催化氧化
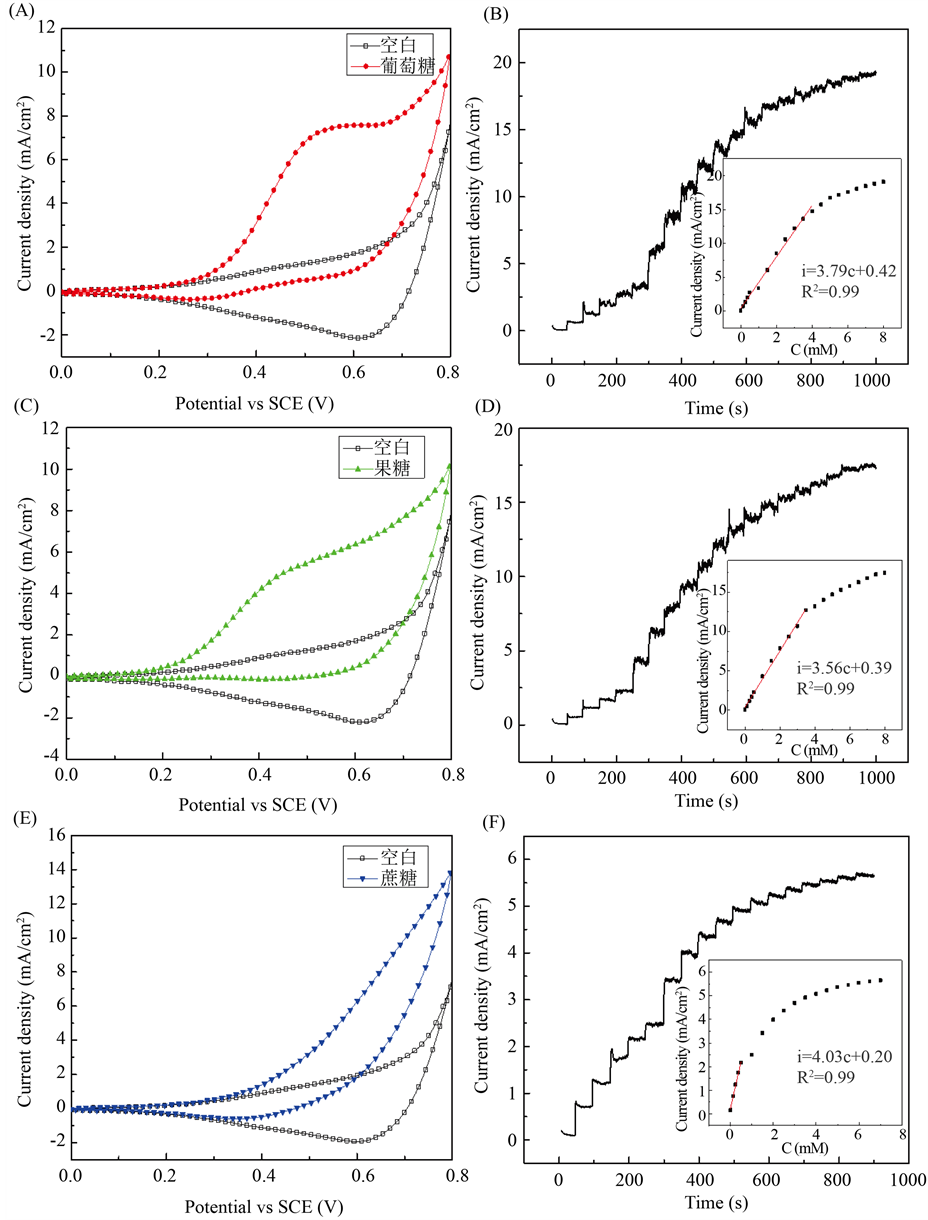
图3为葡萄糖、果糖和蔗糖在CCT电极上的CV曲线与计时电流曲线图。由图3(A)可知,当加入

Figure 1. XRD patterns of CCT (A) and TNTS (B)
图1. CCT电极(A)与TNTS(B)的XRD图

Figure 2. SEM images of TNTS (A) and CCT (B)
图2. TNTS电极(A)与CCT (B)的SEM图
2.0 mM葡萄糖溶液后,电流密度明显增大。而葡萄糖在CCT电极上的氧化峰则从0.3 V开始至0.65 V结束,最佳氧化峰的电位为0.55 V。通过将CCT电极与Cu/石墨烯电极在相同实验条件下进行对比可以发现 [8] ,其氧化峰电位高于Cu/石墨烯电极0.45 V的响应值,且此处氧化峰处对应的电流密度可达7 mA以上,也高于文献报道中0.5 mA的电流密度值。以上结果表明此电极对葡萄糖有着较好的催化氧化性能。图3(B)为葡萄糖在0.55 V的工作电位下的计时电流曲线与拟合曲线。可以看到,CCT电极对葡萄糖的响应可在3 s内达到稳定。其线性响应范围可达4 mM (R2 = 0.99),而灵敏度则为3790 µA cm−2 mM−1,检测限(LOD)为17 µM (S/N = 3)。但是在更高浓度葡萄糖溶液条件下,电流响应逐渐趋于平缓,这是由于高浓度的葡萄糖吸附在电极表面而不利于电子在葡萄糖和电极之间的传递,导致电极表面钝化所致。同样,根据图3(C)果糖的循环伏安曲线可知,果糖在CCT电极上的氧化峰范围为0.25~0.7 V,其最佳氧化峰处的电位为0.50 V,比葡萄糖的最佳氧化峰处的电位略低。图3(D)为果糖在0.5 V工作电压下的计时电流曲线与拟合曲线。其线性响应可达3.5 mM (R2 = 0.99),灵敏度为3560 µA cm−2 mM−1。此外可以得到此电极对果糖的检测限(LOD)为1.3 µM,低于葡萄糖的检测限的17 µM (s/N = 3),该结果说明此电极对果糖响应比葡萄糖更好。
 Note: glucose concentration 2.0 mM, NaOH concentration 0.1 M, scan rate 0.05 V s-1
Note: glucose concentration 2.0 mM, NaOH concentration 0.1 M, scan rate 0.05 V s-1
Figure 3. The CV and Amperometric curves of glucose, fructose and sucrose over CCT electrode (the insets are the corresponding calibration curves)
图3. 葡萄糖、果糖和蔗糖在CCT电极上的CV曲线与计时电流曲线(内插图为对应的拟合滴定曲线)
从蔗糖的循环伏安曲线图3(E)可知,加入蔗糖后,CV曲线电流明显增大,但是没有明显氧化峰。这是由于蔗糖是双糖,因而不易被氧化所致。由该图可知,蔗糖在CCT电极上的氧化峰范围为0.5~0.7 V。为了避免高电压可能对实验产生干扰,我们选取工作电位为0.55 V进行计时电流曲线的测试。由计时电流曲线与拟合曲线图3(F)可知,蔗糖的线性响应范围较窄,只有0.6 mM (R2 = 0.99),灵敏度为4030 µA cm−2 mM−1,检测限(LOD)为12 µM。
3.3. 葡萄糖与果糖混合溶液在CCT电极上的催化氧化
图4为不同溶液在CCT电极上的循环伏安曲线对比图。通过比较葡萄糖、果糖和蔗糖在CCT电极上的电催化性能可以发现,葡萄糖的催化氧化电流最高,果糖的氧化电位最低,而蔗糖的催化氧化性能最差。而从葡萄糖与果糖混合溶液的循环伏安曲线图4(e)可知,混合溶液的催化氧化电流最高,氧化电位比葡萄糖的低,而比果糖的高。另外,曲线中只出现了一个宽的氧化平台,因而无法区分混合物中葡萄糖和果糖的氧化峰,该结果说明CCT电极对葡萄糖与果糖混合溶液的催化氧化没有单一选择性。值得注意的是,混合溶液的最大氧化电流密度达到了8 mA cm−2,比Pt/Ru/C电极对葡萄糖和果糖燃料电池 [2] 的最大氧化电流密度的2.67 mA cm−2高出了2倍左右,表明该电极对这两种糖有较好的电催化氧化性能。
3.4. 碱性条件下三种糖在CCT电极上的催化氧化机理
根据以上CV结果,可以发现CCT电极对葡萄糖、果糖和蔗糖在0.25~0.7 V范围内有不同程度的氧化峰,表明糖类在较低电位下就能发生氧化反应。另外,观察到CCT电极对三种糖类响应程度有所不同。其中果糖和葡萄糖的响应电流比较接近,都明显高于蔗糖的响应电流,表明蔗糖在该电极上的氧化机制与葡萄糖/果糖不同。根据文献报道,当电位为0.8 V时,铜离子在碱性条件中可形成Cu3+,该离子可以一定程度地断裂糖类中的C-C链 [12] [14] [15] ,从而实现对糖类的氧化。更重要的是,葡萄糖和果糖等还原糖在碱性条件下可实现一定程度的烯醇式转换 [16] ,其反应如图5(I)所示(S表示葡萄糖和果糖)。烯醇式结构的出现有利于其被氧化,故CCT电极对葡萄糖和果糖的催化氧化机制如图5(II, III)所示 [17] 。
而蔗糖虽然由一分子果糖和一分子葡萄糖缩合而成,但是在碱性条件下无法水解,仅仅以蔗糖分子
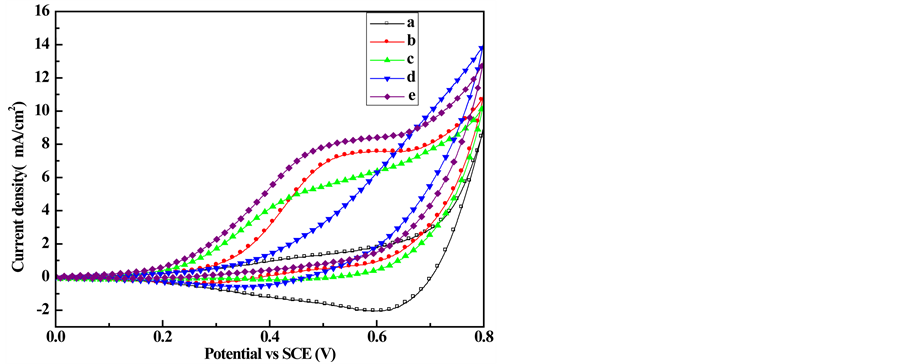
Figure 4. The CVs of CCT electrode in different solutions. (a) Blank, (b) 2.0 mM of glucose solution; (c) 2.0 mM of fructose solution; (d) 2.0 mM of sucrose solution and (e) The mixed solution composed of 1 mM of glucose and 1 mM of fructose solution (volume ratio: 1:1)
图4. 不同溶液在CCT电极上的循环伏安曲线对比图。(a) 空白;(b) 2.0 mM葡萄糖;(c) 2.0 mM果糖;(d) 2.0 mM蔗糖;(e) 1 mM葡萄糖与果糖1:1混合液
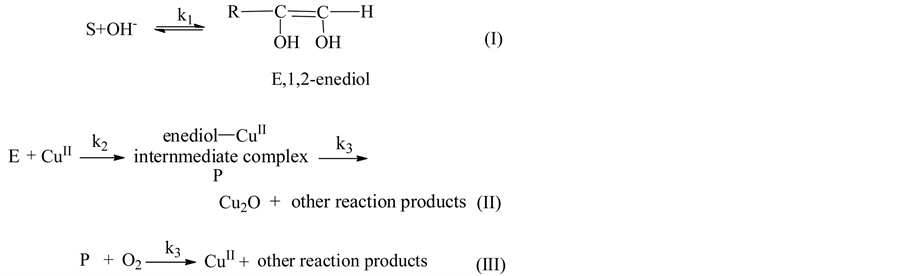
Figure 5. The reaction mechanism of glucose and fructose at CCT electrode [17]
图5. 葡萄糖和果糖在CCT电极上的反应方程式 [17]
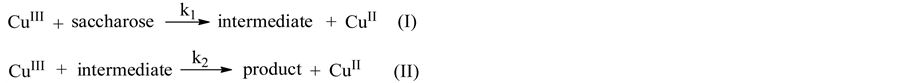
Figure 6. The reaction mechanism of sucrose at CCT electrode [8]
图6. 蔗糖在CCT电极上的反应方程式 [8]
形式存在 [18] 。因而蔗糖只能被Cu3+离子氧化 [8] ,其反应机制如图6(I, II)所示。相对来说,葡萄糖和果糖容易被氧化,而蔗糖难于被氧化,故该电极对葡萄糖和果糖的响应电流相近,均高于对蔗糖的响应电流。
4. 结论
1) 本实验采用二次阳极氧化法制备二氧化钛纳米管,并以二氧化钛纳米管作为基底,采用电沉积法,成功地在其上面组装Cu/Cu2O纳米颗粒。2) 采用此电极在0.1 M NaOH溶液条件下,对葡萄糖、果糖、蔗糖进行电催化测试。结果表明,该电极对葡萄糖的催化氧化电流最高,而对果糖的氧化电位最低,对蔗糖的催化氧化性能最低。3) 该电极在碱性条件下对三种糖类及其混合溶液均表现出一定的氧化性能,其催化电流密度均高于5 mA cm−2。此类电极未来有望作为阳极材料用于生物燃料电池。
基金项目
国家自然科学基金资助项目(No. 51374250);湖南省自然科学创新研究群体基金(湘基金委[2014]-2号)。