1. 燃料电池工作原理
车载质子燃料电池的关键结构主要包括阴极/阳极板,气体流道,冷却液流道,阴/阳极扩散层,催化层和质子交换膜,如图1所示 [1] 。在燃料电池工作过程中,具有一定压力的反应气体进入阴极/阳极气体通道中,并通过多孔介质扩散层到达相应的催化层发生电离生成氢离子质子和电子,由于电渗透迁移作用,在阴极在发生氧化反应的同时,伴有液滴的形成。另外,电子会经过外电路向阴极侧流动形成电流,在阴极催化层,氧气和来自阳极电离的氢离子及以外电路迁移来的电子发生化学反应 [2] 。在阴极/阳极的集流板中布有响应的冷却液流道 [3] [4] 。反应如下式:
阳极: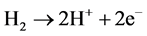
阴极:
电池总反应:
2. 控制方程
2.1. 热力学控制方程
2.1.1. 连续方程
假设流体为连续介质和低速流条件下,连续方程为:
 (1)
(1)
式中左边第一项为非稳态相,左边第二项为对流相,右边项为质量源项 [5] [6] 。其中: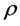 为密度,
为密度, 代表孔隙率,
代表孔隙率, 为速度矢量,
为速度矢量,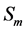 代表质量源项。计算域的不同,也会引起质量源项表达式的差异。对于阴极和阳极的流道与扩散层,质量源项为0;对于参与化学反应的阴极和阳极催化层 [7] ,质量源项即表示如下:
代表质量源项。计算域的不同,也会引起质量源项表达式的差异。对于阴极和阳极的流道与扩散层,质量源项为0;对于参与化学反应的阴极和阳极催化层 [7] ,质量源项即表示如下:
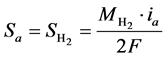 (2)
(2)
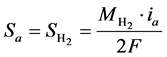 (3)
(3)

Figure 1. Working principle of fuel cell
图1. 燃料电池工作原理图
式中, 代表不同组分的摩尔质量,下角标a,c分别为阳极和阴极,
代表不同组分的摩尔质量,下角标a,c分别为阳极和阴极,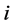 为电流密度,
为电流密度,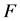 为法拉第常数。根据法拉第定理推出电流与反应气体消耗的关系,即:
为法拉第常数。根据法拉第定理推出电流与反应气体消耗的关系,即:
 (4)
(4)
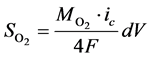 (5)
(5)
 (6)
(6)
式中rw是考虑水冷凝时的凝结率,其负数表示水蒸发率。
 (7)
(7)
2.1.2. 动量守恒方程
水是不可压缩流体,考虑了切应力和正应力的影响,采用了N-S粘性定律推导其动量方程,表达式如下:
 (8)
(8)
式中,等号左边的第一项为非稳态项,第二项为对流项,等号右边前两项为扩散项,右边最后一项代表动量源项其中:P为流体的压力,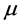 是流体的有效粘性系数,
是流体的有效粘性系数, 代表动量方程的动量源项,U代表动量方程中的速度场。在扩散层和催化层的多孔电极中,流速慢梯度较小,因此不考虑流体粘性力和惯性力的影响,上述动量源项方程可简化成下式:
代表动量方程的动量源项,U代表动量方程中的速度场。在扩散层和催化层的多孔电极中,流速慢梯度较小,因此不考虑流体粘性力和惯性力的影响,上述动量源项方程可简化成下式:
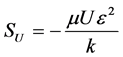 (9)
(9)
k为扩孔介质的气相渗透率,表示了在多孔介质中,流体气相对固体表面所施加的曳力的大小。
2.1.3. 能量守恒方程
对于燃料电池而言,认为集流板中不存在气体传质,热量的传递只考虑导热,在反应气体通道中,存在了反应气体的传热传质过程,而在多孔电极中,其热量的传递更为复杂。在多孔介质的热量传递过程中,不考虑粘性耗散相产生的热量,对流体和固体中的微观能量分别进行加权平均 [8] ,然后将其相加集总,即可获得催化层,膜,扩散层等多孔介质中的能量方程。计算域相应的温度场分布的能量守恒方程计算如下:
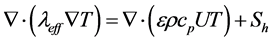 (10)
(10)
 代表能量守恒方程中的热源项,该热源项包括电化学反应产生的焓变净值
代表能量守恒方程中的热源项,该热源项包括电化学反应产生的焓变净值 ,包括由于阴阳极过电势和电流传递产生的化学反应热
,包括由于阴阳极过电势和电流传递产生的化学反应热 ,包括接触电阻产生的欧姆热
,包括接触电阻产生的欧姆热 ,也包括水分冷凝和蒸发的相变潜热。热源的表达式如下:
,也包括水分冷凝和蒸发的相变潜热。热源的表达式如下:
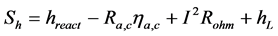 (11)
(11)
其中: 为有效导热系数,
为有效导热系数, 代表电流密度,
代表电流密度,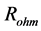 为电阻率,
为电阻率,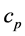 为等压比热
为等压比热
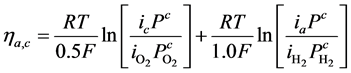 (12)
(12)
2.1.4. 组分守恒方程
由于速度场U的存在,各个化学组分的流量包括对流流量和扩散流量两部分,对于参与化学反应的氢气,氧气和水分的化学组分,其通用的传递方程如下所示:
 (13)
(13)
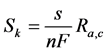 (14)
(14)
式中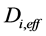 是气体混合物中组分i的多孔介质中的有效扩散系数,s是阴极阳极反应的化学计量系数,n为组分k反应的得失电子数。式中:等式右边第一项为扩散流量,由Fick定律表述。Y为组分i的质量分数,
是气体混合物中组分i的多孔介质中的有效扩散系数,s是阴极阳极反应的化学计量系数,n为组分k反应的得失电子数。式中:等式右边第一项为扩散流量,由Fick定律表述。Y为组分i的质量分数, 为化学组分在催化层中发生电化学反应的组分源项 [9] 。氢气,氧气和水分的源项可表示为如下:
为化学组分在催化层中发生电化学反应的组分源项 [9] 。氢气,氧气和水分的源项可表示为如下:
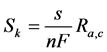 (15)
(15)
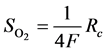 (16)
(16)
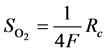 (17)
(17)
2.2. 电化学控制方程
化学模型的建立是针对的是阳极氢气氧化速率和阴极氧气还原速率对电化学反应的影响作用。主要包括以下几类方程,Butler-Volmer方程,电流守恒方程,开路电压控制方程,活化极化控制方程,欧姆过电位和浓差过电位控制方程,以及反应物的消耗和液滴生成方程 [10] 。
2.2.1. 电流守恒方程
质子交换膜燃料电池人为的定义为固体项电势和膜电势 [11] 。
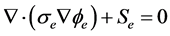 (18)
(18)
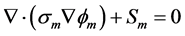 (19)
(19)
式中,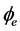 和
和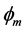 分别代表固相电势和膜相电势;
分别代表固相电势和膜相电势;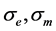 分别代表固相和膜相的电势,
分别代表固相和膜相的电势, 和
和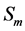 分别代表电子电流源项和质子电流源项即交换电流密度(A/m³),电子和质子只存在于催化层的电化学反应区,即只有催化层的内部才不为零,且他们满足一下关系:
分别代表电子电流源项和质子电流源项即交换电流密度(A/m³),电子和质子只存在于催化层的电化学反应区,即只有催化层的内部才不为零,且他们满足一下关系:
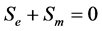 (20)
(20)
在阳极:
 (21)
(21)
 (22)
(22)
在阴极:
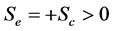 (23)
(23)
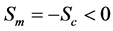 (24)
(24)
电极电势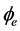 和
和 与过电势之间存在着以下的关系:
与过电势之间存在着以下的关系:
 (25)
(25)
在阳极,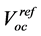 值为零,也就是说阳极要接地,在阴极
值为零,也就是说阳极要接地,在阴极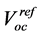 值即使开路电压。
值即使开路电压。
2.2.2. Butler-Volmer方程
Bulter-Volmer方程是在基于考虑反应气体浓度,温度,极化对电化学反应的影响基础上,计算催化层中电流的传递,即和这两个代表阴阳极交换电流密度的源项,其定义式如下:
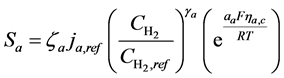 (26)
(26)
 (27)
(27)
式中,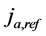 和
和 分别代表阳极和阴极的参考体积交换电流密度,
分别代表阳极和阴极的参考体积交换电流密度,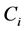 代表不同组分的摩尔浓度,
代表不同组分的摩尔浓度, 代表不同组分的参考摩尔浓度,
代表不同组分的参考摩尔浓度, 是无量纲浓度指数,对于阳极取值0.5,对于阴极为无量纲的传递系数。
是无量纲浓度指数,对于阳极取值0.5,对于阴极为无量纲的传递系数。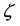 是活性比面积。F是法拉第常数。
是活性比面积。F是法拉第常数。
2.3. 动力学控制方程
在可逆电池的情况下,整个电池处于电化学平衡状态,两个电极电位也分别处于平衡状态的电极电位 [11] 。但是,在实际电池中,电子经过膜与电解液接触的时候,会形成电偶层,发生电位跳跃,产生了电压损耗,使得电极电位偏离平衡电位,即发生了电极极化 [12] 。实际电位偏离平衡电位程度用电位差,称为过电位。常见的电极极化包括有活化极化、浓差极化,欧姆极化等,燃料电池的过电位也由极化发生的原因不同分为,活化过电位,欧姆过电位,浓差过电位。因此,电池的工作电压和活化过电位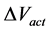 ,欧姆过电位
,欧姆过电位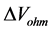 ,浓差过电位
,浓差过电位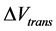 和开路电压
和开路电压 之间存在以下的关系:
之间存在以下的关系:
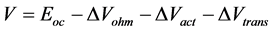 (28)
(28)
2.3.1. 开路电压方程
开路电压为电池处于断路状态即电流为零时的电压。没有电流经过时,认为电化学反应出于平衡状态,其电位即为于平衡电压,也就是能斯特电压。燃料电池的开路电压控制方程可以利用能斯特方程进行表达。
 (29)
(29)
式中: 代表吉布斯自由能的变化量,T为温度,P根据下角标不同代表不同组分的分压。
代表吉布斯自由能的变化量,T为温度,P根据下角标不同代表不同组分的分压。
但是,燃料电池反应气体氢气分子不断通过质子膜从阳极向阴极扩散,是在不断消耗的,虽然消耗量很小,但是外部电路是一个开路的状态,实际上是非平衡状态。
2.3.2. 活化过电位方程
与平衡状态电位的电压差是驱动电化学反应进行的动力源,活化过电位是由于电极表面电化学反应受到动力驱动而产生的,即燃料电池电化学反应需要克服服活化能。活化过电位方程根据塔菲尔公式表达如下:
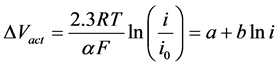 (30)
(30)
式中,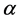 为电荷转移系数,表示改变化学反应速度所用电能的比率,取值与电极材料有关,在0~1之间。氢气电极多为0.5,氧气电极0.5~1之间。
为电荷转移系数,表示改变化学反应速度所用电能的比率,取值与电极材料有关,在0~1之间。氢气电极多为0.5,氧气电极0.5~1之间。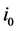 为交换电流密度,
为交换电流密度,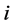 为电流密度,a是塔菲尔方程的截距,b为塔菲尔方程的斜率。
为电流密度,a是塔菲尔方程的截距,b为塔菲尔方程的斜率。
2.3.3. 欧姆过电位控制方程
燃料电池质子膜中存在对离子流的阻抗和对流过燃料电池到电元件电子流的阻抗欧姆过电位,其中电解质的离子阻抗影响更大。由于电极、集流板等电池组件的电阻以及电解质的离子电阻引起的电压降称为欧姆过电位,其值的大小可以用欧姆定律来计算:
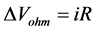 (31)
(31)
i为电池的电流密度,A/cm2,R为电池的面电阻,Ω·cm2。
2.3.4. 浓差过电位控制方程
燃料电池中,反应气体到达催化剂上发生电化学反应时,会产生气体消耗。气体消耗的过程发生在多孔介质传递的过程以及反应物和生成物在质子膜中的溶解和解析过程中。由于浓度梯度的变化,就发生由物质传递浓差产生的过电位。
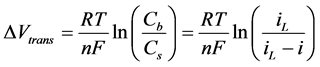 (32)
(32)
其中,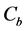 为反应物总浓度,
为反应物总浓度,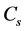 为催化剂表面的反应物浓度,
为催化剂表面的反应物浓度, 时极限电流密度,i为扩散电流密度。
时极限电流密度,i为扩散电流密度。
3. 燃料电池水热管理多物理场耦合仿真研究
Fluent的PEMFC模型将质量守恒方程,动量守恒方程,组分守恒方程,能量守恒方程,液态水形成与传输方程,电化学反应速率方程,电池电势控制方程高度集成,便于电势分布,电流密度分布,电压分布,各组分浓度分布,温度分布,含水量分布,压力场,速度场等等的求解分析 [13] [14] 。该模型通过用户自定义方法(UDF),定义了质子交换膜燃料电池的反应气体消耗和热量生成,水含量,电子/质子电势的传输与消耗等等,从而为解决燃料电池内部水热管理的复杂的部电流密度分布、温度场分布、水的传输机理等多场耦合,多相传热与传质,多尺度多工况问问题研究提供一个高效便捷手段 [15] [16] 。
3.1. 几何模型设置与边界条件定义
本文采用Fluent的PEMFC模块对燃料电池多物理场多尺度水热管理展开研究分析。计算对象为直型单流道单个燃料电池,建立了其非稳态物理模型,主要包括阴极阳极集流板,扩散层,催化层和质子膜以及冷却液流道,这九个部分,计算模型如下图:其结构和网格划分如下图2所示:主要研究在如表所示的不同工况条件下,冷却液水温变化,流量变化,冷却液流道结构变化对于燃料电池催化层,扩散层和质子膜温度场和含水量的影响。
3.2. 仿真工况参数
在模拟计算的时候,假设燃料电池在稳态状态下运行,且忽略重力的影响;反应气体为牛顿流体不可压缩,液滴水是细小的雾状,当成气体处理,流道内的气体流动是层流 [17] 。本文针对燃料电池多物理场多尺度水热管理,采用Fluent的PEMFC模块进行计算,仿真工况设置如下表1。
3.3. 燃料电池水热管理多场耦合仿真结果分析
质子交换膜是质子交换膜燃料电池中的关键部件之一,它稳定正常工作需要有足够的水份,使其处于润湿状态,另外如果温度过高也会影响膜的寿命 [18] [19] [20] 。因此本文针对燃料电池阴极工作压力和冷却液进口温度变化对质子膜含水量和温度的影响进行了分析如下。
由图3可知:冷却液进口温度一定时,随着阴极压力的增加,质子膜含水量增加,阴极压力为0.3 V时,进深10 cm处的质子膜含水量为1.46,0.5 V时质子膜的含水量为1.49,0.7 V时为质子膜含水量为1.55。这说明高压对于燃料电池工作更有利,阴极压力的增加,增大了电位,一方面利于质子膜内的电化学迁移 [21] ,另一方面压差变大气体扩散率和液体渗透率也随之增加,利于水分和气体迁移。但随着进深的增加,质子膜含水量是在降低的,说明随着进深的增加,质子膜存在脱水现象,脱水程度随着

Table 1. Simulation conditions and parameters
表1. 仿真工况与参数表

Figure 3. Effect of cathode pressure on water content
图3. 阴极压力对含水量影响
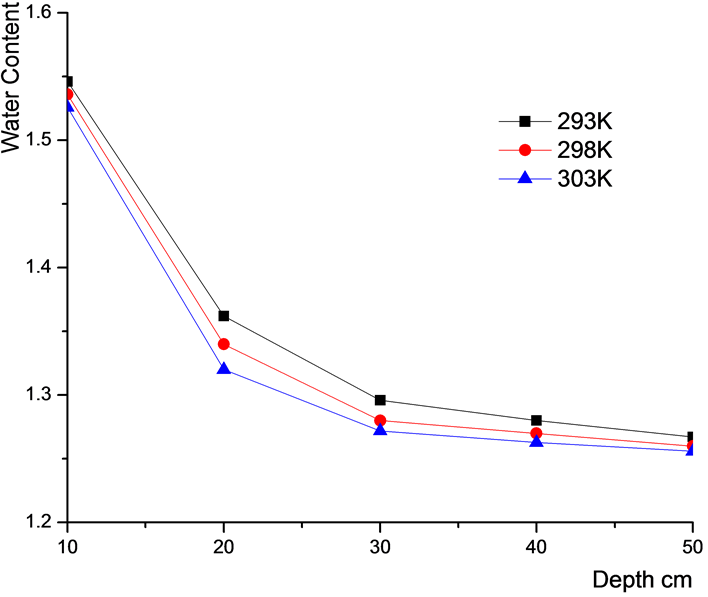
Figure 4. Effect of inlet temperature on water content
图4. 冷却液进口温度对含水量影响
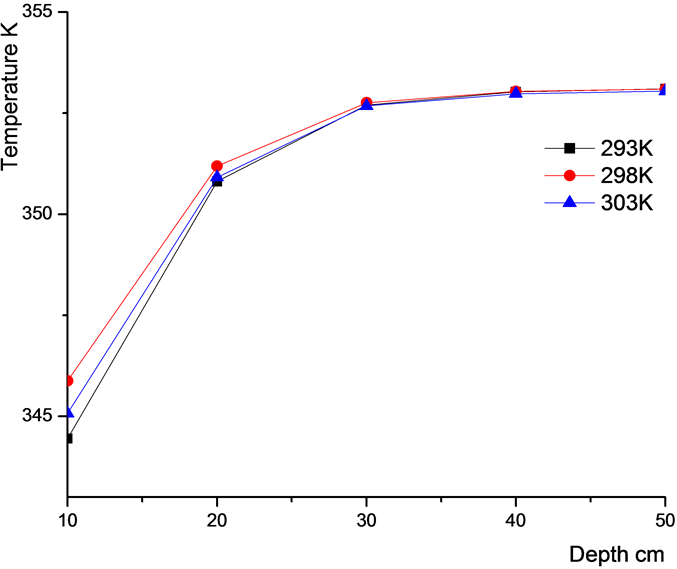
Figure 5. Effect of inlet temperature on water content
图5. 冷却液进口温度对含水量影响
压强的增加呈现出增加的趋势,阴极进气压力为0.3 V时,进深10 cm和50 cm两处含水量差为0.25,0.5 V时含水量的差为0.27,0.7 V时含水量差为0.277。
由图4可知:当阴极气体压力一定时,随着冷却液进口温度的增加,质子膜含水量减少;在20 cm处,冷却液进口温度为293 K时含水量为1.32,冷却液进口温度为303 K时,质子膜此处含水量为1.28,当冷却液进口温度提高到303 K时,此处的质子膜含水量为 1.25,说明随着冷却液进口温度降低,燃料电池的外表面散热改善。
由图5可知,当进气压力一定时,随着冷却液进口温度降低,质子膜工作温度降低,2冷却液进口温度为293 K时,在质子膜20 cm处温度为350.807,冷却液进口温度为298 K时,此处的温度为351.188 K,当冷却液进口温度为303 K时,20 cm处质子膜温度为350.913 K。随着冷却液温度降低,质子膜温度呈现降低趋势,但是随着进深的增加,质子膜温度上升。在质子膜进深达到40 cm后,质子膜温度基本维持在353.03 K处在高温区。
4. 结论
车载燃料电池水热管理不仅涉及温度的优化控制,更是综合考虑热场,化学场,电场,流场,压力场,组分运输等多尺度,多物理,多过程的场流固耦合的多形态,多相,多工况下传热传质的动态的集成优化与协同控制。车载燃料电池的水热管理即对水–气体–质子三相界面上发生的水分生成与传输和热量传递等的空间分布和时间分布优化设计与研究分析,以寻求保持燃料电池水热平衡并提高电池性能和寿命的关键技术。
基金项目
国家自然科学基金(51376079);吉林省科技发展计划重大项目(20130204018GX)。