1. 引言
水中磷的存在是生物体生长不可缺少的主要元素之一,但也是植物生长的限制因素之一 [1] ,当水中磷含量过高,会引起水体富营养化问题。现有常用的将废水中磷去除的方法主要有离子交换法 [2] 、生物法 [3] 、化学沉淀法 [4] 和吸附法 [5] 等。其中,化学沉淀法投加药剂形成的沉淀物需要通过固液分离从污水中分离;生物法通过好氧–厌氧的交替运行来实现除磷,但对于生物的控制要求较高;而吸附法通过表面的物理吸附或者离子交换等方式,实现磷从废水中分离,操作简单,效率高。因此,如何选择高效低价的吸附剂成为了吸附法的重点研究方向。
对于吸附材料的选择,高岭土、膨润土以及生物炭等都能完成对磷的吸附。近几年,制备出低成本、高效的吸附材料成为了除磷吸附剂研究的重点方向。任琪琪等人通过镧对膨润土进行改性,使得改性膨润土对于磷的最大吸附量达到10.4 mg P/g [6] 。付瑜玲等人通过对磷酸盐高效吸附的镁铝水滑石进行改性,进一步提升其吸附性能,改性水滑石表现出较好的磷吸附能力,磷酸盐去除率达到了94.4% [7] 。但是对于污水中的磷的处理,不仅仅涉及成本,更涉及处理效率。而对于高岭土和膨润土等无机黏土矿物,虽然便宜易得,但不能有效吸附磷。国内,中国科技大学江宏课题组将废弃生物质浸泡海水并经过煅烧,形成负载氧化镁和氧化钙的生物炭,可以吸收空气中的二氧化碳。国外类似的研究还没有报道。据我们所知,目前采用低成本的材料通过浸泡和煅烧获得海水中的钙镁资源的研究还鲜有报道,因此本项目拟采用无机粘土矿物和废弃生物质获取海水中钙镁资源,并通过煅烧形成负载氧化钙和氧化镁的高效吸附剂。
2. 实验部分
(1) 改性膨润土除磷吸附剂的制备
采用Na离子型膨润土(20.0 g)与1000 ml过滤后的海水混合,在室温下剧烈磁力搅拌3 h。然后不断地过滤和洗涤,直到通过硝酸银检测不产生白色沉淀为止,即滤液中已经不存在氯离子。得到固体即为含有Mg2+和Ca2+的膨润土。用烘箱进行干燥,温度恒定120℃。将烘干的样本在空气中进行煅烧,温度恒定600℃煅烧1 h。负载有MgO和CaO的膨润土吸附剂被称为BS600。作为对比,膨润土不经过海水浸渍而直接在600℃以下的空气中煅烧1 h,得到的吸附剂被命名为B600。膨润土分别浸渍同浓度的氯化钙或者氯化镁溶液后,其余步骤与制备BS600的一样,最后得到的吸附剂被命名为BCa600和BMg600。
(2) 实验涉及的主要设备
实验设备如表1所示。
(3) 模拟溶液中磷酸盐的吸附实验
在500 mL锥形瓶的锥形瓶中,重复进行三次的吸附实验。将吸附样品分散到磷溶液中,并通过恒温摇床震荡1天。在pH为7.5 ± 0.3的磷酸盐溶液中进行等温吸附实验,将初始的磷酸盐浓度调整为0.1~60 mg P/L之间。在等温吸附实验结束之后,采集上清液,通过光谱仪测定吸附平衡后的磷酸盐浓度。将剩余的固体进行表征分析。样品表面吸附磷酸盐的量(qe, mg P/g)和去除效率按下式计算:
(1)
(2)
其中,V (L)为溶液的体积,m (g)为样品质量,C0和Cf (mg P/L)分别为初始浓度和平衡浓度。
(4) 实际河水中总磷的吸附实验
在实际河水总磷吸附的实验中,首先对于实际的河水样本进行过滤,去除杂质后,标定pH、温度及总磷浓度等。实验中将吸附样品分散在100 mL的水样中,磁吸搅拌1 h。吸附实验完成后,采集样本上清液,采用分光光度法测量吸附平衡后的总磷浓度。
3. 改性膨润土吸附剂的结果与讨论
(1) XRD分析
尽管海水中的钠离子浓度远远大于钙镁离子浓度,但从热力学角度考虑,钙镁离子的插层作用比碱金属离子更能有效地中和并稳定层长硅酸盐片的永久电荷,因此会发生离子交换。为了证明样品的成功制备,图1是样品的d 001衍射峰。与B600 (2θ = 9.24˚)相比,BS600经过修饰后的d 001衍射峰从2θ = 9.24˚转移到2θ = 8.98˚。对应的层间距是从9.56 Å增加到9.84 Å。从图1中还可以得到BCa600和BMg600的层间距分别为9.84 Å和9.70 Å。因此,可以推断膨润土通过海水浸渍后,层间的钠离子主要是被海水中的钙离子通过离子交换后取代。由于钙离子的离子半径比钠离子的离子半径要大,导致取代后的层间距增大。在图2中也可以看到,在2θ = 32.20˚、37.35°和53.85˚都是CaO的衍射峰。因而,从XRD分析可知,BS600吸附剂负载有CaO。
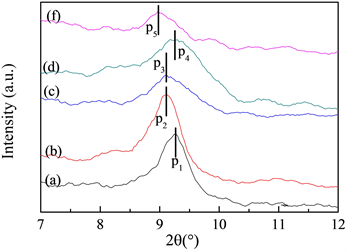
Figure 1. The d 001 diffraction pattern of the sample (a: B600, b: BS600, c: BCa600, d: BMg600, f: BS600 after phosphorus adsorption)
图1. 样品的d 001衍射图(a: B600, b: BS600, c: BCa600, d: BMg600, f:吸附磷后的BS600)
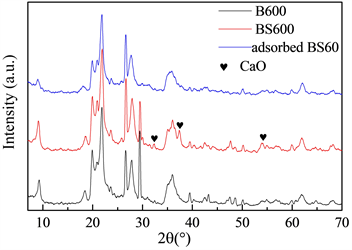
Figure 2. XRD pattern of B600, BS600 and BS600 after phosphorus adsorption
图2. B600、BS600和吸附磷后的BS600的XRD图
(2) BET和SEM分析
如图3所示,B600和BS600都属于介孔材料。B600和BS600的比表面积分别为37.34 m2/g和27.80 m2/g。与B600相比,BS600的比表面积大约减少了25%,主要是由于CaO/MgO颗粒的形成堵塞了膨润土的孔隙,从而大大降低了BS600的比表面积。图4是B600和BS600的SEM图和BS600的EDX图。由图可见,BS600表面出现细小的氧化钙颗粒(黑色箭头,图4(b))。另外的EDX分析结果(图4(c))表明,BS600的表面含有Ca、Mg、K和Cl,这些物质显然是从使用过的海水中获得的,这再次证实了改性的成功,并证明了获取海水资源制备功能材料是可行的。由EDX结果可知,BS600中CaO和MgO的含量分别为7 wt%和2 wt%。
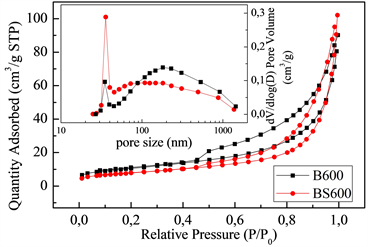
Figure 3. N2 adsorption and desorption isotherms and pore-size distribution (inset) for B600 and BS600
图3. B600和BS600的N2吸脱附曲线和孔径分布图
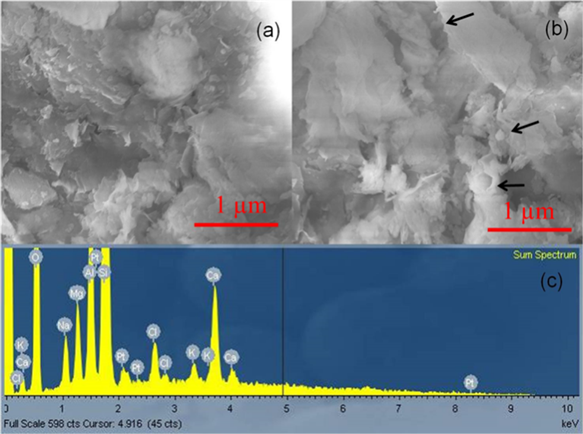
Figure 4. SEM patterns of B600 (a) and BS600 (b) and EDX pattern of BS600 (c)
图4. B600 (a)和BS600 (b)的SEM图及BS600的EDX图(c)
(3) 表面电荷特性分析
图5是溶液pHi-pHf间的关系曲线。可见,随着起始pHi的增加,滴定溶液pHf的变化逐渐趋于平缓。B600和BS600电荷零点所对应的pHzpc分别pH = 9.4 ± 0.1和7.2 ± 0.1。经过CaO/MgO负载后降低了BS600表面的酸度。因而,与B600相比,BS600的表面与磷酸盐之间的静电斥力减弱,这可能是BS600即使在碱性环境下也能大量吸收磷酸盐的原因。零电荷点的增加进一步说明BS600表面的碱度增加,吸附位点较多,有利于磷酸盐吸附。
(4) pH的影响和吸附量分析
图6(a)是pH值对吸附磷的影响。在pH = 2~11之间,B600对磷酸盐的吸附量非常有限(<5%)。这是由于磷酸盐和带负电荷的膨润土表面之间的静电斥力导致的。对于BS600吸附剂,当pH值为 > 4时,BS600对磷酸盐的吸附量大大增加,达到80%左右。即使在碱性环境中,BS600对磷酸盐的吸附量也较高(>80%),这意味着,在这种情况下,可能是由于钙磷酸构型的形成,而不是静电相互作用,CaO和磷酸盐之间的高亲和力导致了较多磷酸盐被吸附。图6(b)在pH = 7.5 ± 0.3时,B600和BS600对磷酸盐的吸附性能图。通过Langmuir模拟计算得到B600和BS600对磷酸盐的最大吸附量为0.1和11.45 mg P/g (表2)。根据Langmuir方程(3)计算获得B600和BS600对水中磷酸盐的最大吸附量。

Figure 5. The relationship of pHi-pHf
图5. pHi-pHf间的关系图
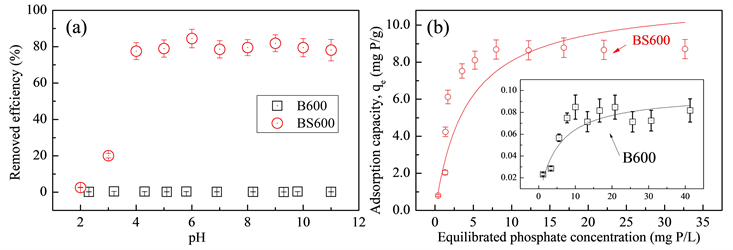
Figure 6. Effect of pH on phosphate removal (a) and adsorption properties of B600 and BS600 for phosphate in water (b)
图6. pH对吸附磷的影响(a)和B600和BS600对水中磷酸盐的吸附性能(b)

Table 2. Model parameters for Langmuir
表2. Langmuir模型参数
(3)
其中,Ce:磷溶液的初始浓度(mg/L);qe和qm分别是吸附量和最大吸附量(mg/g);KL:Langmuir吸附平衡常数(L/mg)。
(5) 实际河水水样中总磷的吸附
如图7所示,通过调节BS600投加量,分析吸附剂的投加量对于投加效率的影响,投加剂量1~8 g/L。通过图7可以看出,随着投加量的增加,去除率快速增大,主要的原因是由于投加吸附剂越多,则活跃的吸附点位越多,吸附点位的增加可以有效的去除水中的总磷。从图中可以看出,当吸附剂的投加量大于4 mg/L时,样品对于水中总磷的吸附量已经超过95%,达到了本次研究的技术指标。并且对于剩余的上清液进行分析,可以发现,吸附后,总磷的残留量可以满足国家二级地表水环境质量标准(≤ 0.1 mg/L)的总磷浓度的要求。所以,BS600具有从实际河水中有效去除总磷的能力。
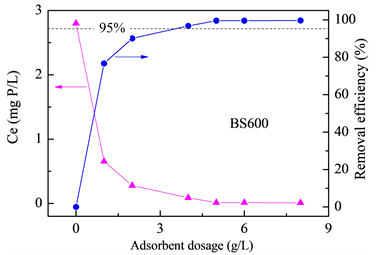
Figure 7. Effect of BS600 dosage on removal of total phosphorus in river water
图7. BS600吸附剂投加量对河水中总磷的去除率影响
4. 结论
通过上述研究可以发现,BS600对于水中磷酸盐有着显著的吸附效果。并且溶液的pH值对于水中磷酸盐的吸附有影响。当pH值大于4的时候,样品对于水中磷酸盐的去除率达到80%。通过Langmuir模型进行等温吸附研究后发现,BS600样品对于水中的磷酸盐的最大吸附量为11.45 mg P/g。当样品的投加量大于4 mg/L时,样品对于水中的磷酸盐吸附效率大于95%,且通过对于吸附后的水样进行分析,发现吸附后总磷残留满足国家二级地表水环境质量标准(≤ 0.1 mg/L)的总磷浓度的要求。因此,BS600具有从实际河水中有效去除总磷的能力。