1. 引言
阿尔茨海默病(Alzheimer’s disease, AD)是一种慢性进行性神经退行性疾病,是最常见的老年痴呆类型 [1]。AD的发病机制目前尚未完全阐明。
随着先进的全基因组和转录组等测序技术的发展,越来越清楚的是,人类基因组的80%被转录为非编码RNA (ncRNAs),在细胞中行使必要的功能 [2]。ncRNA是一个庞大而多样的非蛋白编码转录物家族,通过许多不同的机制控制基因表达程序来调节细胞功能。实验证明与AD相关的ncRNA包括circular RNA (circRNA)、long non-coding RNA (lncRNA)、microRNA (miRNA)等。
竞争性内源RNA (competing endogenous, ceRNA)是一种能够竞争结合RNA的作用元件,通常lncRNA和circRNA会竞争结合miRNA。ceRNA调控网络中包括四种RNA,即mRNA、miRNA、circRNA和lncRNA,其中miRNA处于调控的核心地位。
MiRNA是一类单链RNA分子,研究表明,miRNA与突触功能和记忆形成过程中的特定信号密切相关 [3] [4]。miRNA作为一个转录后调控的重要因子,其活性可被lncRNA通过“海绵”吸附的方式调控。lncRNA已被证实参与AD疾病中β淀粉酶的生成、突触损伤、神经营养因子的丢失、炎症、线粒体功能障碍、氧化应激等多种过程 [5] [6] [7]。
circRNA可以通过吸附miRNA、与mRNA结合蛋白相互作用或调节转录来调控基因的表达,甚至可以翻译产生多肽。最近的报告显示,circRNA在AD等神经退行性疾病的发展中起着重要作用 [8]。
越来越多的研究发现ncRNAs与AD发病机制有关 [9],尽管如此,与AD相关的ceRNA调控网络研究较少见,本文对ceRNA调控网络与AD发病机制的关系进行系统的挖掘,深入探讨ceRNA调控网络与AD疾病发病机制的潜在关系,为临床治疗提供基础。
2. 材料与方法
2.1. 材料
通过美国国立生物技术信息中心(NCBI)平台的基因表达综合数据库GEO (Gene Expression Omnibus),在人类物种下以“Alzheimer’s disease”为关键词寻找相关数据芯片,分别检索有关mRNA和miRNA的原始数据。本项目下载mRNA表达谱GSE18309 (下载日期:2021/07/18)和miRNA表达谱GSE120584 (下载日期:2021/07/18)进行后续数据分析。
2.2. 差异表达分析
利用GEO数据库自带的交互式线上分析工具GEO2R对GSE18309 (3个AD样本和3个正常样本)和GSE120584 (1021个AD样本和288个正常样本)两个数据集进行分析,在miRNA和mRNA中比较出正常对照组和AD组中存在差异表达的信息,筛选出差异表达miRNA和mRNA (P值均≤0.05,其中miRNA数据集FDR也≤0.05)。
2.3. DAVID做差异表达基因的本体论功能富集分析
使用DAVID对差异表达的mRNA进行GO通路富集分析,从生物学过程(BP, Biological Process)、细胞成分(CC, Cellular Component)及分子功能(MF, Molecular Function)三个角度,对这些基因的功能进行描述,以检测潜在的生物学功能和通路,筛选标准为P ≤ 0.05。
2.4. 目标基因筛选
分析生物学过程,通过注释信息,筛选与AD发病相关的信号通路基因进行后续分析。
2.5. 目标基因ceRNA调控网络分析
选取表达量高的top 10 miRNA,使用miRWalk 3.0数据库预测10个miRNA的靶向mRNA,并对预测的靶向mRNA和通过AD发病相关通路筛选到的目标差异表达mRNA取交集,利用Cytoscape 3.8.2构建miRNA-mRNA网络关系图。利用DIANA数据库对top 10 miRNA进行预测,获得lnRNA-miRNA关系对;利用ENCORI 数据库预测top 10 miRNA的靶向circRNA,获得circRNA-miRNA关系对,然后与文献中已报道的AD相关circRNA取交集,得到的重叠circRNA作为目标circRNA。最后利用以上靶向关系,构建circRNA-miRNA-mRNA和lncRNA-miRNA-mRNA ceRNA调控网络,并探讨其与AD发病机制的关系。
3. 结果
3.1. 人类血液中差异性表达mRNA及miRNA的筛选
用GEO2R来筛选差异表达的miRNA和mRNA,得到1819个差异表达的mRNA,包括769个上调基因和1050个下调基因;742个差异表达的miRNA,包括642个上调表达miRNA和100个下调表达miRNA。
3.2. 差异表达基因的本体论功能富集分析
在DAVID软件中进行基因的本体论功能富集GO分析发现,差异表达基因中,ITGB1,SPARC,COL13A1和ITGB5等36个基因在细胞外基质(extracellular matrix organization)的生物学过程中起作用,ITGB1,RAB1A,FOXE1和WWC1等26个基因在细胞迁移(cell migration)的生物学过程中起作用,SPON1,NRP2,ITGB5和ITGB4等53个基因在细胞粘附(cell adhesion)中发挥作用。根据P值大小排序,GO分析中生物学过程富集结果前20名P值对数大小结果(见图1)。
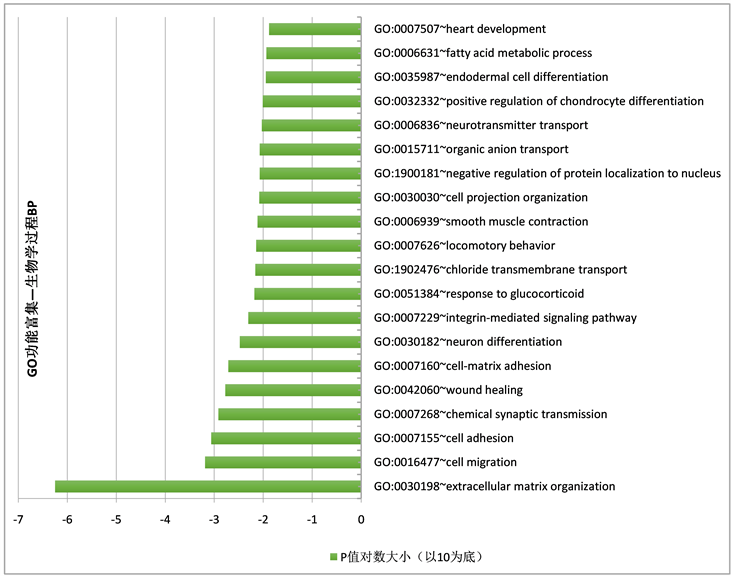
Figure 1. Functional enrichment of differentially expressed gene GO—BP results of biological process
图1. 差异表达基因GO功能富集——生物学过程BP结果
差异表达基因在细胞连接(cell junction)、基底膜(basement membrane)、蛋白质细胞外基质(proteinaceous extracellular matrix)等处发挥作用。根据P值大小排序,GO分析中细胞成分富集结果前20名P值对数大小结果(见图2)。
差异表达基因在肝素结合(heparin binding)、钙离子结合(calcium ion binding)、细胞外配体门控离子通道活性(extracellular ligand-gated ion channel activity)等分子功能中起作用。根据P值大小排序,GO分析中分子功能富集结果前20名P值对数大小结果(见图3)。
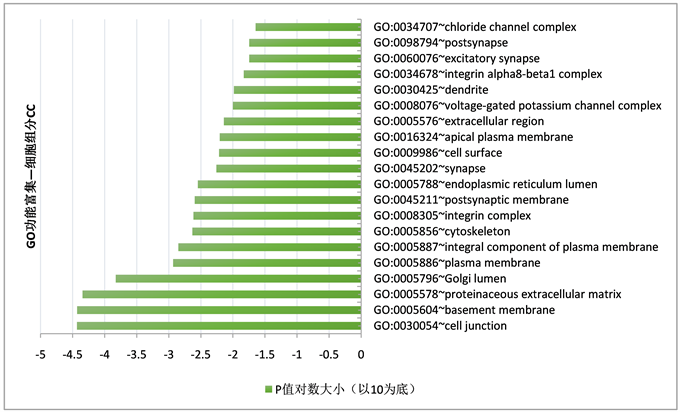
Figure 2. Functional enrichment of differentially expressed gene GO—cell component CC results
图2. 差异表达基因GO功能富集——细胞组分CC结果
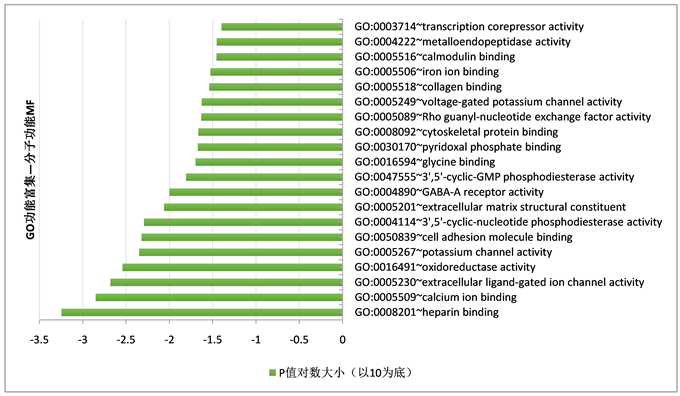
Figure 3. Functional enrichment of differentially expressed gene GO—results of molecular function MF
图3. 差异表达基因GO功能富集——分子功能MF结果
3.3. 功能分析
使用DAVID对差异表达的mRNA进行GO通路富集分析,依据生物学过程,筛选了18条与神经系统疾病相关的通路(见表1),选择这些通路所对应的基因,经过对这些通路包含的基因进行重复项等的筛选,共得到252个基因。

Table 1. 18 pathways related to AD
表1. 与AD相关的18条通路
3.4. 差异表达miRNA的靶基因预测
利用miRWalk 3.0数据库预测10个miRNA (见表2)的靶向mRNA,对预测的靶向mRNA和通路筛选到的目标差异表达mRNA取交集,得到181个重合的差异表达基因。

Table 2. 10 highly expressed miRNAs
表2. 10个高表达的miRNA
3.5. miRNA-Gene靶向调控网络的构建
利用miRWalk 3.0数据库预测10个高表达miRNA的靶向mRNA,并对预测的靶向mRNA和通路筛选到的目标差异表达mRNA取交集,得到相对应的miRNA-mRNA关系对,选取有特定对应关系的miRNA和mRNA (上调miRNA对应下调的mRNA,下调miRNA对应上调的mRNA),使用Cytoscape 3.8.2构建miRNA-mRNA靶向调控网络,如下(见图4),并可以借此图讨论其生物学意义。
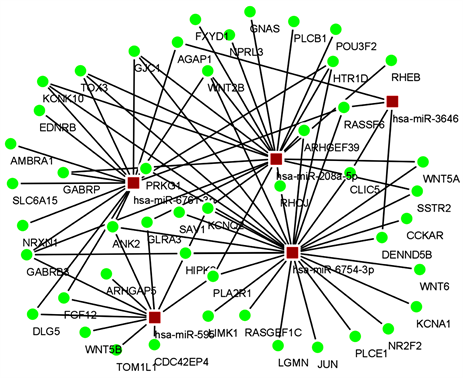
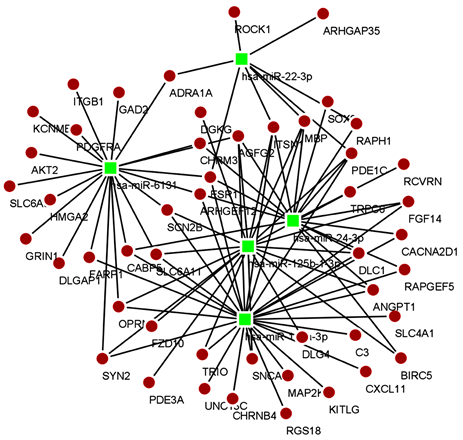 注:红色代表上调,绿色代表下调;方形代表miRNA,圆形代表mRNA (上调miRNA对应下调mRNA,下调miRNA对应上调mRNA)。
注:红色代表上调,绿色代表下调;方形代表miRNA,圆形代表mRNA (上调miRNA对应下调mRNA,下调miRNA对应上调mRNA)。
Figure 4. miRNA-Gene targeting regulatory network
图4. miRNA-Gene靶向调控网络
3.6. lnRNA-miRNA关系对和circRNA-miRNA关系对的预测
利用DIANA数据库获得lnRNA-miRNA关系对,选取Score = 1的lncRNA (见表3);利用ENCORI数据库中预测circRNA-miRNA关系对,然后与文献中和AD相关的circRNA取交集,得到重叠的circRNA (见表4)。

Table 3. Relationship between lncRNA-miRNA-mRNA
表3. lncRNA-miRNA-mRNA关系表

Table 4. Relationship between circRNA-miRNA-mRNA
表4. circRNA-miRNA-mRNA关系表
4. 讨论
AD是一种进行性神经退行性疾病,是全世界老年人痴呆的主要原因。尽管在研发关于预防和治疗AD的药物方面付出了巨大努力,但目前还没有有效的成果,这在个人、医疗和社会经济层面都造成了越来越大的负担。
通过对靶mRNA的作用,miRNA参与了许多细胞过程,包括增殖、凋亡、分化、衰老、应激和免疫刺激反应,以及癌症、心血管、糖尿病、AD和其他神经退行性过程等人类疾病 [10]。本研究共选取了10个高表达的miRNA (5个上调,5个下调)。
在本研究中发现,与对照组相比,AD患者的miR-125b显著下调。此外,在APP/PS1转基因小鼠模型中也发现循环miR-125b减少 [11]。在另一项研究中,Galimberti等人使用miRNA PCR阵列分析,他们发现miR-125b显著下调 [12]。在βamyloid (Aβ)病理状态下,miR-125b表达的降低是皮质神经元神经毒性效应的关键事件。miR-125b的异常表达可能是AD脑内神经功能障碍的原因之一。
且已有文献报道hsa-miR-22与hsa-miR-24在AD病人中低表达,与本研究中的发现一致:Jovicic等 [13] 指出miR-22在阿尔茨海默症患者中低表达,增强miR-22表达可能是治疗神经退行性疾病的合理治疗策略。Hu等 [14] 通过荟萃分析发现miR-24在AD患者的脑脊液中低表达。
在差异表达基因GO功能富集—生物学过程BP分析结果中,我们选取了18条与神经系统疾病相关的通路(如表1),对预测的靶向mRNA和通路筛选到的目标差异表达mRNA取交集,得到重合的差异表达基因共181个。
通过表3可发现,Estrogen Receptor 1 (ESR1)、Intersectin 1 (ITSN1)、Myelin Basic Protein (MBP)、Phosphodiesterase 1C (PDE1C)、Ras association and pleckstrin homology domains 1 (RAPH1)等上调基因均与hsa-miR-22和hsa-miR-24有对应关系,其中Bertram等报道,ESR1 PvuII和XbaI多态性与AD风险相关,通过系统荟萃分析,ESR1基因可能是AD发病的候选基因 [15]。
在基因中值得注意的还有DiscsLarge Homolog (DLG4)。DLG4与将谷氨酸受体锚定到突触后膜有关。DLG4的异常表达可能导致谷氨酸能神经传递的紊乱。此外,DLG4参与调节淀粉样蛋白b沉积 [16]。在我们的研究中,在AD患者中检测到上调的DLG4,DLG4在化学性突触传递、信号转导和三磷酸鸟苷环水解酶(GTPase)活性的正调控等方面发挥作用,且DLG4与两个下调miRNA hsa-miR-125b-1-3p和hsa-miR-125a-3p均有对应关系,表明其在AD中的重要作用,已有文献报道上调的DLG4可能作为AD的生物标志物 [17]。
此外,已有研究发现一个可以调节特定miRNA和突触功能的circRNA-CDR1-AS在AD大脑中表达下调 [8]。还有研究发现在人脑和视网膜中一种高度表达的circRNA ciRS-7 (cerebellar degeneration-related protein 1 antisense, CDR1as),它作为一种内源性、抗补体的miRNA抑制剂或“海绵”来抑制miRNA-7的正常功能 [18]。然而,在AD发病机制中通过其他机制发挥作用的circRNA (例如,作为蛋白质翻译模板、与蛋白质相互作用形成circ Ribonucleoprotein或作为mRNA陷阱的circRNA)仍需要进一步探索。
在过去的几年里,ceRNA假说已经被大量的实验所证实。然而,ceRNA机制及其相互作用网络的研究主要在癌症研究中进行 [19] [20]。近年来,研究人员开始系统地探讨ceRNA对特定神经退行性疾病的调控机制,由于ceRNA相互作用网络是多因素的,它们可能在这些复杂的神经退行性疾病的研究中具有优势;ceRNA network的构建也有助于识别新的基因调控分子机制,从而更好地理解各种AD的发病机制,并揭示新的治疗靶点和获得有关疾病病理过程的相关信息。
我们希望基于ceRNA的分析将成为预防、延迟发病、诊断和治疗阿尔茨海默病的可行思路。然而,这项研究有一些局限性。首先,需要对更大样本的患者进行全面和详细地分析,以进一步验证我们的发现。此外,还需要后续的相关实验研究来验证我们的结果。
基金项目
2021年省级大学生创新创业训练计划项目(NO: S202110092003; NO: S202110092004);河北省教育厅青年项目(QN2019099);河北省卫生厅重点科技研究计划(20200196)。
NOTES
*通讯作者。