1. 引言
肺癌是世界以及中国范围内发病率及死亡率最高的恶性肿瘤,其中85%为非小细胞肺癌,确诊时多数患者均为中晚期,失去手术治疗的机会。对于不可手术切除的肺癌且无驱动基因表达的患者,世界各大权威指南,如NCCN、CSCO,均推荐采取化学治疗为主的综合治疗,一线的经典化疗方案为含铂双药的化疗方案。顺铂(DDP)作为标准的铂类药物,在肺癌的治疗中占据较高的地位。然而顺铂耐药性的产生降低了顺铂的疗效,严重限制了顺铂的临床应用 [1],因此逆转顺铂耐药性或增强其化疗敏感性是目前临床上亟待解决的问题 [2]。益肺解毒方(YFJDF)为临床经验方,前期临床研究表明其可明显改善肺癌患者的临床症状,提高患者生活质量,延长生存时间。且益肺解毒方能够抑制人肺腺癌A549干细胞的生长,呈剂量依赖性,并与顺铂有协同增效作用。与顺铂联合应用时具有抑制A549细胞侵袭转移的能力,并且与两者单用比较明显增强,其作用机制可能主要为下调MMP2表达、上调E-cad表达 [3] [4]。本研究通过多种实验方法探讨益肺解毒方含药血清对人肺腺癌A549/DDP细胞株顺铂耐药性及凋亡相关蛋白的影响,以期为逆转顺铂耐药性提供新线索。
2. 材料与方法
2.1. 细胞株、动物及试剂
A549、A549/DDP细胞株购自中国医学科学院肿瘤研究所。SD大鼠购自上海杰思捷实验动物有限公司,雌雄各半,体重190~230 g,动物合格证号:SCXK(沪)2018-0004。益肺解毒方(YFJDF)购自南方医科大学附属齐齐哈尔医院制剂室制备,顺铂(DDP)购自江苏豪森药业股份有限公司。胎牛血清、1640培养基均购自Gibco公司,CCK-8试剂盒购自碧云天生物公司,Bcl-2、Bax单克隆抗体购于美国Abcam公司。
2.2. 方法
2.2.1. 益肺解毒方含药血清的制备
益肺解毒方由黄芪、北沙参、天冬、麦冬、女贞子、白术、茯苓、山药组成。加水浸泡30 min后,按汤剂常规方法煎熬,过滤并浓缩成生药量含量为10 g/ml的药液,冷却后装入灭菌药瓶,4℃保存。
将40只SD大鼠按24、48、96 g/kg/d的给药剂量随机分为:益肺解毒方低剂量(YFJDFL)组、益肺解毒方中剂量(YFJDFM)组、益肺解毒方高剂量(YFJDFH)组及空白血清组,每组各10只。各组分别灌注等体积的中药煎剂及生理盐水,每日灌胃2次,连续3日。末次给药后2 h,行腹主动脉取血,室温静置30 min,3000 r离心力下离心15 min,将同组血清收集混匀,56℃恒温水箱30 min灭活,0.22 μm微孔滤膜过滤除菌,分装,−20℃保存备用。
2.2.2. 细胞培养
A549细胞、A549/DDP细胞用含10%胎牛血清的RPMI 1640培养基,于37℃,湿度95%,5% CO2培养箱中培养和传代。
2.2.3. CCK8法检测顺铂、益肺解毒方及益肺解毒方 + 顺铂对A549、A549/DDP细胞的增殖抑制作用
取对数生长期的A549细胞或A549/DDP细胞,将细胞消化计数后接种于96孔板,细胞密度用相应培养基调整到2 * 104/mL,每孔加入150 μl细胞,设置3复孔。于37℃、5% CO2细胞培养箱中培养24 h后进行试验分组。按下列分组后分别再培养24 h、或48 h、或72 h后,每孔加15 μl的CCK8溶液,细胞培养箱内孵育2小时,450 nm测定OD值,保存数值。
A) 顺铂对A549、A549/DDP细胞的增殖抑制作用分组:空白对照组、顺铂(2、4、8、16、32 μg/mL)组。计算A549细胞和A549/DDP细胞培养48h的增殖抑制率、半数抑制浓度(IC50),A549/DDP细胞对顺铂的耐药指数。
B) 益肺解毒方对A549/DDP细胞的增殖抑制作用分组:空白对照组(NC组)、空白血清组、YFJDFL组、YFJDFM组、YFJDFH组。计算A549/DDP细胞培养24 h、48 h、72 h的增殖抑制率,选出益肺解毒方合适的干预时间及浓度剂量,用于后续实验。
C) 益肺解毒方 + 顺铂对A549、A549/DDP细胞的增殖抑制作用分组:YFJDF (筛选后剂量) + DDP (2、4、8、16、32 μg/mL)组。计算A549细胞和A549/DDP细胞培养48 h的增殖抑制率、半数抑制浓度(IC50),A549/DDP细胞对顺铂的耐药指数、益肺解毒方对A549/DDP的逆转耐药倍数。
计算细胞增殖抑制率 = (对照组OD值 − 实验组OD值)/(对照组OD值 − 空白组OD值) × 100%,实验数据以均值标准差方式描述并制作增殖抑制曲线折线图。应用SPSS 22.0软件计算半数抑制浓度(IC50),进而计算耐药指数 = A549/DDP的IC50值/A549的IC50,逆转耐药倍数 = 单独顺铂对A549/DDP的IC50值/(益肺解毒方 + 顺铂)对A549/DDP的IC50值。
2.2.4. 流式细胞术检测细胞凋亡
取对数生长期的A549/DDP细胞,以1 × 105 cells/mL浓度接种于75 cm2细胞培养瓶中,贴壁培养24 h后,分为NC组、空白血清组、DDP组、YFJDF组、YFJDF + DDP组,药物处理后继续培养48 h。流式细胞术检测各组细胞的凋亡情况。
2.2.5. Western blot法检测Bcl-2、Bax蛋白表达
取对数生长期的A549/DDP细胞,以1 × 105 cells/mL浓度接种于75 cm2细胞培养瓶中,贴壁培养24 h后,分为NC组、空白血清组、DDP组、YFJDF组、YFJDF + DDP组,药物处理后继续培养48 h。流式细胞术检测各组细胞的凋亡情况。按照试剂盒的说明书进行操作,检测Bcl-2、Bax蛋白表达水平。
2.2.6. 统计分析
应用SPSS13.0进行数据处理,t检验比较两组之间的差异。以P < 0.05定义为差异有统计学意义。
3. 结果
3.1. DDP对A549、A549/DDP细胞增殖抑制作用
2、4、8、16、32 μg/mL的DDP作用A549、A549/DDP细胞48 h后,结果显示,随着DDP浓度的升高对两种细胞的抑制作用逐渐增加(见表1、图1),差异具有统计学意义(P < 0.05)。计算DDP对A549、A549/DDP细胞的IC50值分别为4.49 μg/mL和45.09 μg/mL,计算出的耐药指数为10.05倍。
3.2. 益肺解毒方对A549/DDP细胞的增殖抑制作用
NC组、空白血清组、YFJDFL组、YFJDFM组、YFJDFH组分别作用24 h、48 h、72 h后,结果显示,随着益肺解毒方浓度的升高和药物作用时间的延长对A549/DDP细胞的抑制作用也逐渐增加(见表2、图2),差异具有统计学意义(P < 0.05)。根据以上结果,选择中剂量的YFJDF、并作用48 h用于后续逆转实验。

Table 1. Proliferation inhibitory rate of DDP impacting on A549、A549/DDP cells for 48 h ([ x ¯ ± S ]%, n = 6)
表1. DDP对A549、A549/DDP细胞48 h增殖抑制率([
]%, n = 6)
注:*P < 0.05。
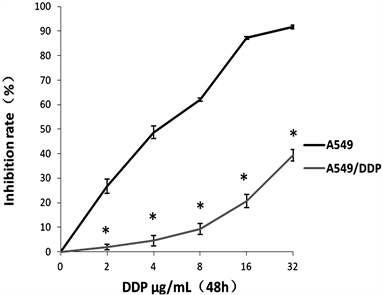 *P < 0.05,与A549组对比。
*P < 0.05,与A549组对比。
Figure 1. Proliferation inhibitory rate of DDP impacting on A549, A549/DDP cells for 48 h ([
]%, n = 6)
图1. DDP对A549、A549/DDP细胞48 h增殖抑制率([
]%, n = 6)

Table 2. Proliferation inhibitory rate of YFJDF impacting on A549/DDP cells ([ x ¯ ± S ]%, n = 6)
表2. 益肺解毒方对A549/DDP细胞增殖抑制率([
]%, n = 6)
注:*P < 0.05。
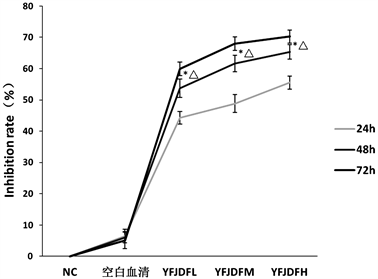 *P < 0.05,与24小时组对比,△P < 0.05,与72小时组对比。
*P < 0.05,与24小时组对比,△P < 0.05,与72小时组对比。
Figure 2. Proliferation inhibitory rate of YFJDF impacting on A549/DDP cells ([
]%, n = 6)
图2. 益肺解毒方对A549/DDP细胞增殖抑制率([
]%, n = 6)
3.3. 益肺解毒方协同顺铂对A549/DDP细胞的耐药逆转作用
YFJDF和不同浓度的DDP共同作用48 h,随着DDP浓度的增加对A549/DDP细胞的抑制率也逐渐增大。在同一个浓度作用下,YFJDF + DDP组比DDP组细胞的抑制率增加(见表3、图3),差异具有统计学意义(P < 0.05)。计算YFJDF + DDP组IC50值为29.37 μg/mL,与单独DDP组的IC50值45.09 μg/mL相比,逆转倍数为1.53倍。

Table 3. Proliferation inhibitory rate of YFJDF + DDP impacting on A549/DDP cells for 48 h ([ x ¯ ± S ]%, n = 6)
表3. YFJDF + DDP对A549/DDP细胞48 h增殖抑制率([
]%, n = 6)
注:*P < 0.05。
 *P < 0.05,与DDP组对比。
*P < 0.05,与DDP组对比。
Figure 3. Proliferation inhibitory rate of YFJDF + DDP impacting on A549/DDP cells for 48 h ([
]%, n = 6)
图3. YFJDF + DDP对A549/DDP细胞48 h增殖抑制率([
]%, n = 6)
3.4. 流式细胞仪检测益肺解毒方对A549/DDP细胞凋亡率的影响
流式细胞仪检测结果显示:与对照组相比各组细胞的凋亡率都增加,尤其联合用药组细胞凋亡率显著增加(见图4)。差异具有统计学意义(P < 0.05)。

Figure 4. Apoptosis rate of A549/DDP cell
图4. A549/DDP细胞凋亡率
3.5. Western blot检测益肺解毒方对A549/DDP细胞凋亡蛋白的影响
Western blot结果显示,与对照组相比,单独益肺解毒方组和单独DDP组,Bax的表达量均有不同程度的增加、Bcl-2的表达水平均有不同程度的降低(见图5),差异具有显著性(P < 0.05)。联合用药组相比单独顺铂组的Bax升高、Bcl-2降低更加明显,差异具有统计学意义。
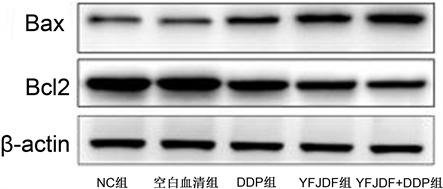
Figure 5. Expression of apoptosis-related proteins of A549/DDP cell
图5. A549/DDP细胞凋亡相关蛋白表达
4. 讨论
临床上,虽然靶向、免疫治疗开启了肺癌治疗的新时代,但对于无驱动基因表达、无PD-L1表达的非小细胞肺癌患者,化学药物治疗仍是基石,是主要的治疗方法。含顺铂的化疗方案在肺癌化疗的方案中,是标准的治疗方案,但是仍有一部分病人会出现治疗失败,主要原因在于肺癌细胞对顺铂耐药性的产生,成为肺癌化疗疗效难以提高的瓶颈。肿瘤耐药的机制十分复杂,相同肿瘤细胞的耐药可能是多种机制共同介导的,不同肿瘤细胞对同一种药物产生的耐药机制也不尽相同。中医药作为我国的瑰宝,已有几千年的历史,在逆转肿瘤耐药方面体现出了明显的优势,其存在多靶点、多阶段性的作用特点,且本身就具抗肿瘤特性,毒副作用较小。
中医学理论认为,痰、瘀、毒、虚是肺癌发生、发展过程中常见的病理因素,其正虚为本,邪实为标。气虚、阴虚、血瘀、痰湿、气滞、热毒证为肺癌患者常见的中医证型。张明萍等研究结果表明,化疗可以导致肺癌患者中医证型发生转变,化疗后气阴两虚证逐渐增加,说明化疗可耗气伤阴。益肺解毒方为孙玺媛博士自主研制的临床经验总结方,由黄芪、北沙参、天冬、麦冬、女贞子、白术、茯苓、山药组成。该方剂针对肺癌患者化疗后的气阴两虚证型拟定,其中方中黄芪补气固表,北沙参、天冬、麦冬、女贞子滋养肺胃肾阴,白术、茯苓、山药健脾益气。诸药合用,共奏益气养阴之效。另外现代药理学研究表明,黄芪 [5] 可以调节肿瘤微环境中NK细胞、T细胞的活性,并可显著改善肿瘤患者的免疫功能。北沙参 [6] 中的多糖能显著降低人肺癌细胞株增殖时间,并且通过抑制A549细胞的迁移和增殖诱导细胞凋亡。天冬 [7] 的单体及粗提物可抑制肿瘤细胞增殖并促进肿瘤细胞凋亡。麦冬 [8] 中的麦冬皂苷B可通过抑制髓鞘转录因子1及磷酸化组蛋白H3的表达,从而影响细胞周期的S及G2/M期,诱导细胞凋亡。女贞子 [9] 中的红景天苷可抑制肿瘤细胞增殖。白术 [10] 可诱导肿瘤细胞调亡,抑制肿痛细胞增殖,抑制肿瘤细胞的迁移、侵袭和转移,调节肿瘤细胞免疫反应,抑制肿瘤血管生成。茯苓可诱导细胞凋亡,阻滞细胞周期,抑制DNA拓扑异构酶活性,抑制肿瘤细胞的侵袭,逆转细胞耐药性。山药中的有效成分山药多糖能明显抑制4种肿瘤细胞的增殖与生长。以上现代药理研究显示,益肺解毒方所含中药,可能通过抑制肿瘤细胞增殖、调控肿瘤细胞周期、诱导肿瘤细胞凋亡、抑制肿瘤血管新生等途径,从而起到抗肿瘤作用。另外本研究前期的研究亦证实了,益肺解毒方能抑制人肺腺癌A549细胞的增殖并且与顺铂联合用药时,可显著增强顺铂的疗效 [3] [4]。
本研究结果表明,益肺解毒方对A549/DDP的增殖抑制作用呈剂量依赖性,并且可逆转A549/DDP对顺铂的耐药性。另外,益肺解毒方可诱导A549/DDP细胞凋亡,尤其是与顺铂联合应用时,可使细胞凋亡率显著增加,其作用机制可能是通过调节凋亡相关蛋白的表达。综上所述,益肺解毒方作为益气养阴的方剂,其抑制肿瘤增殖,改善顺铂耐药的机制以及明确具体靶点,值得继续挖掘,以期为益肺解毒方临床抗肿瘤应用提供确切的理论依据。
基金项目
齐齐哈尔市科学技术计划项目,项目编号:SFGG-201925;黑龙江省自然科学基金项目,项目编号:LH2019H123。
NOTES
*通讯作者。