1. 引言
锌是动植物生长发育过程中所必需的微量元素,其为维持生物的生命活动提供了重要的力量 [1] ,但是无机锌很难被生物吸收,而大部分被排泄到环境中,造成了极大的资源浪费和环境污染。复合氨基酸螯合物营养价值高,化学稳定性好,可以被高效吸收,同时氨基酸本身也可以作为营养物质被生物利用,是一种优良的动物食品添加剂 [2] [3] 。虽然目前国内外已有不少关于氨基酸螯合物的研究报道,却只是局限于一种氨基酸中,而且涉及范围较小,只是在少数的食品、药学等方面使用,另外,单一氨基酸的价格高昂,生产成本高,很难在实际生产中进行大范围推广 [4] [5] [6] 。
本文充分利用了我国丰富的废弃角蛋白资源与锌渣合成复合氨基酸螯合锌,极大程度的降低了原料成本,并用红外光谱对产物结构进行表征,证明实验得到了复合氨基酸螯合锌产物,同时利用EDTA滴定法和原子吸收分光光度法测定了复合氨基酸螯合锌的螯合率 [7] 。
2. 试验部分
2.1. 原料试剂与仪器
原料:锌渣:在生产除草剂敌草快时,需要采用大量的锌元素作为催化剂,而这些催化剂仅能使用一次,不可重复利用,通过对这些催化废液进行处理,可得到大量的锌渣,其锌含量大约为49.25%;复合氨基酸:动物皮毛及毛发等均含有丰富的角蛋白资源,经过水解获得复合氨基酸,其中甲硫氨酸含量为4.35%,丙氨酸含量为3.22%。
试剂:硫酸(98%国药集团化学试剂有限公司)、碳氨(AR上海阿拉丁生化科技股份有限公司)、PAN(1-(2-吡啶偶氮)-2-萘酚)指示剂、乙醇(≥ 99.5%,无水级,水分 ≤ 0.005%上海阿拉丁生化科技股份有限公司)、EDTA (乙二胺四乙酸)标准溶液(99.999%上海阿拉丁生化科技股份有限公司)
仪器:德国布鲁克INVENIO傅里叶红外光谱仪、江苏天瑞AAS8000原子吸收光谱仪。
2.2. 分析方法
1) EDTA滴定法计算螯合率
2) 原子吸收分光光度法测定螯合率
3) 红外光谱法产物结构表征
2.3. 试验方法
1) 本文的复合氨基酸来自于废弃的动物毛发,将这些废弃毛发清洗后在105℃~110℃条件下进行水解,水解过程中加入质量分数为50%的硫酸,然后加入碳氨,对体系进行中和,最后经过过滤、结晶和分离得到精制的复合氨基酸成品。详细的试验流程如图1所示。
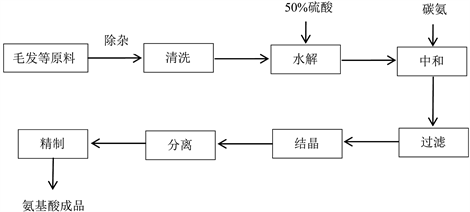
Figure 1. Using waste keratin to produce complex amino acids
图1. 废弃角蛋白制得复合氨基酸
2) 将1)中制得的复合氨基酸与含有锌离子的水溶液进行反应,浓缩后经过乙醇洗涤、抽滤和干燥,得到产物复合氨基酸螯合锌,制备试验过程如图2所示。

Figure 2. Preparing the complex chelated amino acidic zinc
图2. 制备复合氨基酸螯合锌
用98%浓硫酸溶液将锌渣溶解得到硫酸锌水溶液,将处理后的硫酸锌水溶液滴加到复合氨基酸水溶液中,将温度设置在85℃左右,反应2~3小时,将所得溶液放入适当容量的烧杯里,温度控制在80℃~85℃之间常压浓缩蒸发,蒸发量约为混合溶液总体积的1/2~2/3时即停止加热,加入乙醇水溶液(体积比应为3:1),加入量约为浓缩液总体积的1/2,降低溶液温度于0~5℃下,即有大量微晶产品析出,抽滤,采用乙醇水溶液漂洗晶体,离心分离干燥得到甲硫氨酸螯合锌和丙氨酸螯合锌。
3. 结果与分析
3.1. 螯合率测定
螯合率是指螯合物中有机物和无机物的比值,对于复合氨基酸螯合锌其螯合率就是螯合态锌含量与锌总量的比值,可以通过多种方法来测定复合氨基酸螯合锌的螯合率,本文采用EDTA滴定法和原子吸收分光光度法来测定复合氨基酸锌的螯合率。
1) EDTA (乙二胺四乙酸)滴定法
称取一定量的氨基酸螯合锌,溶于蒸馏水并定容至100 mL容量瓶,移取25 mL至250 mL锥形瓶中,先滴加3滴PAN(1-(2-吡啶偶氮)-2-萘酚)指示剂,用配置好的EDTA (0.02 mol/L)标准溶液滴定,消耗体积为V1,再称取等量的氨基酸螯合锌加50 mL乙醇提取,水浴加热并充分搅拌,离心分离后用蒸馏水清洗,定容到100mL容量瓶,移取25 mL至250 mL锥形瓶,滴加3滴PAN (1-(2-吡啶偶氮)-2-萘酚)指示剂,用相同浓度EDTA标准溶液滴定,消耗体积为V2。根据以下公式计算得螯合率。
式中:C——标准EDTA溶液的浓度,mol/L;
V2——滴定螯合态金属元素所消耗的EDTA溶液的体积,mL;
V1——滴定金属元素总量所消耗的EDTA溶液的体积,mL。
式中:C——标准EDTA溶液的浓度,mol/L;
V1——滴定金属元素总量所消耗的EDTA溶液的体积,mL;
M——金属元素的分子量,g/mol;
m——称取的样品量,g。
试验共对制备好的五个样品进行分析,根据消耗体积计算得到样品的螯合率,其结果如表1所示。

Table 1. The chelating rate determined by EDTA titration method
表1. EDTA滴定法测定螯合率
EDTA滴定法测定螯合率是用滴定螯合态金属消耗的EDTA溶液体积和滴定金属元素总量所消耗的EDTA的溶液体积之比来计算氨基酸的螯合率,而本次试验测得的螯合率在72.50%~78.10%之间,其相对标准偏差为2.79%。
2) 原子吸收分光光度法
通常原子吸收分光光度法与凝胶色谱法或者离子交换树脂法联用来测定螯合物的螯合率,用无水乙醇提取复合氨基酸螯合物后,再用原子吸收法测定螯合锌,其结果如表2所示。

Table 2. The chelating rate determined by atomic absorption spectrophotometer
表2. 原子吸收分光光度法测定螯合率
由原子吸收分光光度法测得的螯合率在73.10%~75.85%之间,其相对标准偏差为1.38%。
EDTA滴定法在配置标准溶液时,容易引入系统误差,同时,在滴定过程中,也存在偶然误差,这就造成EDTA滴定法的相对标准偏差高于原子吸收分光光度法,而偶然误差又无法通过多次测量来消除;另外,有可能氨基酸形成了多肽化合物,并非所有的氨基酸都参与了螯合反应,所以,整体的螯合率均偏低。
3.2. 红外光谱表征
1) 以甲硫氨酸为例

Figure 3. Schematic structure of methionine chelated zinc
图3. 甲硫氨酸螯合锌结构图
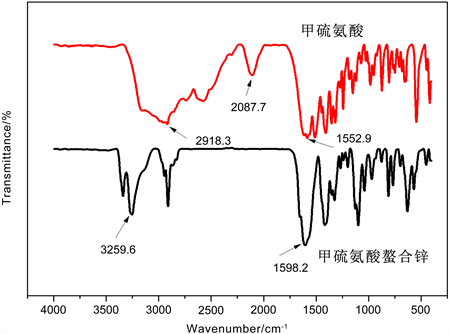
Figure 4. Infrared spectra of methionine and methionine chelated zin
图4. 甲硫氨酸及甲硫氨酸螯合锌红外谱图
由图4结合图3螯合甲硫氨酸锌结构图可知,螯合甲硫氨酸锌的红外吸收峰数量明显少于甲硫氨酸的吸收峰数目,说明产物在结构上的对称性增强,2087.7 cm−1是氨基酸的NH3+官能团中N-H键的拉伸和弯曲引起的氨基酸红外光谱特征峰,在游离的甲硫氨酸中该段有强烈吸收峰,而在产物中该峰消失,说明NH3+与Zn2+形成Zn-N配位键,产物中不再有NH3+官能团,同时,甲硫氨酸在2500 cm−1~3500 cm−1有宽的吸收峰,而甲硫氨基酸螯合锌仅在2800 cm−1~3000 cm−1有一个较窄的吸收峰,说明产物中已经没有游离的-OH,羧基的吸收峰由1552.9 cm−1红移至1598.2 cm−1,氨基吸收峰红移至3259.6 cm−1,这说明甲硫氨酸的氨基和羧基中的羟基氧与锌离子参与配位形成螯合物,-NH-键和C=O键发生了化学反应,锌与给电子的氮离子形成了配位键,又与给电子的羰基中的羟基氧配位形成五元环。
2) 以丙氨酸为例
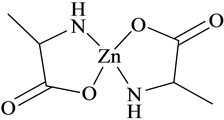
Figure 5. Schematic structure of alanine chelated zinc
图5. 丙氨酸螯合锌结构图

Figure 6. Infrared spectra of alanine and alanine chelated zinc
图6. 丙氨酸及螯合丙氨酸锌红外谱图
由图6结合图5螯合丙氨酸锌结构图可知,螯合丙氨酸锌的红外吸收峰数目明显少于丙氨酸的吸收峰数目,说明产物的对称性增强,而氨基酸在2110.2 cm−1处的特征峰消失,说明丙氨酸与金属锌离子发生了配位反应,而氨基在3077.7 cm−1处的吸收峰也红移至3305.3 cm−1,而羧基的特征峰由1586.9 cm−1红移至1620.9 cm−1,说明丙氨酸中氨基的氮原子与羧基上的羟基氧和锌离子形成了配位共价键,构成了稳定的五元环结构。
4. 总结
通过对废弃的角蛋白进行水解处理,获得高纯度的复合氨基酸,利用水溶液合成法制备复合氨基酸螯合锌;采用EDTA滴定法和原子吸收分光光度法测试了复合氨基酸螯合锌的螯合率,EDTA滴定法测试复合氨基酸螯合锌的螯合率的相对标准偏差为2.79%,原子吸收分光光度法的相对标准偏差为1.38%;对多种氨基酸螯合锌的结果进行了红外表征,通过谱图对比,特征峰数目发生变化且有明显位移,说明形成了目标产物。
基金项目
校企产学研联合科技攻关项目。
NOTES
*通讯作者。