1. 引言
硝酸咪康唑搽剂为广谱抗真菌药,主要含有硝酸眯康唑、乙醇和二甲基亚砜等成分,对皮肤癣菌、念珠菌等有抗菌作用,对某些细菌也有一定抑制作用。为了开发这一产品,我们按照《化学药物刺激性、过敏性和溶血性研究技术指导原则》([H]GPT4-1)做了硝酸咪康唑搽剂多次皮肤刺激性试验及皮肤过敏试验研究,报告如下:
2. 实验材料
2.1. 供试品及对照
硝酸咪康唑搽剂,襄樊隆中药业有限责任公司生产,批号:090404,规格和含量:供试品规格20 ml/瓶,含硝酸咪康唑:2%,数量60瓶(批号090404);高浓度含量供试品规格20 ml/瓶,含硝酸咪康唑:4%,数量60瓶(批号090404);性状:粉红色粘稠液体。保存条件:密闭,阴凉处保存。阴性对照:蒸馏水,自制。赋形剂对照,20 ml/瓶,不含硝酸咪康唑的赋形剂基质,数量60瓶(批号090404);由襄樊隆中药业有限责任公司提供。上市药物对照,硝酸咪康唑搽剂(阿特维斯(佛山)制药有限公司),规格20 ml/瓶,含硝酸咪康唑浓度:2%,数量60瓶,批号0807312。阳性对照品:2,4-二硝基氯苯(分析纯。上海化学试剂厂分装厂,批号050801)。
2.2. 试验动物
豚鼠,普通级,90只,雌雄各半,体重226~333 g,均由湖北省实验动物研究中心提供,生产许可证号为:SCXK(鄂)2008-0005。家兔单笼饲养,温度:24℃~28℃,湿度:60%~79%。光照时间明暗交替12小时。豚鼠饲养在普通级实验室,温度:24℃~27℃,湿度:64%~70%。光照时间明暗交替12小时。健康成年日本大耳白兔,普通级,24只,雌雄各半,体重2.03~2.28 kg。
3. 实验方法
3.1. 多次皮肤刺激性试验 [1]
3.1.1. 剂量设计
根据《化学药物刺激性、过敏性和溶血性研究技术指导原则(2005年)》要求,给药组设计2个浓度组,低浓度组为临床用药浓度,高浓度组为临床用药浓度的2倍。每只兔给予0.5 ml/次。
3.1.2. 给药方法
1) 准备皮肤
试验前24 h对试验兔背部两侧皮肤剃毛,每侧剃毛面积为3 cm × 3 cm左右,并用记号笔画出给药部位为2.5 cm × 2.5 cm区域。剃毛区左右各分一块;观察给药前动物皮肤表面有无红斑、破损、结痂等情况,如有,应另外更换试验兔背部其他区域皮肤。
破损皮肤制作:给予受试物前,用消毒的5号针头在破损皮肤组家兔剃毛区域划出井字,以皮肤出现渗血为度。
2) 给药部位
设置完整皮肤试验(A组)和破损皮肤试验(B组),完整皮肤给药组设置2个浓度组,低浓度组为临床用药浓度,高浓度组为临床用药浓度的2倍。同时设计阴性对照组,给予蒸馏水;赋形剂对照组,给予辅料;上市药物对照组,给予硝酸咪康唑搽剂(阿特维斯(佛山)制药有限公司)。每只兔给予0.5 ml/只次。剂量设置给药部位、给药量见表1、表2。

Table 1. Complete skin test grouping and related experimental information
表1. 完整皮肤试验分组及相关实验信息

Table 2. Grouping of damaged skin tests and relevant experimental information
表2. 破损皮肤试验分组及相关实验信息
3) 给药步骤
由助手固定试验兔,并使其俯卧,准确吸取0.5 ml各相应的受试物,均匀涂布于已经做好记号的2.5 cm × 2.5 cm受试区域,待药液稍干后,用玻璃纸覆盖后再取3 cm × 3 cm双层纱布,覆盖在该区域皮肤上,再在纱布上覆盖一层玻璃纸,并用透气胶带小心的固定受试部位,保持4 h。4 h后,小心撕去胶带,取下纱布,用温水清洗给药部位,在每次去除药物后1小时以及最后一次给药1、24、48和72小时肉眼观察并记录涂敷部位有无红斑和水肿等情况,并根据指导原则标准对红斑及水肿进行评分。皮肤刺激反应评分标准见表3。
4) 给药频率和时间
根据药物性质,最大疗程为4周,设计给药周期为4周,每天贴敷4 h,贴敷完毕后,除去受试物并用温水清洁给药部位。

Table 3. Scoring criteria for skin irritation response
表3. 皮肤刺激反应评分标准
3.1.3. 观察指标
1) 肉眼观察:观察动物物局部反应,包括红斑、水肿、充血程度及范围,并以计分的方式表示。同时观察动物的一般状态、行为、体征以及初末体重等。在每次去除药物后1小时以及再次贴敷前观察及记录红斑及水肿、涂敷部位是否有色素沉着、出血点、皮肤粗糙或皮肤菲薄情况及其发生时间及消退时间,并对红斑及水肿进行评分。末次贴敷后,在去除药物后1,24、48和72小时肉眼观察并记录涂敷部位有无红斑和水肿等情况。72小时观察后各组处死一半动物,取给药部位的皮肤组织作病理检查,留下一半动物观察恢复情况。
2) 组织病理学检查
在去除药物观察72小时及恢复期结束,将各组家兔处死,取皮肤组织,进行组织病理学检查。
3.1.4. 评分标准
每次每只动物皮肤刺激反应评分标准见表3,多次给药按下列方式计算每天每只动物平均积分。
皮肤刺激强度评价标准见表4。

Table 4. Criteria for evaluating skin irritation intensity
表4. 皮肤刺激强度评价标准
3.2. 皮肤过敏试验 [1]
3.2.1. 剂量设计
根据《化学药物刺激性、过敏性和溶血性研究技术指导原则》([H]GPT4-1)以及厂家提供的说明书,本品为液体制剂,试验时不需要稀释,直接取液体贴敷于实验动物皮肤表面,设供试品低、高浓度两个组,上市药物对照组,阴性对照组、赋形剂对照组和阳性对照组,阳性对照物为2,4-二硝基氯苯。其中,供试品低、高浓度组和上市药物对照组动物数为20只,赋形剂对照、阳性对照和阴性对照各10只,雌雄各半。致敏及激发剂量见表5。

Table 5. Dose setting and grouping of miconazole nitrate liniment in guinea pig skin allergy test
表5. 硝酸咪康唑搽剂对豚鼠皮肤过敏反应试验剂量设置及分组
3.2.2. 试验方法
1) 样品配制及给予
分别量取供试品低、高浓度,上市药物、赋形剂空白基质0.2 ml,均匀涂于2.0 cm × 2.0 cm的豚鼠皮肤上。
阳性对照组:致敏用1% 2,4-二硝基氯苯配制:将0.1 g 2,4-二硝基氯苯,溶于1:1丙酮和橄榄油的混合物10 ml中。吸取0.2 ml均匀涂于2.0 cm × 2.0 cm的豚鼠皮肤上;激发用0.5% 2,4-二硝基氯苯配制:将0.05 g 2,4-二硝基氯苯,溶于1:1丙酮和橄榄油的混合物10 ml中。阳性物现配现用。
2) 致敏
试验前24 h对豚鼠左侧肋腹部皮肤剃毛,剃毛范围约为2.0 cm × 2.0 cm。由助手固定豚鼠,操作者取量取好受试物,均匀涂抹于剃毛部位,然后用双层纱布覆盖受试部位,再用无刺激性胶布加以固定,贴敷时间为6小时。贴敷结束后,轻轻撕下胶带,去除受试物,并用温水将受试部位清洗干净。阳性对照组吸取1% 2,4-二硝基氯苯,均匀涂布于剃毛部位约2.0 cm × 2.0 cm范围,再覆盖双层纱布,用胶带固定,6 h后按同样的方法去除受试物。致敏次数为3次,分别为第0、7、14天。
3) 激发
按照同样的方法,于末次致敏后14天、第21天,对豚鼠致敏部位对侧相应部位进行激发给药,激发物和激发剂量见表1,去除受试物后24 h和4 8小时,按照表6要求对过敏反应进行评分,并记录评分结果。计算过敏反应发生率,按表7判定供试品的致敏强度。
4. 试验结果
4.1. 多次皮肤刺激试验试验结果
4.1.1. 一般情况观察
试验兔给药期间和给药结束后观察期内饮食均未见明显异常,精神状况良好。试验开始和结束时称取动物体重,动物体重无明显差异。

Table 6. Scoring criteria for skin allergy
表6. 皮肤过敏反应程度的评分标准

Table 7. Criteria for evaluation of skin sensitization
表7. 皮肤致敏性评价标准
4.1.2. 皮肤刺激反应情况
完整皮肤和破损皮肤组试验兔各12只,连续28天给予以下浓度受试物:供试品高浓度组(拟临床用药浓度2倍)、供试品低浓度组(拟临床用药浓度)、赋形剂对照组、上市药物对照组(阿特维斯(佛山)制药有限公司生产的硝酸咪康唑搽剂),阴性对照组(蒸馏水),按表6对每天给药前及每次给药后皮肤反应情况进行评分,结果硝酸咪康唑搽剂供试品低浓度、供试品高浓度、赋形剂以及上市药物、蒸馏水对照连续28天经皮给药以及恢复72小时恢复观察对家兔完整皮肤每天每只动物积分均值分别为:0.74、0.77、0.69、0.76、0.00,给药部位皮肤在停止给受试物后6天内基本都能恢复。硝酸咪康唑搽剂供试品低浓度、供试品高浓度、赋形剂以及上市药物、蒸馏水对照连续28天经皮给药以及恢复72小时恢复观察对家兔破损皮肤每天每只动物积分均值分别为:0.78、0.76、0.69、0.73、0.00,受试物在停止给药后第5天给药部位皮肤基本恢复,这表明供试品高浓度组、供试品低浓度组、赋形剂对照组、上市药物对照组在给药期间肉眼观察有轻度刺激性,停止给药6天内恢复正常。
病理组织学检查
给药期结束后病理组织学检查:赋形剂对照组、上市药物对照组、供试品低剂量组和供试品高剂量组均见到皮肤表皮层角质层略有增厚,恢复期末各组组织学检查均未见明显异常,表示病理已恢复,该供试品主要引起家兔皮肤表层角质化上皮增厚,赋形剂对照组、上市药物组、供试品低剂量组和供试品高剂量组之间病变性质和程度上均无明显差异,恢复期结束,各组均恢复正常。按照《皮肤刺激强度评价标准》,属轻度刺激性。阴性对照组(蒸馏水)肉眼观察及病理组织学检查均未见明显刺激性反应,按照《皮肤刺激强度评价标准》,属无刺激性。
4.2. 皮肤过敏反应
4.2.1. 一般症状观察
各试验组在致敏后饮食、精神状态均未见明显异常。阳性对照组在第二次致敏和第三次致敏后24 h均可见部分豚鼠致敏部位皮肤出现轻度红斑,供试品低剂量组、供试品高剂量组、上市药物对照组、赋形剂对照组和阴性对照组致敏后均未见明显异常。试验前后,给药各组与阴性对照组豚鼠体重比较均未见明显差异。
4.2.2. 过敏反应观察
各试验组于末次致敏后第14天激发,阳性对照组60%的豚鼠于激发后24 h在激发部位出现明显红斑,未见水肿,48小时未见消退;其他各试验组均未出现皮肤过敏反应,未见哮喘、战立不稳或休克等严重的全身性过敏反应出现,致敏率均为0%;在第一次激发后7天在右侧肋腹部进行第二次激发,阳性对照组100%的豚鼠于激发后24 h在激发部位出现明显红斑,未见水肿,48小时未见消退;其他各试验组均未出现皮肤过敏反应,未见哮喘、站立不稳或休克等严重的全身性过敏反应出现,致敏率均为0%,按照《皮肤致敏性评价标准》,赋形剂及供试品致敏性。过敏反应结果见表8、表9。本次研究结果表明,硝酸咪康唑搽剂对豚鼠过敏反应致敏发生率为0%,未见皮肤过敏反应。
5. 讨论
硝酸咪康唑1984年获准上市,商品名为“Lotrimin”,1989年由西安杨森公司引进中国市场,商品名为“达克宁” [2] 。硝酸咪康唑系一种广谱、高效、毒副作用小的咪唑类抗真菌药物,对大多数皮肤癣菌、酵母菌和放线菌等有良好的抗菌作用 [3] ,还对葡萄球菌、链球菌和炭疽杆菌等革兰阳性菌有抑菌作用 [4] ,市场上常用剂型有软胶囊剂、散剂和软膏剂等。有报道硝酸咪康唑乳膏对于新生儿臀红的治疗效果明显优于一般的常规治疗。缩短了住院天数,减轻了患儿家庭经济负担,具有可用性和实用性 [5] 。

Table 8. Skin allergy test of miconazole nitrate liniment in guinea pigs (first inspiration)
表8. 硝酸咪康唑搽剂豚鼠皮肤过敏试验结果(第一次激发)
注:分子表示发生例数,分母表示动物总数。

Table 9. Second stimulation results of skin allergy test in guinea pigs with miconazole nitrate liniment
表9. 硝酸咪康唑搽剂豚鼠皮肤过敏试验第二次激发结果
注:分子表示发生例数,分母表示动物总数。
这类产品临床上存在偶见过敏、水疱、烧灼感、充血、瘙痒或其他皮肤刺激症状。非常罕见血管神经性水肿、荨麻疹、湿疹、接触性皮炎、红斑、骨盆痛(痉挛)、阴道刺激、阴道分泌物和给药部位不适。
这类产品安全性引起人们的高度重视,在开发这类产品时应开展皮肤刺激性试验和过敏试验;本产品经过家兔皮肤刺激性试验证实有轻度刺激性:供试品高浓度组、供试品低浓度组、赋形剂对照组、上市药物对照组在给药期间肉眼观察有轻度刺激性,停止给药6天内恢复正常;病理组织学检查:给药期皮肤表皮层角质层略有增厚,恢复期各组均恢复正常,未见明显异常,按照《皮肤刺激强度评价标准》,属轻度刺激性。由于供试品高浓度组、供试品低浓度组、赋形剂对照组在给药期间肉眼观察有轻度刺激性,阴性对照组则无刺激性,可以排除由于人为操作引起的轻度刺激;供试品高浓度组、供试品低浓度组刺激反应无明显差异,无剂量反应关系,且与赋形剂对照组也无明显差异,不能排除各制剂刺激是用赋形剂引起的,因而开展赋形剂组方研究对减轻制剂的刺激有现实意义。豚鼠皮肤过敏试验表明:硝酸咪康唑搽剂过敏反应致敏发生率为0%,未见皮肤过敏反应。这些动物实验结果为这类产品开发上市提供安全性实验依据。
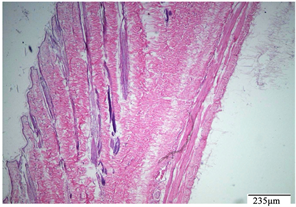
Figure 1. Negative control group, intact skin
图1. 阴性对照组,完整皮肤
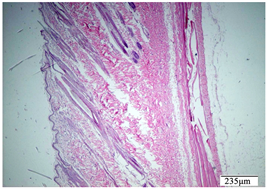
Figure 2. Negative control group, damaged skin
图2. 阴性对照组,破损皮肤
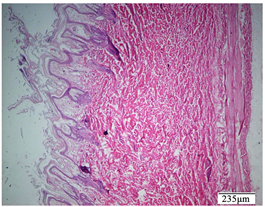
Figure 3. Excipient control group, intact skin
图3. 赋形剂对照组,完整皮肤
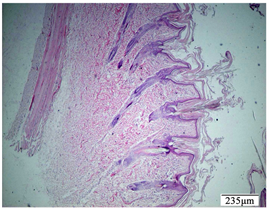
Figure 4. Excipient control group, damaged skin
图4. 赋形剂对照组,破损皮肤
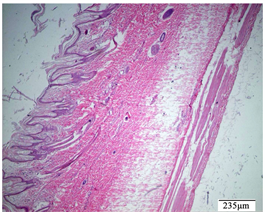
Figure 5. Control group of marketed drugs, intact skin
图5. 上市药物对照组,完整皮肤
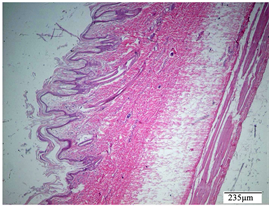
Figure 6. Control group of marketed drugs, damaged skin
图6. 上市药物对照组,破损皮肤
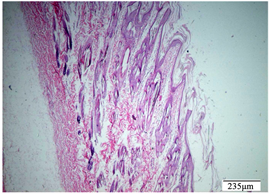
Figure 7. Low dose group, intact skin
图7. 供试品低剂量组,完整皮肤
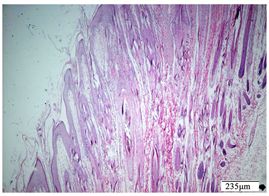
Figure 8. Low dose group, damaged skin
图8. 供试品低剂量组,破损皮肤
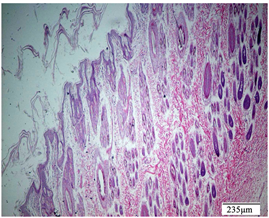
Figure 9. High dose group, intact skin
图9. 供试品高剂量组,完整皮肤
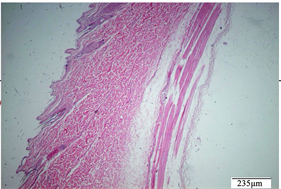
Figure 11. Negative control group, intact skin
图11. 阴性对照组恢复期,完整皮肤
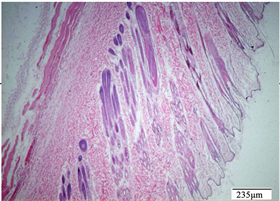
Figure 12. Negative control group, damaged skin
图12. 阴性对照组 恢复期 破损皮肤
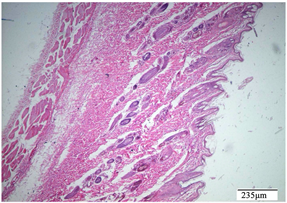
Figure 13. Excipient control group, intact skin
图13. 赋形剂对照组恢复期,完整皮肤
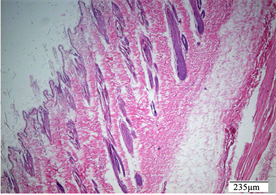
Figure 14. Excipient control group, damaged skin
图14. 赋形剂对照组恢复期,破损皮肤
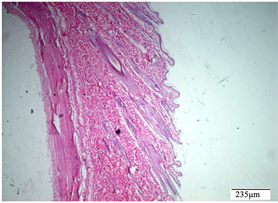
Figure 15. Control group of marketed drugs, intact skin
图15. 上市药物对照组,完整皮肤
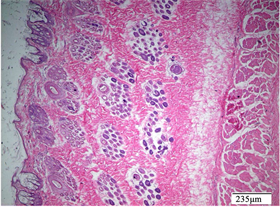
Figure 16. Control group of marketed drugs, damaged skin
图16. 上市药物对照组,破损皮肤
附多次皮肤刺激实验病理图:其中给药期结束多次皮肤刺激病理图(见图1至图10),恢复期结束多次皮肤刺激病理图(见图11至图20)。
NOTES
*通讯作者。