1. 引言
氧化铈由于具有独特的立方晶系萤石型晶体结构和储氧能力,广泛应用于发光材料、催化剂、紫外吸收剂等领域 [1] [2] [3] 。但是由于电子禁带宽度大(2.94 eV) [4] ,可见光利用率低,极大限制了氧化铈的应用。通过掺杂以减小氧化铈的禁带宽度,成为近年来研究的热点之一 [5] 。在氧化铈中掺杂的元素除了过渡金属元素如Fe,Ni,Cu等外 [6] ,稀土元素的掺杂氧化铈研究的较多。
K. Krishna等(2007)研究了稀土La,Pr,Sm,Y改性二氧化铈的物理化学性质 [7] 。S. V. Chavan等(2008)合成了Gd,Sm掺杂的纳米晶二氧化铈粉末 [8] 。贺素姣等(2016)得到了Gd3+离子掺杂CeO2,并研究了其离子电导率 [9] 。
在稀土元素中,La3+和Ce4+离子半径十分接近,分别为1.061 × 10−10 m和0.94 × 10−10 m [10] ,但存在电荷差异,因此La3+的掺杂引起了广大研究者的兴趣。研究表明,La3+掺杂氧化铈以氧化铈固溶体的形式存在,可保持氧化铈的萤石立方型晶体结构类型 [11] [12] [13] [14] 。Basu指出La3+掺杂后可影响氧化铈的晶面生长方向 [11] 。A. Bueno-López等(2005)证实La3+阳离子能取代CeO2晶格中的Ce4+阳离子形成固溶体 [15] 。当La3+掺杂量达到30% [16] ,40% [17] ,50% [18] 后,萤石立方晶体结构仍然可以维持。但是在50%掺杂条件下,压力超过22.6 GPa会破坏其晶体稳定性 [18] 。Gong. W等发现只要La含量不超过80%,Ce-La合金被氧化后均形成CeO2为基的固溶体 [19] 。
镧离子的半径大于铈离子的半径,是造成氧化铈晶格畸变的主要原因 [20] 。A. Rangaswamy等(2015)研究表明,掺杂La后的CeO2材料表现出较小的微晶尺寸,具有比纯CeO2更高的BET表面积 [17] 。Wang L也证明掺杂后,氧化铈的结晶性会变差,晶粒更细小 [17] [21] 。Hou X等(2016)将La3+引入CeO2中后在高温条件下不仅可以细化晶粒,还可以稳定主体晶格,认为La能阻碍烧结 [22] 。
掺镧氧化铈应用于光催化降解有机染料方面的报道较少。马娟宁考察了La掺杂CeO2在300 W紫外灯照射下,添加H2O2作为电子捕获剂,对亚甲基蓝溶液的降解情况 [23] 。尽管30% La掺杂CeO2表现出较好的效果,但所用光源功率过大,而且在紫外灯照射下H2O2自身对亚甲基蓝也有较强的降解作用,不能因此认定La掺杂能提高氧化铈的光催化效果。
前人对La掺杂氧化铈的研究主要集中在晶胞。在晶体结构变化研究中,普遍认为La的掺杂都会使得CeO2的晶胞膨胀,晶格常数变大以及晶粒尺寸更细小,但是对禁带宽度及光催化活性的研究较少,因此本文分析晶体结构变化,着重研究了La掺杂对氧化铈禁带的变化,并以光催化降解实验验证禁带宽度与光催化降解效率的关系。
2. 实验
2.1. 原料
Ce(NO3)3∙6H2O,La(NO3)3∙6H2O,纯度均为99.99%,四川科龙试剂有限公司;NaOH,分析纯,四川科龙试剂有限公司;蒸馏水,实验室自制。
2.2. 过程
采用水热法合成镧掺杂的氧化铈。按照摩尔比(Ce:La = 10:0, 8:2, 5:5, 2:8, 0:10)称量六水硝酸铈(Ce(NO3)3∙6H2O),六水硝酸镧(La(NO3)3∙6H2O),加入蒸馏水,置于磁力搅拌器上搅拌使其溶解,得到混合稀土溶液。称量一定量的固体NaOH加蒸馏水溶解后,在磁力搅拌作用下,将硝酸稀土溶液缓慢滴加到NaOH溶液中,继续搅拌20 min后转移至内衬为聚四氟乙烯(容积100 ml)的水热反应釜中,定容75 ml。将反应釜置于一定温度的烘箱中反应一段时间后冷却取出。将水热反应后得到的悬浊液用去离子水抽滤洗涤,重复三次后,放入温度为120˚C烘箱中干燥12 h。最后在400˚C马弗炉中热处理2 h,取出研磨得到产物。
2.3. 表征
本文中样品的物相、晶体结构、晶化程度分析采用丹东方园DX-2700型X射线粉晶衍射分析仪,其中CuKα射线,λ = 0.154184 nm,扫描范围2θ = 20˚~80˚,管电流30 mA,管电压40 kV,扫描速度0.05˚/min。试样微观形貌采用FEI Inspect F50型场发射扫描电子显微镜表征,加速电压为10 kV。测试前对试样镀金处理以减少电荷累积。用扫描电镜自带的OctaneSuper型能谱仪(EDAX公司)对样品进行成分测试。
紫外吸收光谱采用安捷伦CARY 5000型紫外-可见-近红外分光光度计进行测定,以BaSO4粉末为参比,扫描范围200~700 nm。样品的光降解性能以紫外光催化降解亚甲基蓝(5 mg/L)来表征。光源采用功率35 W,波长253.7 nm的低压汞灯。量取100 ml亚甲基蓝溶液置于100 ml的烧杯中,并加入合成的铈镧稀土氧化物粉末0.1 g,在黑暗环境中,避光搅拌30 min,使粉末在溶液中达到吸附-脱附平衡。然后置于汞灯下光照,同时用磁力搅拌器搅拌。取样时间间隔1 h,将所取得的上层清液进行离心分离,转速为4000 r/min,离心5 min。离心得到的上层清液,利用紫外可见分光光度计测定665 nm处亚甲基蓝特征波长的吸收率A,并通过公式D = (1 − A/A0) × 100%计算相应的降解率D。
3. 结果与讨论
3.1. 掺杂CeO2粉体的XRD分析
图1显示的是不同镧铈摩尔比产物的XRD图,其中Ce:La = 10:0和Ce:La = 0:10产物的衍射峰分别与CeO2标准卡片(编号为PDF#34-0394)和La2O3标准卡片(PDF#05-0602)的特征峰对应,无其他杂峰产生,说明实验获得的是纯度较高的氧化铈(空间群:Fm-3m (225))和氧化镧(空间群:P-3m1 (164))。当镧掺杂浓度从0%提高到80%,产物的物相与氧化铈一致,在80%掺杂量下,即镧铈摩尔比为4:1时,产物仍然

Figure 1. XRD patterns of different molar ratios
图1. 不同镧铈摩尔比的XRD图
保持着CeO2的萤石立方晶体结构类型。这与姜银举等研究结果一致:当镧的摩尔分数在5%~85%范围内时,铈镧稀土氧化物CeO2-La2O3都是以CeO2面心立方结构存在 [24] 。
从图1还可以看出,随着镧浓度的增大,XRD衍射峰的峰强度逐渐变弱,半高宽变大,CeO2的结晶性变差。这是因为La3+的离子半径为1.061 × 10−10 m,Ce4+的离子半径为0.94 × 10−10 m,三价稀土La3+与四价的Ce4+的离子半径差异达到13.29%,而且不等价离子的替换会造成氧空位,从而影响晶体的完整性。因此过的La必然阻碍CeO2的结晶,从而导致衍射峰变宽。
图2显示的是样品在2θ角为25~35之间的精细扫描图。如图2所示,特征衍射峰明显向低角度方向发生偏移,而以上XRD图都是在相同的实验测试条件下得到的,纯的氧化铈最强峰角度为28.60˚,随着镧掺入量的增加,依次偏移到了28.05˚,27.45˚,26.75˚由于面心立方八面体间隙大于面心立方四面体间隙,因此无论是以全部为铈离子还是以氧离子为主的八面体,La3+离子半径(1.061 × 10−10 m)都远大于此八面体间隙(Ce为主的八面体间隙为0.94 × 10−10 m × 0.414 = 0.389 × 10−10 m;氧原子为主的八面体间隙为0.66 × 10−10 m × 0.414 = 0.275 × 10−10 m),因此La3+很难进入晶格间隙形成间隙固溶体。
La3+的离子半径为1.061 × 10−10 m,Ce4+的离子半径为0.94 × 10−10 m,O2-离子半径为1.43 × 10−10 m,因此无论从离子半径还是电荷平衡的角度,La3+更容易取代Ce4+,形成置换固溶体,最终形成以氧化铈为基体的萤石立方晶体结构。随着镧的掺杂浓度增大,衍射峰向低角度偏移的角度也随之增大。这是因为La3+离子半径比Ce4+大,取代会造成晶格膨胀。根据布拉格公式2dsinθ = nλ可知,晶面间距的增大必然导致CeO2的衍射峰向低角度偏移。
用软件Jade6.5对上述粉体的晶格常数、晶胞体积、晶面间距进行了拟合计算,
结果见表1。如表1所示,水热法合成得到的纯CeO2晶体常数a实测值为0.5416 nm,与理论值0.5411 nm相近;纯CeO2晶体的d111和d220晶面间距分别为0.3142 nm和0.1923 nm,晶粒尺寸为92 nm。

Figure 2. XRD patterns of certain range of fine scanning
图2. 样品一定角度范围精细扫描XRD图

Table 1. Crystal parameters of the CeO2 doped by different content of La ion
表1. 不同La离子掺杂后CeO2的晶体参数
随着La含量的增加,晶面间距总体上呈现缓慢增大的趋势,晶格常数也在增大,依次为5.459 Å、5.633 Å、5.701 Å,尤其是掺镧80%时的晶格常数与纯的氧化铈相比,晶格膨胀了5.3%。而晶粒尺寸随着La含量的降低而逐渐减小,依次为92 nm、80 nm、67 nm、51 nm,掺镧80%时晶粒尺寸相对纯CeO2减小了44.5%。
3.2. 能谱分析
将50% La-CeO2样品进行能谱分析,图3(a)为EDX分析所选取的区域,图3(b)为相应的谱图和元素结果。
由能谱分析可以看出,样品中主要的元素为氧、镧和铈,不含有其他杂质元素。且镧铈的摩尔比接

Figure 3. Selected region (a) and EDX spectrum (b) of the 50% La-CeO2 sample
图3. (a) 点分析所选区域;(b) 元素含量
近1:1,与实验投料量吻合。而XRD图谱分析表明,对50% La-CeO2,XRD没有检测到氧化镧的特征峰。结合EDX和XRD,说明镧已掺杂入氧化铈晶格,并以固溶体的形式存在。
3.3. SEM分析
由图4可以看出,不同La掺杂量的氧化铈样品都存在颗粒团聚,但是一次颗粒尺寸在100 nm以下。晶粒呈现近球形。在相同放大倍数下,随着La3+浓度的提高,颗粒之间的界线越来越模糊,且粒径越来越小。说明La3+的掺入会抑制CeO2的结晶,阻碍氧化铈晶体的形核和长大,这与XRD计算所得的晶粒尺寸结果一致。实验中,硝酸铈盐与碱NaOH反应先形成的是六方晶型的Ce(OH)3和La(OH)3。在实验水热条件下,La(OH)3不能转化为La2O3,因此La会以取代Ce的形式进入氧化铈晶格。但是La的掺杂会导致氧化铈晶格畸变和晶格能量升高,使得体系不能稳定存在。氧化铈晶粒越大,晶格畸变能越大,体系越不稳定。相反,当掺杂氧化铈以较小的粒径存在时,可以减小晶格畸变能,有利于晶格的稳定。
3.4. 紫外可见漫反射分析
对掺杂氧化铈固溶体进行紫外漫反射光谱分析,可以用来考察掺杂离子对结构的影响及材料能隙的变化情况。
从图5可以看出,紫外吸收值随着La含量上下摆动:纯的CeO2和50% La-CeO2的紫外吸收较强,而20% La-CeO2和80% La-CeO2的紫外吸收弱,但两者的紫外吸收峰形状十分相近。这表明紫外吸收强弱和蓝移程度均存在一个掺杂极限值。
在可见光范围(390~780 nm)内,不同掺杂浓度样品的紫外可见漫反射光谱趋势与纯CeO2的图谱基本相同,从波长480 nm开始吸收,吸收在270 nm~370 nm达到峰值。随着掺杂浓度的增大,吸收边逐渐向低波长方向移动,而当达到掺杂量50%时,吸收边随着掺杂量的增加又出现了红移的现象。当掺杂量继续增加到80%时,又出现了蓝移。在吸收范围(200~700 nm)内,光谱总体呈现出先蓝移后红移再蓝移的现象,与张国芳的研究结果一致 [20] 。一方面是Ce3+和Ce4+价态转变中,引起了静电势效应导致带隙的蓝移 [25] ;另一方面是因为La的掺入造成晶格畸变,影响相应的吸收性能 [26] 。
由于CeO2的带间跃迁方式为直接跃迁。为了估算样品的禁带宽度值,釆用(Ahv)2对hv作图(图6),其中A代表吸收率,hv代表光子的能量,单位为eV。反向延长插图中线性部分的曲线与X轴交点的
值即为样品的直接半导体禁带宽度。结果表明,纯氧化铈的禁带宽度为3.074 eV,而20%、50%及80% La掺杂的氧化铈,禁带宽度分别为3.115、3.087、3.127 eV。禁带宽度的变化,引起了吸收边的红移或者蓝移,主要来源于量子尺寸效应和杂质能级效应的协同影响。随着La掺入量的增加,粒度减小,

Figure 4. SEM images of cerium lanthanum rare earth oxides with different La concentrations (a): 0%, (b): 20%, (c): 50%, (d): 80%, (e): 100%
图4. 不同掺La浓度(a):0%,(b):20%,(c):50%,(d):80%,(e):100%铈镧稀土氧化物的SEM图

Figure 5. Ultraviolet-visible diffuse reflectance spectra of cerium oxide doped with different lanthanum concentrations
图5. 不同镧浓度掺杂的氧化铈紫外可见漫反射光谱
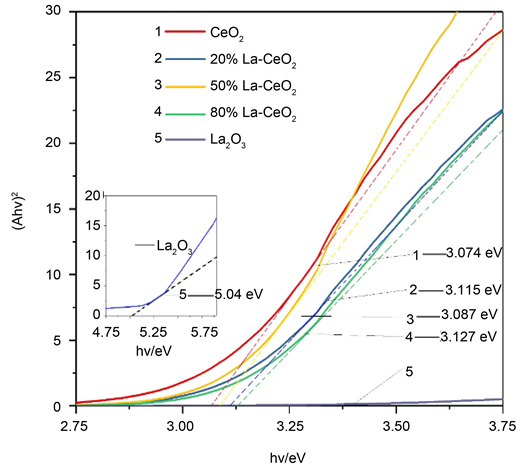
Figure 6. Functions of hv and (Ahυ)2 of cerium oxide: (1. La-0%, 2. La-20%, 3 La-50%, 4. La-80%, 5. La-100%)
图6. 氧化铈的hv和(Ahυ)2的函数关系图:(1. La-0%, 2. La-20%, 3 La-50%, 4. La-80%, 5. La-100%)
量子尺寸效应会引起能隙增大 [27] 。同时由于掺杂浓度逐渐增大,晶格缺陷逐渐增多,引起缺陷能级及杂质能级效应,激发态与基态能带变小,导致分子内电荷分布发生变化,此时杂质能级会使得能隙变小。在两种相反作用的影响下,出现了掺杂氧化铈禁带宽度随着La的浓度不同而呈现先增大后减小再增大的情况。因此La3+的掺入会造成CeO2禁带宽度和紫外吸收强弱的变化。
为了验证能带间隙的变化,将水热合成的样品用于光催化性能测试。以亚甲基蓝溶液(5 mg/L)模拟有色染料废水进行光催化降解,其降解率与光反应时间关系如图7所示。
从图中可以看出,随着光催化反应时间的延长,掺杂La3+的CeO2降解亚甲基蓝的降解率逐渐增大。当反应时间为5 h时,降解率最大的催化剂为纯的CeO2 (35%),其次为掺杂50%的氧化铈(32%),掺杂20% La3+和掺杂80% La3+的CeO2降解率较小,分别为24%和15%。纯La2O3开始1 h有9%,到8小时后仅为11%,其降解效果最差。考虑到紫外灯下空白对照对亚甲基蓝的降解率有2%,可以认为纯La2O3只有吸附效果,吸附率为9%。这是因为纯La2O3的禁带宽度达到5.04 eV,对应的波长为216 nm,而实验使用的紫外灯波长为254 nm,光子能量不足以激发产生氧空位,从而只能表现为吸附,而无光催化功能。
而掺La氧化铈粉末具有一定的光催化活性,其光催化性能与紫外漫反射的结果是一致的,即禁带宽度最小(3.074 eV)的氧化铈光催化效果最好,而禁带宽度最大(3.127 eV)的80% La-CeO2氧化铈光催化效果最差。实验结果表明,要获得好的光催化性能,需要调节氧化铈的禁带宽度,使其尽量趋近于所用的光源波长。而掺杂La并非是完全有利于其光催化性能,需要调节掺杂量来满足实际需求。
4. 结论
本文采用水热法制备了纯的氧化铈和氧化镧以及不同铈镧比例的稀土氧化物。

Figure 7. Degradation of methylene blue solution with different La3 + doped CeO2
图7. 不同La3+掺杂浓度的CeO2对亚甲基蓝溶液的降解
1) XRD表明所制备的镧掺杂的稀土氧化物均为立方萤石型结构的氧化铈,在80% La掺杂情况下,仍然具有较强的特征衍射峰。La的掺入使得衍射峰向低角度偏移,半峰宽变宽,计算结果证实La造成氧化铈晶格膨胀和晶粒尺寸减小。
2) SEM表明,样品呈现类球形的纳米颗粒,且粒径随着镧含量的增加而减小,EDX分析表明所得产物纯度高,成分与实验设计一致。
3) 紫外可见漫反射光谱表明La3+的掺入会造成CeO2禁带宽度和紫外吸收强弱呈规律变化:50% La掺杂的氧化铈禁带宽度比20%和80% La掺杂样品小而吸收值大,但均不及纯氧化铈。
4) 对亚甲基蓝溶液的光催化实验也证实,纯氧化铈样品的光降解率最大,其次为50% La掺杂,而纯氧化镧因为禁带宽度最大,只有吸附作用。
资助信息
四川省科技支撑计划项目(项目编号:2015GZ0054,2017GZ0400)。